Файл: 6,3694. значения коэффициентов m и n определить в зависимости от параметров f и vм f 1000 f 1000 3,245.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.02.2024
Просмотров: 29
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Практическая часть
Задача 1.Расчет концентрации вредного вещества в приземной области атмосферы, при выбросе нагретой газовоздушной смеси из трубы промышленного предприятия.
Ответ.
Максимальное значение приземной концентрации вредного вещества Cm, мг/м3 при выбросе нагретой газовоздушной смеси из одиночного точечного источника с круглым устьем при неблагоприятных метеорологических условиях определяется по формуле:
СМ =
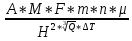
Берем исходные данные из приложения №8:
A = 140; F = 1; Q = 3,2; ∆T = 16; H = 25; D = 0,8; М=0,9
Для определения Cm необходимо:
1. Рассчитать среднюю скорость w0, м/с выхода газовоздушной смеси из устья источника выброса:
w0 =
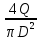
w0 =
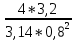 = 6,3694.
= 6,3694.2. значения коэффициентов m и n определить в зависимости от параметров f и vм:
f = 1000*
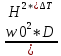
f = 1000*
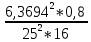 = 3,245.
= 3,245.vм = 0,65*
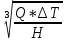
vм = 0,65*
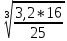 = 0,825.
= 0,825.3. Коэффициент m определить в зависимости от f по формуле:
m =
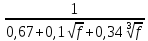
m =
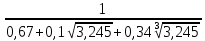 = 0,739.
= 0,739.4. Коэффициент n определить в зависимости от величины vм:
n = 1 при vм ≥ 2
n = 0,532 vм 2 - 2,13 vм +3,13 при 0,5 ≤ vм < 2
n = 4,4 vм при vм < 0,5
n = 0,532 vм 2 - 2,13 vм +3,13 = 0,532*0,8252-2,13*0,825+3,13 = 1,735.
5. Расстояние от источника выброса xm, м, на котором при неблагоприятных метеорологических условиях достигается максимальная приземная концентрация вредных веществ определяется по формуле:
xm =
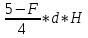
где d – безразмерный коэффициент, определяемый по формуле:
d = 4,95* vм*(1+0.28
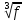 )
)d = 4,95*0,825*(1+0,28
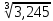 ) = 5,774.
) = 5,774.xm =
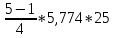 =144,356
=144,356Вычисляем СМ:
СМ =
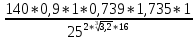 = 0,069 – максимальное значение из одиночного точечного источника.
= 0,069 – максимальное значение из одиночного точечного источника.Определим фактическую концентрацию вредного вещества у поверхности земли с учетом фонового загрязнения воздуха по формуле:
См’ = См+Сф
См’ = 0,069+0,03 = 0,099 - фактическая концентрация вредного вещества у поверхности земли с учетом фонового загрязнения воздуха.
Данная концентрация не превышает максимальную разовую предельно допустимую концентрацию (0,6 мг/м3), и превышает среднесуточную (0,06 мг/м3).
Рассчитаем концентрацию загрязнителя на расстоянии x1 и x2 от источника выброса по формуле:
СX = Сm*SX, где SX – коэффициент, зависящий от величины
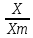
Дано: x1 = 100; x2 = 500
Вычисляем СX1:
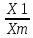 =
= 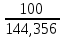 = 0,692 < 1
= 0,692 < 1SX1 =
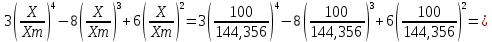
= 0.907
СX1 = 0,099*0,907 = 0,089
Вычисляем СX2:
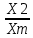 =
= 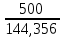 = 3,463 1<
= 3,463 1<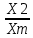 <8
<8SX2 =
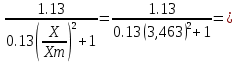 0.445
0.445СX2 = 0,099*0,445 = 0,044
Определим фактическую концентрацию вредного вещества у поверхности земли с учетом фонового загрязнения воздуха по формуле:
Сх’ = Сх+Сф
Сх1’ = Сх1+Сф = 0,089+0,03 = 0,119
Сх2’ = Сх2+Сф = 0,044+0,03 = 0,074
Данные концентрации не превышают максимальную разовую предельно допустимую (0,6 мг/м3), однако превышают среднесуточную (0,06 мг/м3) концентрации.
Задача 2.Оценка загрязнения атмосферного воздуха отработанными газами автотранспорта на участке магистральной улицы (по концентрации CO).
Ответ.
Формула оценки концентрации окиси углерода (Сco):
CCO = (СCФ+0,01*N*KT)*КA*КУ*КС*КВ*КП
Коэффициент токсичности автомобилей определяется как средневзвешенный для потока автомобилей по формуле:
KT = ∑PI*KTI
Пусть на некотором участке магистральной улицы состав движения для легкого грузового транспорта – 15%, KTI = 2,3
среднего грузового транспорта – 0%, KTI = 2,9
тяжелого грузового транспорта – 0%, KTI = 0,2
автобуса – 5%, KTI = 3,7
легкового транспорта – 80%, KTI = 1,0
тогда коэффициент токсичности автомобилей на данном участке:
KT = 0,15*2,3+0*2,9+0*0,2+0,05*3,7+0,8*1,0 = 0,345+0+0+0,185+0,8=1,33
Данные для формул берем согласно шифра из приложений № 11-16:
СCФ = 0,03; N = 500; КA = 1,0; КУ = 1,55; КС = 1,05; КВ = 1,15; КП = 2,0
Вычисляем:
CCO = (0,03+0,01*500*1,33)*1,0*1,55*1,05*1,15*2,0 = 25,004 мг/м3
Выброс на данном участке дороги превышает разовую максимальную дозу (5 мг/м3) и суточную (3 мг/м3).
Предложения:
1. Увеличение зеленых насаждений.
2. Установка светофоров с вызывными фазами.
Задача 3.Опишите основные химические, физические и опасные свойства фенол, напишите соответствующие уравнения химических реакций.
Ответ.
Фенол (гидроксибензол, химическая формула - C6O6OH) - органическое соединение, возглавляющее класс фенолов. Токсичен, является сильным ирритантом (группа веществ, вызывающих при попадании сильное местное раздражение слизистых оболочек, кожных покровов и расположенных в них нервных рецепторов с формированием ответной рефлекторной защитной реакции организма направленной на устранение раздражающего вещества (зуд, жжение, боль, першение, слезотечение, чиханье, кашель).
Физические свойства:
Представляет собой бесцветные игольчатые кристаллы, розовеющие на воздухе из-за окисления, приводящего к образованию окрашенных веществ (это связано с промежуточным образованием хинонов). Обладает специфическим запахом (таким, как запах гуаши, так как в состав гуаши входит фенол). Умеренно растворим в воде (6 г на 100 г воды), в растворах щелочей, в спирте, в бензоле, в ацетоне. 5%-й раствор в воде — антисептик, широко применявшийся в медицине в прошлом.
Химические свойства:
Фенол проявляет кислотные свойства, поэтому в водных растворах он диссоциирует по типу кислоты с образованием протона водорода, поэтому фенол называют карболовой кислотой.
Фенол, как и спирты, взаимодействует со щелочными металлами. Так, в реакции фенола с натрием образуется фенолят натрия и водород.
Фенол реагирует с растворами щелочей, так как кислотные свойства у него выражены сильнее, чем у спиртов. Например, в реакции фенола с гидроксидом натрия образуется фенолят натрия и вода.
Кислотные свойства у фенола выражены слабее, чем у неорганических кислот, даже таких, как угольная кислота. Поэтому, если добавить к водному раствору фенолята натрия соляную кислоту, то образуется фенол и хлорид натрия.
Реакции галогенирования у фенола протекают с замещением атомов водорода в бензольном кольце. Так, в реакции фенола с бромной водой образуется белый осадок 2, 4, 6-трибромфенола. Эта реакция используется для качественного обнаружения фенола.
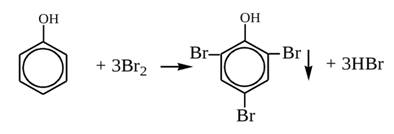
Фенол, как и бензол, реагирует с азотной кислотой. Но у фенола эта реакция идёт легче. В реакции фенола с азотной кислотой образуется 2, 4, 6-тринитрофенол, или пикриновая кислота.
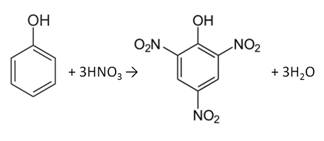
Токсические свойства:
Фенол — токсичное вещество. По степени воздействия на человеческий организм фенол относится к высокоопасным веществам (Класс опасности 2). При вдыхании вызывает нарушение функций нервной системы. Пыль, пары и раствор фенола раздражают слизистые оболочки глаз, дыхательных путей, кожу, вызывая химические ожоги. Доказательства канцерогенности фенола для людей отсутствуют.
Предельно допустимые концентрации (ПДК) фенола:
-
ПДКр.з. = 1 мг/м³ (2 класс опасности) -
ПДКр.с. = 0,3 мг/м³ (2 класс опасности) -
ПДКм.р. = 0,01 мг/м³ -
ПДКс.с. = 0,006 мг/м³ -
ПДКв. = 0,001 мг/л.
Попадая на кожу, фенол очень быстро всасывается даже через неповреждённые участки и уже через несколько минут начинает воздействовать на ткани головного мозга. Сначала возникает кратковременное возбуждение, а потом — паралич дыхательного центра. Даже при воздействии минимальных доз фенола наблюдается чихание, кашель, головная боль, головокружение, бледность, тошнота, упадок сил. Тяжелые случаи отравления характеризуются бессознательным состоянием, синюшностью, затруднением дыхания, нечувствительностью роговицы, скорым, едва ощутимым пульсом, холодным потом, нередко судорогами. Смертельная доза для человека при попадании внутрь — 1—10 г, для детей — 0,05—0,5 г.
ПДК в воздухе рабочей зоны — 1 мг/м³ (максимально-разовая) и 0,3 мг/м³ (среднесменная). Порог восприятия запаха фенола у разных людей разный; и он может достигать (среднее значение в группе) 5,8-7,5 мг/м³[22]. А у отдельных работников он может быть значительно больше среднего значения. По этой причине можно ожидать, что использование широко распространённых фильтрующих СИЗОД в сочетании с «заменой фильтров по появлении запаха под маской» (как это почти всегда рекомендуется в РФ поставщиками) приведёт к чрезмерному воздействию паров фенола на, по крайней мере, часть работников, и причинить вред их здоровью[23] — из-за запоздалой замены противогазных фильтров. Для защиты от фенола следует использовать более эффективные изменение технологии и средства коллективной защиты.
Получение:
В настоящее время производство фенола в промышленном масштабе осуществляется тремя способами:
-
кумольный метод. В каскаде барботажных колонн кумол подвергают некаталитическому окислению воздухом с образованием гидропероксида кумола (ГПК). Полученный ГПК, при катализе серной кислотой, разлагают с образованием фенола и ацетона. Кроме того, ценным побочным продуктом этого процесса является α-метилстирол. 95 % всего производимого в мире фенола производят этим методом. Способ был изобретён советскими учёными П. Г. Сергеевым, Н. М. Горнасталевой, Р. Ю. Удрисом, Б. Д. Кружаловым. По сравнению с большинством других процессов, процесс кумола использует относительно мягкие условия синтеза и относительно недорогое сырьё. Однако, чтобы работать экономно, должен быть спрос как на фенол, так и на ацетон[11][12]. В 2010 году мировой спрос на ацетон составлял примерно 6,7 миллиона тонн, 83 процента из которых были удовлетворены ацетоном, полученным кумольным методом; -
окисление толуола, с промежуточным образованием бензойной кислоты (около 3 %); -
выделением из каменноугольной смолы.
Фенол также можно получить восстановлением хинона.
Применение:
Мировое производство фенола на 2006 год составляет 8,3 млн т/год. По объёму производства фенол занимает 33-е место среди всех выпускаемых химической промышленностью веществ и 17-е место среди органических веществ[источник не указан 1595 дней]. По данным на 2006 год мировое потребление фенола имеет следующую структуру:
-
43 % фенола расходуется на производство бисфенола А, который, в свою очередь, используется для производства поликарбонатов и эпоксидных смол; -
30 % фенола расходуется на производство фенолформальдегидных смол; -
12 % фенола гидрированием превращается в циклогексанол, используемый для получения искусственных волокон — нейлона и капрона[13]; -
в России большое количество фенола используется в нефтепереработке, в частности, для селективной очистки масел на технологических установках типа 37/1 и А-37/1. Фенол проявляет высокую селективность и эффективность при удалении из масел смолистых веществ, различных полициклических ароматических углеводородов с короткими боковыми цепями, а также соединений, содержащих серу[14]; -
остальной фенол расходуется на другие нужды, в том числе на производство антиоксидантов (ионол), неионогенных ПАВ — полиоксиэтилированных алкилфенолов (неонолы), других фенолов (крезолов), лекарственных препаратов (аспирин), антисептиков (ксероформа) и пестицидов. Раствор 1,4 % фенола применяется в медицине (орасепт) как обезболивающее и антисептическое средство[15].

