ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 17.03.2024
Просмотров: 6
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Тексерілді
| Бөлім: | 11.3B 14-топ элементтері |
| Педагогтің аты-жөні: | Г.Сатанова |
| Күні: | 16.02.2023ж |
| Сыныбы: | 11 |
| Қатысушылар саны | |
| Қатыспағандар саны | |
| Сабақтың тақырыбы: | Әр түрлі тотығу дәрежелерін көрсететін 14 (ІV) -топ элементтері оксидтерінің қасиеттері |
| Оқу бағдарламасына сәйкес оқу мақсаты | 11.2.1.2 - 14 (ІV) элементтерінің және олардың қосылыстарының химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастыру; |
| Сабақтың мақсаты: | - 14 (ІV) элементтерінің және олардың қосылыстарының химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастырады. |
Сабақтың барысы:
| Сабақ кезеңі/Уақыты | Педагогтің іс-әрекеті | Оқушының іс-әрекеті | Бағалау | Ресурстар |
| Сабақтың басы Қызығушылықты ояту. 7 мин. |
Оқушылармен амандасу, түгелдеу. Мұғалім іс-әрекетті: Мұғалім оқушыларға өткен тақырыпты еске түсіру үшін тапсырма береді. |
Мақсаты: сабақ тақырыбын енгізу Тапсырма сипаты:алдыңғы білімді тексеру. Сабақ тақырыбын, Сабақтың мақсаты мен тілдік тапсырмалар беріледі. | Мақсаты: Оқушылар бір-біріне тілек білдіреді, тыңдау дағдыларын дамытуға бағытталады, сондай-ақ барлық оқушылардың қатыстырылуы арқылы сабаққа белсенділігі артады. Тиімділігі: Оқушылар бір-біріне тілек айту арқылы жақындасады, көңіл-күйін көтереді және бауырмалдығын оятады. | |
| Жаңа сабаққа кіріспе | | Оқушы іс-әрекетті: оқушылар өткен сабақта қарастырылған 14 топ элементтерінің топ бойынша өзгерістерін еске түсіреді. Ол үшін “Quiz” тапсырмасын орындайды. Кейін жаңа сабақтың тақырыбы мен мақсаттарымен танысады. Кері байланыс: Оқушы-оқушы Жаңа тарау, сабақ тақырыбы, мақсаттары мен жетістік критерийлерімен танысу. | Мақсаты: Жылдам әрі функционалды түрде сыни ойлануды дамыту. Тиімділігі: оқушының танымдық дағдысы артады. Сонымен қатар оқушыға сабақтың өмірмен байланысын көрсетеді және сабақтың тақырыбы мен мақсатын анықтауға мүмкіндік береді. | Қалыптастырушы бағалау: Өз ойын дұрыс мағынада білдіріп, талқылауға белсенділікпен қатысқан оқушыға «Жарайсың!» деген мадақтау сөзімен ынталандыру. |
| Сабақтың ортасы 15 мин. | Мұғалімнің іс-әрекеті: Мұғалім оқушылардың тәжірибені жүргізуді қадағалайды. Кері байланыс: Оқушы-мұғалім, оқушы-оқушы. Жетістік критерийі: 14 топ элементтері мен қосылыстарының реакцияларын түсіну; 14-топтың элементтері мен қосылыстарының реакцияларын түсіндіру. | Тапсырма сипаты: ! Қауіпсіздік техникасы ережелерін тексеру. Оқушыларды 2 топқа бөлінеді және элементтер мен олардың қосылыстарының қасиеттерін зерттеу бойынша эксперименттер жүргізу сұралады. Оқушылар келесі реакцияларды қамтуы тиіс: Қалайы және қорғасын: * сұйылтылған тұз қышқылымен * сұйылтылған күкірт қышқылымен * азот қышқылымен * концентрацияланған қышқылдармен-демонстрация *натрий гидроксидінің концентрацияланған ерітіндісі (демонстрация). Хлорид қалайы ерітіндісі (II) : * натрий гидроксиді * аммиак ерітіндісі * мырыш кесектері * калий дихроматының қышқылданған ерітіндісі (VI) * калий манганатының қышқылданған ерітіндісі (VII). Қорғасын нитратының (II) ерітіндісі: * калий хлориді, бромид және йодид ерітінділері. * сұйылтылған күкірт қышқылымен * натрий гидроксиді ерітіндісі. Қалайы хлориді (II) ерітіндісі бастапқыда концентрацияланған тұз қышқылында дайындалады және бұл процедураны құзыретті тұлға орындауы тиіс. Қалайы хлориді (II) зиянды. Көзді қорғау құралдарын киген жөн. ! Қорғасын тұздары улы және қоршаған ортаға қауіпті. Көзді қорғау құралдарын киіп, қолданғаннан кейін қолды мұқият жуу керек. | Саралау: Бұл жерде саралаудың «Жіктеу» тәсілі көрінеді. Оқушылардың оқуға деген қызығушылығын арттыру мақсатында мүмкіндігінше оларға таңдау еркіндігі беріледі. | http://zadachi-po-ximii.megapetroleum.ru/zadacha-na-parallelnoe-protekanie-reakcij/ |
| Топтық жұмыс 6 мин | Мұғалімнің әрекеттері: Мұғалім есеп шығаруда қолданылатын негізгі формулаларды сұрайды. Неге стехиометрияны білу маңызды? Параллель реакциялар теңдеулерін қолдану арқылы есептерді шешу алгоритмін оқушылармен талқылайды. | Оқушы іс-әрекеті: Оқушылар қауіпсіздік ережесін сақтай отырып қорғасын, қалайы және олардың қосылыстарының химиялық реакцияларын жүргізеді. Дескрипторлар * Эксперимент жүргізу * Химиялық теңдеулерді жазыңыз * Өз тұжырымдарыңызды жазыңыз Тапсырманың сипаттамасы: қосымша парақты құру | Саралау: Бұл жерде саралаудың «Диалог және қолдау көрсету» тәсілі көрінеді. Дұрыс мағынада жауап беруге бағыттау мақсатында кейбір оқушыларға ашық сұрақтар, ал кейбір көмек қажет ететін оқушыларға жетелеуші сұрақтар қойылады. | http://uchebilka.ru/fizika/30572/index.html?page=7 |
| Жеке жұмыс 5 мин | Мұғалімнің әрекеттері: Студенттерге параллель реакциялардың теңдеулері бойынша есептеу үшін дифференциалды тапсырмалары бар жеке карточкалар беріледі. Оқушыларды бағалау үшін, жұмыс аяқталғаннан кейін, бір-бірін бағалауды ұсынылады. | Тапсырманың сипаттамасы: Есептер шығару Оқушы әрекеті: Оқушылар жеке берілген есептерді шығарады. Жетістік критерийі: * есептеу үшін математикалық формулаларды білу * химиялық теңдеулерді жазыңыз * молярлық қатынас бойынша қосылыстардың массасын / көлемін анықтау Бағалау:бірін- бірі бағалау Көлемі 1,68л пропан мен этанның қоспасы жанғанада көлемі 4,48л көміртек (IV)оксиді (көмір қышқыл газы) түзілген. Қоспадағы әр газдың көлемін табыңыздар. Берілгені: V1 =1.68л V(қоспа)= 4.48л Т/К: V2=? Шешуі: 1-тәсіл. Алдымен реакция теңдеулерін жазамыз. Х г У л 2C2H6+ 7O2=4 CO2+ 6H2O (1) (1,68-х) (4,48у) C3H8+ 5O2= 3CO2+ 4H2O (2) Енді (1) және (2) теңдеу бойынша олардың мәндерін есептеп, есептің шартына суйене отырып алгебралық теңдеу құрамыз. y= 2x(1a) (4.48-y)=3(1.68-x) (2а) есептің шарты 2x+3(1.68-x) =4.48 бойынша 2x+5.04-3x=4.48 x= 0.56 Демек бастапқы газдар қоспасы 0,56л этаннан және 1,68-0,56=1,12л пропаннан тұрады. 2- тәсіл.Алдымен реакция нәтижесінже түзілген көміртек (IV) оксидінің зат мөлшерін есептейміз. v(CO2) = 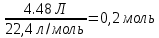 Этан пропанның зат мөлшерін табамыз. v(C2Н6) = 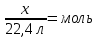 ; v(C3Н8) = ; v(C3Н8) =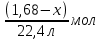 ь ьх/22,4моль у моль 2C2H6+ 7O2=4 CO2+ 6H2O (1) (1,68-х)/22,4 моль (0,2-у) моль C3H8+ 5O2= 3CO2+ 4H2O (2) 1). Реакция бойынша түзілген CO2 – нің зат мөлшері y = 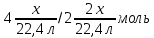 2). Реакция бойынша түзілген CO2 – нің зат мөлшері (0,2 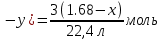 Есептің шарты бойынша: 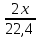 + +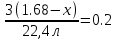 2x+3(1.68-x)=0.2×22.4 2x+5.04-3-x=4.48 х=0.56 Демек, бастапқы газдар қоспасы 0,56л этаннан және 1,68-0,56=1,12л пропаннан тұрады. | | https://drive.google.com/file/d/0BzWC5XH_Ts5BQ2F6WVdieXpBb2c/edit |
| Сабақтың соңы Ой толғаныс. Рефлексия 7 мин. | Мақсаты:Оқушы алған білімін саралай білуге дағдыланады. Тиімділігі:Тақырып бойынша оқушылардың пікірін анықтайды. Жинақталған деректердің құнды болуын қадағалайды. Саралау: Бұл кезеңде саралаудың «Қорытынды» тәсілі көрінеді. | Оқушылар бүгінгі сабақтың мақсаты, тақырыбы бойынша өз ойын айту арқылы сабаққа қорытынды жасайды. | «Дұрыс келісемін», «Толықтырамын, басқа көзқарасым бар», «Менің сұрағым бар». Сонымен қатар 1-10 баллдық жүйе бойынша оқушылардың сабаққа қатысу белсенділігі бойынша бағаланады. | |
