ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 27.03.2024
Просмотров: 7
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
ПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ РОССИИ

МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
«НАЦИОНАЛЬНЫЙ МИНЕРАЛЬНО-СЫРЬЕВОЙ УНИВЕРСИТЕТ «ГОРНЫЙ»
Кафедра физической химии
Лабораторная работа №1
По дисциплине: ХИМИЯ
Тема: Определение эквивалентной массы металла
Автор: студент группы МГП-22 ___________ /Фалилеева А. С./
(подпись) (Ф.И.О.)
Дата: ________________
Проверил: доцент каф. ОФХ ___________ /_____________./
(подпись) (Ф.И.О.)
Санкт-Петербург
2022
Цель работы: усвоить одно из основных химических понятий- понятие об эквиваленте- и научиться определять его количественное значение.
Общие сведения.
Эквивалент вещества - это количество вещества, которое соединяется с 1 молем атомов водорода или замещает то же количество атомов водорода в химических реакциях. Эквивалентная масса( ЭМ) – это масса одного эквивалента вещества, т.е. масса вещества и количество эквивалентов связаны уравнением:
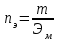 .
.Эквивалентный объём - это объем, занимаемый одним эквивалентом газа при данных условиях.
Закон эквивалентов: вещества взаимодействуют друг с другом в эквивалентных количествах
С


 хема экспериментальной установки.
хема экспериментальной установки.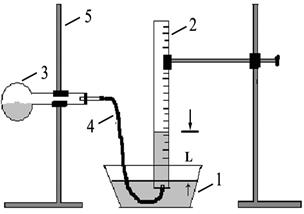
Схема установки:
1 – чашка с водой;
2 – бюретка;
3– колба Вюрца;
4- штатив.
Порядок выполнения работы:
1. Наполнить водой кристаллизатор и бюреткуПроверить, плотно ли закрыт кран бюретки.
2. Закрыв верхнее отверстие пальцем, перевернуть бюретку и опустить её в кристаллизатор с водой. Палец убрать под водой, при этом вода из бюретки не вытечет.
3. Закрепить бюретку в штативе. Уровень воды в ней не должен быть выше крайнего деления шкалы.
4. В колбу Вюрца при помощи мерного цилиндра отобрать 15−20 мл соляной кислоты.
5. Вытереть насухо горло колбы фильтром.
6. Расположив колбу горизонтально, поместить в её горло навеску металла и плотно закрыть колбу пробкой.
7. Поместить присоединенную к боковому отводу колбы Вюрца стеклянную трубку в опущенный в воду конец бюретки.
8. После этого отметить уровень жидкости в бюретке.
9. Затем колбу переводят в вертикальное положение, сбрасывая навеску металла в кислоту. В результате реакции выделяется водород.
10. Когда выделение пузырьков водорода прекратится, отметить конечный уровень воды в бюретке.
11. При помощи полоски миллиметровой бумаги измерить высоту столба воды в бюретке от нижнего края мениска до уровня воды в кристаллизаторе.
12. По показаниям барометра и термометра определить атмосферное давление и температуру в лаборатории
Порядок вычислений.
-
записать атмосферное давление и температуру в лаборатории; -
записать массу навески металла; -
рассчитать давление водорода в бюретке:
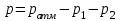 , где
, где 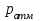 - атмосферное давление в лаборатории, Па;
- атмосферное давление в лаборатории, Па; 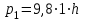 - давление столба воды в бюретке, Па;
- давление столба воды в бюретке, Па; 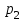 - давление насыщенного водяного пара, Па ( находим его по таблице);
- давление насыщенного водяного пара, Па ( находим его по таблице);-
вычислить массу выделившегося водорода:
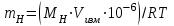 , где:
, где: 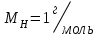 - молярная масса водорода;
- молярная масса водорода; 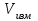 - объем водорода,
- объем водорода,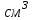 ;
; 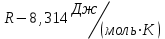 - универсальная газовая постоянная. Найти эквивалент металла по закону эквивалентов:
- универсальная газовая постоянная. Найти эквивалент металла по закону эквивалентов: 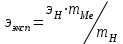 , где
, где 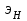 =1- эквивалент водорода. По заданной степени окисления металла определить его молекулярную массу и провести его идентификацию.
=1- эквивалент водорода. По заданной степени окисления металла определить его молекулярную массу и провести его идентификацию. -
Вычислить точное значение эквивалента металла: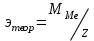 , где z- степень окисления металла,
, где z- степень окисления металла, 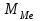 - молярная масса металла(по таблице Д.И. Менделеева);
- молярная масса металла(по таблице Д.И. Менделеева); -
Определить относительную погрешность вычисления: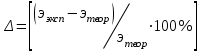 .
.
Обработка результатов эксперимента.
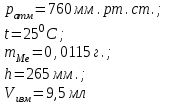
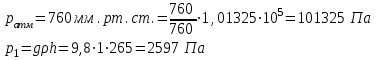
| | mMe | VHCl | V1 | V2 | Vизм. | h | Pатм. | T |
| Ед.Измер. | кг | мг | мг | мг | мг | мм | мм.рт.ст. | ℃ |
| 1 | 0,0094 | 10 | 16,6 | 6,6 | 10 | 144 | 760 | 23 |
Т=296 К;
p2=3172,5 Па;
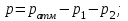
p=95555,5 Па;
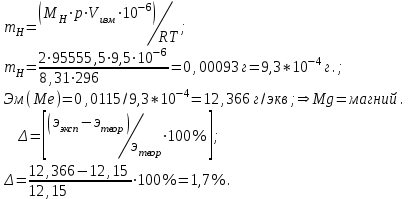
zMg =2, М=24,30 г/моль
Mg+ 2HCl=> MgCl2+H2
Вывод: с помощью данной лабораторной работымы усвоили понятие эквивалента и научились определять его количественное значение.

