Файл: Пермский национальный исследовательский политехнический университет.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 29.04.2024
Просмотров: 23
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
в 350г воды при 293К. Плотность раствора считать равной единице.
217. К 100 мл 0,5М раствора сахарозы С12Н22О11 добавлено 300мл воды. Чему равно осмотическое давление полученного раствора при 250С.
218. При 250С осмотическое давление некоторого водного раствора равно 1,24 кПа. Вычислить осмотическое давление раствора при 00С.
219. При 250С осмотическое давление раствора, содержащего 2,8г высокомолекулярного соединения в 200мл раствора, равно 0,7 кПа. Найти молекулярную массу растворенного вещества.
220. Раствор, в 100мл которого находится 2,3 г вещества, обладает при 298К осмотическим давлением, равным 618,5 кПа. Определить молекулярную массу вещества.
221. Найти при 650С давление пара над раствором, содержащим 13,68г сахарозы С12Н22О11 в 90г воды, если давление насыщенного пара над водой при той же температуре равно 25 кПа.
222. Чему равно давление насыщенного пара над 10% раствором карбамида СО(NH2)2 при 1000С?
223. При 315К давление насыщенного пара над водой равно 8,2 кПа. На сколько понизится давление пара при указанной температуре, если в 540г воды растворить 36г глюкозы С6 Н12 О6?
224. При 293К давление насыщенного пара над водой равно 2,34 кПа. Сколько г глицерина С3Н5(ОН)3 надо растворить в 180г воды, чтобы понизить давление пара на 133,3 Па.
225. При какой приблизительно температуре будет кипеть 50% раствор сахарозы С12Н22 О11?
226. При какой приблизительно температуре будет кристаллизоваться 40% раствор этилового спирта С2 Н5ОН?
227. При растворении 5г вещества в 200г воды получается неэлектролит, кристаллизующийся при -1,450С. Определить молекулярную массу растворенного вещества.
228. При растворении 13г неэлектролита в 400г диэтилового эфира (С2Н5)2О температура кипения повысилась на 0,453К. Определить молекулярную массу растворенного вещества.
229.Температура кипения водного раствора сахарозы равна 101,40С. Вычислить молярную концентрацию и массовую долю сахарозы в растворе.
230. Вычислите массовую долю водного раствора сахара С12Н22О11, зная температуру кристаллизации раствора (–0,930С).
231. Вычислите массовую долю водного раствора глицерина С3Н5(ОН)3, зная, что этот раствор кипит при 100,390С.
232. Вычислите температуру кипения 5%-ного раствора нафталина С10Н8 в бензоле. Температура кипения бензола 80,2
0С.
233. Вычислите массовую долю водного раствора метанола СН3ОН, температура кристаллизации которого –2,790С.
234. В радиатор автомобиля налили 9 л воды и прибавили 2 л метилового спирта (ρ = 0,8 г/мл). При какой наинизшей температуре можно после этого оставлять автомобиль на открытом воздухе, не опасаясь, что вода в радиаторе замерзнет?
235. Водно-спиртовый раствор, содержащий 15% спирта (ρ = 0,97 г/мл), кристаллизуется при –10,260С. Найти молекулярную массу спирта и осмотическое давление раствора при 293 К.
236. Температура кипения водного раствора сахарозы С12Н22О11 равна 101,40С. Вычислить моляльную концентрацию и массовую долю сахарозы в растворе. При какой температуре замерзает этот раствор?
237. Водный раствор метанола имеет концентрацию растворенного вещества 4,85%. При какой температуре будет кристаллизоваться данный раствор?
238. Какой объем метилового спирта (ρ = 0,8 г/мл) нужно добавить к 9 л воды, чтобы полученный раствор не замерзал до –80С?
239. Определить температуру кристаллизации водно-спиртового раствора, плотность которого ρ = 0,97 г/мл, содержащего 15% спирта с относительной молекулярной массой 32.
240. Осмотическое давление раствора, содержащего 3 г сахара в 250мл раствора равно 0,82 атм. при 12 0С. Определить молекулярную массу сахара.
3. Электролитическая диссоциация
Степень диссоциации (ионизации) – α, равна отношению концентрации вещества, распавшейся на ионы (С), к общей концентрации электролита (С0):
α =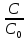 ·100%
·100%
α выражают в % или долях единиц.
Константа диссоциации Кд характеризует диссоциацию слабых электролитов. Значение константы диссоциации зависит от природы электролита, природы растворителя, температуры и не зависит от концентрации раствора. Чем больше константа диссоциации кислоты (основания), тем сильнее кислота (основание).
В общем виде для процесса электролитической диссоциации, выражаемого уравнением:
KmAn ↔ mKn+ + nAm-
константа диссоциации равна:
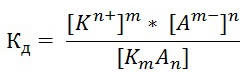
Закон разбавления Оствальда (связь α и Кд)
α =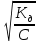
Ионное произведение воды: [H+]·[OH_] = KH20
В чистой воде концентрации ионов водорода и гидроксид-ионов одинаковы и при 25 0С составляют 10-7 моль/л. Отсюда следует, что KH20=10-14.
В нейтральном растворе [H+]=[OH-]=10-7 моль/л.
В кислых растворах [H+]>[OH-],
в щелочных [H+]<[OH-]
Прологарифмировав [H+]·[OH_] = 10-14 , получим:
–lg [H+] – lg [OH-] = 14
pH = –lg [H+] (водородный показатель);
pOH = –lg [OH-] (гидроксильный показатель);
pH + pOH =14
В нейтральных растворах рН = 7, в кислых рН<7, в щелочных рН>7
Задание:
№ 1. Напишите уравнения диссоциации и константы диссоциации для слабых электролитов.
№ 2. По заданным ионным уравнениям напишите соответствующие молекулярные уравнения.
№3. Определите pH раствора заданной концентрации. При расчете pH раствора слабого электролита учитывайте первую стадию диссоциации. Значения констант диссоциации слабых электролитов приведены в справочных таблицах (приложение 5).
Таблица 6.
5. Гидролиз солей
Константа гидролиза и степень гидролиза
Кг =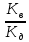 ß =
ß = 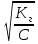 ß =
ß =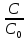
ß – степень гидролиза, (в % или долях ед.)
С – концентрация соли, подвергшейся гидролизу, моль/л;
С0 – концентрация раствора, моль/л
Кг – константа гидролиза;
Кв – константа воды, Кв=10-14
Кд – константа диссоциации слабого электролита, образовавшего данную соль, по последней стадии диссоциации.
Задание:
№ 1. Написать уравнения гидролиза солей А и Б (по ступеням) в молекулярной и ионной формах, указать рН растворов (рН > 7 или рН < 7), тип гидролиза (по катиону, по аниону, по катиону и аниону).
№ 2. Вычислить степень гидролиза и рН раствора соли (Б) заданной концентрации, учитывая первую стадию гидролиза.
Таблица 7.
№ 6. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
1. Окислительно-восстановительные реакции
Правила использования среды
Таблица 8.
Изменение степени окисления окислителей в зависимости от среды
Перманганатометрия
МnО4- + 8Н+ + 5 е- → Мn2+ + 4Н2О
МnО4- + е- → МnО42-
МnО42- + 2Н2О + 2е- → МnО2 + 4ОН-.
Хроматометрия
Cr2O72- + 14H+ +6e- → 2Cr3+ + 7H2O
Йодометрия
I2 + 2S2O32-→ 2I- + S4O62-
Задание:
Расставить коэффициенты электронно-ионным методом в окислительно-восстановительной реакции:
Таблица 9.
217. К 100 мл 0,5М раствора сахарозы С12Н22О11 добавлено 300мл воды. Чему равно осмотическое давление полученного раствора при 250С.
218. При 250С осмотическое давление некоторого водного раствора равно 1,24 кПа. Вычислить осмотическое давление раствора при 00С.
219. При 250С осмотическое давление раствора, содержащего 2,8г высокомолекулярного соединения в 200мл раствора, равно 0,7 кПа. Найти молекулярную массу растворенного вещества.
220. Раствор, в 100мл которого находится 2,3 г вещества, обладает при 298К осмотическим давлением, равным 618,5 кПа. Определить молекулярную массу вещества.
221. Найти при 650С давление пара над раствором, содержащим 13,68г сахарозы С12Н22О11 в 90г воды, если давление насыщенного пара над водой при той же температуре равно 25 кПа.
222. Чему равно давление насыщенного пара над 10% раствором карбамида СО(NH2)2 при 1000С?
223. При 315К давление насыщенного пара над водой равно 8,2 кПа. На сколько понизится давление пара при указанной температуре, если в 540г воды растворить 36г глюкозы С6 Н12 О6?
224. При 293К давление насыщенного пара над водой равно 2,34 кПа. Сколько г глицерина С3Н5(ОН)3 надо растворить в 180г воды, чтобы понизить давление пара на 133,3 Па.
225. При какой приблизительно температуре будет кипеть 50% раствор сахарозы С12Н22 О11?
226. При какой приблизительно температуре будет кристаллизоваться 40% раствор этилового спирта С2 Н5ОН?
227. При растворении 5г вещества в 200г воды получается неэлектролит, кристаллизующийся при -1,450С. Определить молекулярную массу растворенного вещества.
228. При растворении 13г неэлектролита в 400г диэтилового эфира (С2Н5)2О температура кипения повысилась на 0,453К. Определить молекулярную массу растворенного вещества.
229.Температура кипения водного раствора сахарозы равна 101,40С. Вычислить молярную концентрацию и массовую долю сахарозы в растворе.
230. Вычислите массовую долю водного раствора сахара С12Н22О11, зная температуру кристаллизации раствора (–0,930С).
231. Вычислите массовую долю водного раствора глицерина С3Н5(ОН)3, зная, что этот раствор кипит при 100,390С.
232. Вычислите температуру кипения 5%-ного раствора нафталина С10Н8 в бензоле. Температура кипения бензола 80,2
0С.
233. Вычислите массовую долю водного раствора метанола СН3ОН, температура кристаллизации которого –2,790С.
234. В радиатор автомобиля налили 9 л воды и прибавили 2 л метилового спирта (ρ = 0,8 г/мл). При какой наинизшей температуре можно после этого оставлять автомобиль на открытом воздухе, не опасаясь, что вода в радиаторе замерзнет?
235. Водно-спиртовый раствор, содержащий 15% спирта (ρ = 0,97 г/мл), кристаллизуется при –10,260С. Найти молекулярную массу спирта и осмотическое давление раствора при 293 К.
236. Температура кипения водного раствора сахарозы С12Н22О11 равна 101,40С. Вычислить моляльную концентрацию и массовую долю сахарозы в растворе. При какой температуре замерзает этот раствор?
237. Водный раствор метанола имеет концентрацию растворенного вещества 4,85%. При какой температуре будет кристаллизоваться данный раствор?
238. Какой объем метилового спирта (ρ = 0,8 г/мл) нужно добавить к 9 л воды, чтобы полученный раствор не замерзал до –80С?
239. Определить температуру кристаллизации водно-спиртового раствора, плотность которого ρ = 0,97 г/мл, содержащего 15% спирта с относительной молекулярной массой 32.
240. Осмотическое давление раствора, содержащего 3 г сахара в 250мл раствора равно 0,82 атм. при 12 0С. Определить молекулярную массу сахара.
3. Электролитическая диссоциация
Степень диссоциации (ионизации) – α, равна отношению концентрации вещества, распавшейся на ионы (С), к общей концентрации электролита (С0):
α =
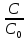 ·100%
·100%α выражают в % или долях единиц.
-
сильные электролиты (α ≈ 1), -
слабые (α < 1) -
неэлектролиты (α ≈ 0).
Константа диссоциации Кд характеризует диссоциацию слабых электролитов. Значение константы диссоциации зависит от природы электролита, природы растворителя, температуры и не зависит от концентрации раствора. Чем больше константа диссоциации кислоты (основания), тем сильнее кислота (основание).
В общем виде для процесса электролитической диссоциации, выражаемого уравнением:
KmAn ↔ mKn+ + nAm-
константа диссоциации равна:
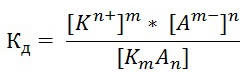
Закон разбавления Оствальда (связь α и Кд)
α =
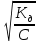
-
Ионное произведение воды. Водородный показатель
Ионное произведение воды: [H+]·[OH_] = KH20
В чистой воде концентрации ионов водорода и гидроксид-ионов одинаковы и при 25 0С составляют 10-7 моль/л. Отсюда следует, что KH20=10-14.
В нейтральном растворе [H+]=[OH-]=10-7 моль/л.
В кислых растворах [H+]>[OH-],
в щелочных [H+]<[OH-]
Прологарифмировав [H+]·[OH_] = 10-14 , получим:
–lg [H+] – lg [OH-] = 14
pH = –lg [H+] (водородный показатель);
pOH = –lg [OH-] (гидроксильный показатель);
pH + pOH =14
В нейтральных растворах рН = 7, в кислых рН<7, в щелочных рН>7
Задание:
№ 1. Напишите уравнения диссоциации и константы диссоциации для слабых электролитов.
№ 2. По заданным ионным уравнениям напишите соответствующие молекулярные уравнения.
№3. Определите pH раствора заданной концентрации. При расчете pH раствора слабого электролита учитывайте первую стадию диссоциации. Значения констант диссоциации слабых электролитов приведены в справочных таблицах (приложение 5).
Таблица 6.
| № задания | № 1 | № 2 | №3 |
| 241 | H2S, CrOHCl2, Mn(OH)2, Li2(HPO4), BaCl2, | Cr3++ OH– + 2Cl– = CrOHCl2 | 0,01М Са(OH)2, |
| 242 | (CoOH)2SO4, HClO2, Cd(OH)2, KHSO3, Ba(NO3)2 | Be2+ + 4OH– = 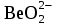 + 2H2O + 2H2O | 0,0002М Al(OH)3, |
| 243 | H3AsO4 FeOHSO4, Zn(NO3)2, Zn(OH)2, LiHSO3, | Ni2+ + OH– + Cl– = NiOHCl | 0,003М Zn(OH)2, |
| 244 | Be(OH)2, H3PO4, CoOHCl, H2SO4, Ba(HSO3)2 | Fe2+ + Cl– + OH– = FeOHCl | 0,001М H2S |
| 245 | А1(ОН)2Cl, H3BO3 NH4OH, Co(HSO4)2,, Cu(NO3)2, | Cd2+ + OH– + Br– = CdOHBr | 0,0003М Bi(OH)3, |
| 246 | Ni(CH3COO)2, LiHS, HAlO2 (ZnOH)2SO4, Ni(OH)2, | Zn2+ + 4OH– = 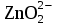 + 2H2O + 2H2O | 0,005М Sn(OH)2 |
| 247 | Fe(NO3)3, CaHPO4, Al(OH)3, AlOHBr2, H2SO4 | H++ 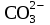 = = 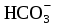 | 0,0015М Be(OH)2 |
| 248 | Sr(OH)2, H3PO4, Ba(HSO4)2, CrOH(NO3)2 CsNO3, | 2H++ 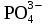 = =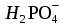 | 0,002М H2SiO3, |
| 249 | ZnОНCl, Al(OH)3, (NH4)2SO4, H2SO3, KHSO4, | NiOHCl + H+ = Ni2+ + H2O + Cl– | 0,0001М Cr(OH)3 |
| 250 | H2Te, FeOHSO4, Co(OH)2, KClO4, KHSO3 | Co2+ + OH– + Cl– = CoOHCl | 0,0005М Al(OH)3 |
| 251 | Cr2(SO4)3, KHCO3, Cr(OH)3, TiOHCl2 Н2CO3, | FeOHCl + H+ = Fe2+ + H2O + Cl– | 0,00025М Fe(OH)3 |
| 252 | MgOHF, Sr(OH)2, LiH2PO4, CH3COOH, Na2SO4 | Cu2+ + OH– + Cl– = CuOHCl | 0,0005М Cr(OH)3, |
| 253 | NaНCO3, NiOHCl, H2SO3, Cr2(SO4)2 Mg(OH)2, | Al3+ + OH– + 2Cl– = AlOHCl2 | 0,03М Са(OH)2 |
| 254 | GaOHCl2, LiHS, H3BO3, Ca(NO3)2 Sn(OH)2 | Cr3+ + OH– + 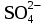 = CrOHSO4 = CrOHSO4 | 0,2М HI |
| 255 | BaОНBr Zn(OH)2, H2SO3, LiHCO3, Co(NO3)2 | Al3+ +OH– + 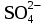 = AlOHSO4 = AlOHSO4 | 0,002М H3BO3 |
| 256 | Cr(OH)3 Fe(OH)SO4, Cu(NO3)2, H2SO4, CaHPO4, | Be2+ + 4OH– = 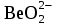 + 2H2O + 2H2O | 0,001М H2Se, |
| 257 | CoОНCl, NaHSO4,, Mg(OH)2, H3BO3, Na2CO3 | Cd2+ + OH– + Br– = CdOHBr | 0,005М H2SeO3 |
| 258 | Cr(OH)3 Pb(NO3)2, Ba(OH)2, NaHCO3, AlOHCl2 | 2H++ 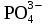 = =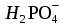 | 0,03М HNO3, |
| 259 | Al(NO3)3, KHSO4, InOH(NO3)2, Ni(OH)2, H2SO3, | Co2+ + OH– + Cl– = CoOHCl | 0,004М Be(OH)2 |
| 260 | NaНS, H2SO4, Ba(OH)2, CaHPO4, (CuOH)2SO4, | Cu2+ + OH– + Cl– = CuOHCl | 0,002М Zn(OH)2 |
| 261 | HMnO4, ZnOHCl, KH2PO4, Sr(OH)2, Cu(NO3)2 | Cd2+ + OH– + I– = CdOHI | 0,1М Cu(OH)2, |
| 262 | NiOHCl, AlCl3, BiOH(NO3)2, Ba(H2PO4)2, Ca(OH)2 | H++ РО43- = НРО42- | 0,5М H2SO4 |
| 263 | (ZnOH)2SO4 Pb(OH)2, LiHS, Ba(NO3), H2SO3 | Al3+ +OH– + 2Cl– = AlOHCl2 | 0,2М Sr(OH)2, |
| 264 | NaНSO4, H2CO3, FeOHCl2, Cu(NO3)2, Ba(OH)2 | H++ 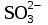 = = 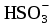 | 0,02М Вa(ОН)2 |
| 265 | NaНCrO4 H3BO3, Pb(NO3)2, Ni(OH)2, MgOHCl | Sn 2+ + OH– + Br– = SnOHBr | 0,35М H2SeO4 |
| 266 | MgОНCl, H2S, Fe(OH)3, Na2HPO4, K2SO4 | Cr2++ OH– + Cl– = CrOHCl | 0,005М Н2СО3, |
| 267 | (ZnOH)2SO4, H2SO4, RbHS, Cu(OH)2, Co(NO3)2 | 2H++ 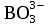 = =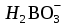 | 0,003М Ni(OH)2, |
| 268 | H3AsO4, H2SO4, KHCO3, Ba(OH)2, CrOH(NO3)2, | Zn2+ + 4OH– = 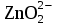 + 2H2O + 2H2O | 0,0025М Fe(OH)3 |
| 269 | Fe(OH)2Cl, H2CO3, NaHSO3, NaHSO4, Ca(OH)2 | AsO33-+3Н+ = H3AsO3 | 0,001М HCN |
| 270 | NaHSO3, Na3PO4, SnOHNO3, Ba(NO3)2, Sr(OH)2 | Cr3++ OH– + 2Cl– = CrOHCl2 | 0,005М Н3PO4 |
5. Гидролиз солей
Константа гидролиза и степень гидролиза
Кг =
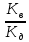 ß =
ß = 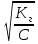 ß =
ß =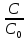
ß – степень гидролиза, (в % или долях ед.)
С – концентрация соли, подвергшейся гидролизу, моль/л;
С0 – концентрация раствора, моль/л
Кг – константа гидролиза;
Кв – константа воды, Кв=10-14
Кд – константа диссоциации слабого электролита, образовавшего данную соль, по последней стадии диссоциации.
Задание:
№ 1. Написать уравнения гидролиза солей А и Б (по ступеням) в молекулярной и ионной формах, указать рН растворов (рН > 7 или рН < 7), тип гидролиза (по катиону, по аниону, по катиону и аниону).
№ 2. Вычислить степень гидролиза и рН раствора соли (Б) заданной концентрации, учитывая первую стадию гидролиза.
Таблица 7.
| № задания | А | Б | С, моль/л |
| 271 | K2S | AlBr3 | 0,01 |
| 272 | CrBr3 | Na2CO3 | 0,1 |
| 273 | SnCl2 | K2SiO3 | 0,001 |
| 274 | Be(NO3)2 | KCN | 0,1 |
| 275 | K2SO3 | Al2(SO4)3 | 0,01 |
| 276 | K2SiO3 | FeCl3 | 1,0 |
| 277 | AlCl3 | K2SO3; | 0,1 |
| 278 | CdBr2 | CaF2 | 0,01 |
| 279 | Ba(NO2)2 | CuSO4 | 0,1 |
| 280 | FeI2 | К2CO3; | 0,001 |
| 281 | Fe2(SO4)3 | Na2SO3 | 0,1 |
| 282 | CuCl2 | K2SO3 | 0,01 |
| 283 | K3PO4 | NiCl2 | 0,01 |
| 284 | FeCl3 | Ba(CH3COO)2 | 0,1 |
| 285 | Na2S | ZnSO4 | 0,01 |
| 286 | K2S | Al2(SO4)3 | 0,1 |
| 287 | K2CO3 | (NH4)2SO4 | 0,001 |
| 288 | CdBr2 | K2CO3 | 0,1 |
| 289 | Be(NO3)2 | K3PO4 | 0,01 |
| 290 | Na2SO3 | CrBr3 | 0,01 |
| 291 | BeCl2 | Na2SO3 | 0,1 |
| 292 | K2S | FeSO4 | 0,01 |
| 293 | Na2S | CrBr3 | 1,0 |
| 294 | Cr(NO3)3 | K2SO3 | 0,001 |
| 295 | Be(NO3)2 | Ba(CH3COO)2 | 0,1 |
| 296 | NaCN | Mn(NO3)2 | 0,01 |
| 297 | CoCl2 | K2CO3 | 0,01 |
| 298 | Cr2(SO4)3 | K2S | 0,1 |
| 299 | Fe(NO3)3 | Na2SiO3 | 0,001 |
| 300 | Cr(NO3)3 | K3PO4 | 1,0 |
№ 6. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
1. Окислительно-восстановительные реакции
Правила использования среды
Таблица 8.
| Процессы | Среда в окислительно-восстановительных реакциях в расчете на «О2-» в соединении | ||
| кислая (Н+) | щелочная (ОН-) | нейтральная (Н2О) | |
| Связать «О2–-» 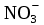 → → 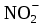 | О2– + 2Н+ = Н2О | О2– + Н2О = 2 ОН– | О2- + Н2О = 2 ОН– |
| Ввести «О2–» 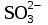 → → 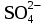 | Н2О = О2– + 2Н+ | 2 ОН– = О2– + Н2О | Н2О = О2– + 2Н+ |
Изменение степени окисления окислителей в зависимости от среды
Перманганатометрия
-
Кислая среда (рН <7):
МnО4- + 8Н+ + 5 е- → Мn2+ + 4Н2О
-
Среда щелочная (рН > 7):
МnО4- + е- → МnО42-
-
Среда нейтральная (рН = 7):
МnО42- + 2Н2О + 2е- → МnО2 + 4ОН-.
Хроматометрия
Cr2O72- + 14H+ +6e- → 2Cr3+ + 7H2O
Йодометрия
I2 + 2S2O32-→ 2I- + S4O62-
Задание:
Расставить коэффициенты электронно-ионным методом в окислительно-восстановительной реакции:
Таблица 9.
| № задания | Окислительно-восстановительные реакции |
| 301 | FeSO4 + KClO3 + H2SO4 → Fe2(SO4)3 + KCl + H2O |
| 302 | MnSO4 + NaBiO3 + HNO3 → Bi(NO3)3 + HMnO4 + Na2SO4 + NaNO3 + H2O |
| 303 | KCrO2 + PbO2 + KOH → K2CrO4 + K2PbO2 + H2O |
| 304 | Cr2(SO4)3 + Br2 + NaOH → Na2CrO4 + NaBr + Na2SO4 + H2O |
| 305 | H2O2 + KMnO4 + KOH → K2MnO4 + O2 + H2O |
| 306 | K2Cr2O7 + Na2SO3 + H2SO4 → Cr2(SO4)3 + Na2SO4 +K2SO4 + H2O |
| 307 | MnSO4 + Br2 + KOH → KMnO4 + KBr + K2SO4 + H2O |
| 308 | KMnO4 + KJ + H2SO4 → MnSO4 + J2 + K2SO4 + H2O |
| 309 | KMnO4 + KJ + KOH → K2MnO4 + KJO4 + H2O |
| 310 | Bi(NO3)3 + NaClO4 + NaOH → NaBiO3 + NaCl + NaNO3 + H2O |
| 311 | NaBiO3 + KCr(SO4)2 + H2SO4 → Bi2(SO4)3 + K2Cr2O7 + Na2SO4 + +H2O |
| 312 | K2Cr2O7 + HJ + HClO4 → KClO4 + Cr(ClO4)3 + J2 + H2O |
| 313 | KMnO4 + MnSO4 + H2O → MnO2 + K2SO4 + H2SO4 |
| 314 | Na[Cr(OH)4] + Cl2 + NaOH → Na2CrO4 + NaCl + H2O |
| 315 | (NH4)2S2O8 + Mn(NO3)2 + H2O → (NH4)2SO4 + HMnO4 + H2SO4 + +HNO3 |
| 316 | KMnO4 + FeCO3 + H2SO4 → Fe2(SO4)3 + CO2 + MnSO4 + K2SO4 + H2O |
| 317 | K2Cr2O7 + K2S + H2SO4 → Cr2(SO4)3 + S + K2SO4 + H2O |
| 318 | KNO3 + KJ + H2SO4 → NO + J2 +K2SO4 + H2O |
| 319 | H2O2 + KJO3 → J2 + KOH + O2 + H2O |
| 320 | AgNO3 + AsH3 + H2O → Ag + H3AsO4 + HNO3 |
| 321 | Na2CrO4+NaJ+H2SO4→Cr2(SO4)3+J2+Na2SO4+H2O |
| 322 | K2Cr2O7+H2S+H2SO4→Cr2(SO4)3+S+K2SO4+H2O |
| 323 | KMnO4+FeCO3+H2SO4→MnSO4+Fe2(SO4)3+CO2+K2SO4+H2O |
| 324 | KMnO4+KNO2+H2O→KNO3+MnO2+KOH |
| 325 | NaCrO2+Br2+NaOH→Na2CrO4+NaBr+H2O |
| 326 | MnSO4+PbO2+HNO3→HMnO4+PbSO4+Pb(NO3)2+H2O |
| 327 | K2MnO4+KJ+H2SO4→MnSO4+J2+K2SO4+H2O |
| 328 | KMnO4+CO+H2SO4→MnSO4+CO2+K2SO4+H2O |
| 329 | FeSO4+HJO3+H2SO4→Fe2(SO4)3+J2+H2O |
| 330 | FeSO4+HNO3+H2SO4→Fe2(SO4)3+NO+H2O |


