Файл: Таырып Газдарды молекулакинетикалы теориясыны негізгі аидалары. Тжірибелік саба 3 (1 саат).docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.02.2024
Просмотров: 10
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Тақырып 1.
Газдардың молекула-кинетикалық теориясының негізгі қағидалары.
Тәжірибелік сабақ №3 (1 сағат)
Мақсаты: Газдардың молекула-кинетикалық теориясының негізгі қағидаларын, негізгі ұғымдарын, формулалары мен заңдарын білу.
Жоспар:
-
Молекулалардың жылдамдығы.
Негізгі формулалар:
1. Зат мөлшері
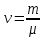 немесе
немесе 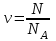
мұндағы
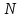 - жүйені құрылымдық элементтерінің (молекулалардың, атомдардың, иондардың және т.б.) саны;
- жүйені құрылымдық элементтерінің (молекулалардың, атомдардың, иондардың және т.б.) саны; 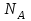 - Авогадро тұрақтысы:
- Авогадро тұрақтысы: 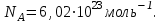
2. Заттың молдік (молярлық) массасы
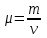
мұндағы
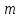 - масса.
- масса.3. Біртекті жүйенің бөлшектерінің (молекулалардың, атомдардың, иондардың және т.б.) концентрациясы
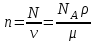
мұндағы
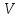 - жүйенің көлемі;
- жүйенің көлемі; 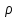 - заттың тығыздығы.
- заттың тығыздығы. 4. Газдардың кинетикалық теориясының негізгі теңдеуі:
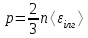
мұндағы
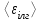 - молекулалардың ілгерілмелі қозғалысының орташа кинетикалық энергиясы.
- молекулалардың ілгерілмелі қозғалысының орташа кинетикалық энергиясы.5. а) Молекулалардың бір екіндік дәрежесіне келетін орташа кинетикалық энергия
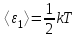
б) Молекулалардың барлық екіндік дәрежесіне сәйкес келетін орташа кинетикалық энергия (молекулалардың толық энергиясы)
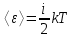
мұндағы
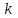 - Больцман тұрақтысы; і - молекулалардың еркіндік дәреже саны;
- Больцман тұрақтысы; і - молекулалардың еркіндік дәреже саны; 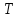 - термодинамикалық температура.
- термодинамикалық температура.в) Молекуланың ілгерілмелі қозғалысының орташа кинетикалық энергиясы
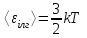
г) Молекулалардың айналмалы қозғалысы орташа кинетикалық энергиясы
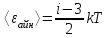
6. Газдың қысымының молекулалардың концентрациясы мен температурасына тәуелділігі
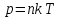
7. Молекулалардың жылдамдығы:
а) орташа квадраттық
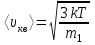 немесе
немесе 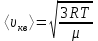
б) орташа арифметикалық
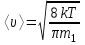 немесе
немесе 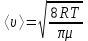
в) ең ықтимал
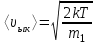 немесе
немесе 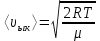
мұндағы
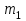 - бір молекуланың массасы.
- бір молекуланың массасы.Есеп шығару үлгілері.
№1 есеп.
Сыйымдылығы 6,9 л ыдыста массасы 23 г азот бар. Қыздырған кезде молекула - лардың бір бөлігі атомдарға диссоциацияланған. Диссоциация коэффициенті (дәрежесі)
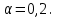 Мыналарды анықтаңдар: 1) қыздырғанға дейінгі азот молекулала -рының
Мыналарды анықтаңдар: 1) қыздырғанға дейінгі азот молекулала -рының 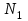 жалпы саны мен
жалпы саны мен 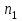 концентрациясын; 2) молекулалардың
концентрациясын; 2) молекулалардың 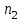 концентрация- сын және азот атомдары - ның қыздырғаннан кейінгі
концентрация- сын және азот атомдары - ның қыздырғаннан кейінгі 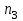 концентрациясын.
концентрациясын.Шешуі:
Анықтамасы бойынша газ бөлшектерінің концентрациясы дегеніміз бөлшектер санының газ алып тұрған ыдыстың сыйымдылығына қатынасы:
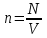 (1)
(1)-
Қыздырғанға дейінгі азот молекулаларының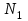 санын мына қатынастан табамыз:
санын мына қатынастан табамыз:
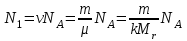 (2)
(2)мұндағы
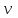 - азоттың зат мөлшері;
- азоттың зат мөлшері;  - Авогадро тұрақтысы;
- Авогадро тұрақтысы; 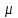 - азоттың молдік массасы;
- азоттың молдік массасы;
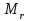 - азоттың салыстырмалы молекулалық массасы;
- азоттың салыстырмалы молекулалық массасы; 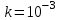 кг/моль.
кг/моль.(2) - ші формулаға шамалардың мәндерін қоямыз:
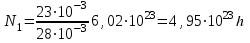
 концентрациясын шамалардың мәндерін (2)-ші формулаға қойып табамыз:
концентрациясын шамалардың мәндерін (2)-ші формулаға қойып табамыз: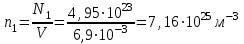
-
Қыздырғаннан кейінгі азот молекулаларының концентрациясын мына қатынастан табамыз:
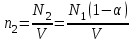 (3)
(3)мұндағы
 - атомдарға ыдырамаған молекулалардың саны.
- атомдарға ыдырамаған молекулалардың саны.(3) - ші формулаға шамалардың мәндерін қоямыз:
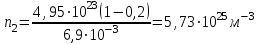
Азотты қыздарғаннан кейінгі атомдардың концентрация
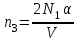 (4)
(4)(4) - ші формуладағы 2 саны әрбір молекула ыдырағаннан кейін екі атомды беретірін білдіреді.
Шамалардың мәндерін (4)-ші формулаға қойып есептейміз:
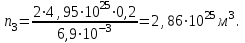
№2 есеп.
Қалыпты жағдайда сыйымдылығы 0,5 л колбада оттегі бар. Колбадағы барлық молекулалардың ілгерілмелі қозғалысының
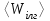 орташа энергиясын анықтаңдар.
орташа энергиясын анықтаңдар.Шешуі:
Барлық молекулалардың ілгерілмелі қозғалысының орташа энергиясы мына формуламен анықталады:
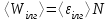 (1)
(1)мұндағы
 - бір молекуланың ілгерілмелі қозғалысының орташа энергиясы;
- бір молекуланың ілгерілмелі қозғалысының орташа энергиясы;  - колбадағы барлық молекулалардың саны.
- колбадағы барлық молекулалардың саны.Бізге белгілі
 (2)
(2)мұндағы
 - Больцман тұрақтысы; Т - термодинамикалық температура.
- Больцман тұрақтысы; Т - термодинамикалық температура.Колбадағы молекулалар санын мына формула бойынша табамыз:
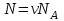 (3)
(3)мұндағы
 - оттегінің зат мөлшері;
- оттегінің зат мөлшері;
 - Авогадро тұрақтысы;
- Авогадро тұрақтысы;Зат мөлшері
 -ді былай табамыз: қалыпты жағдайда
-ді былай табамыз: қалыпты жағдайда 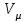 молдік көлем
молдік көлем 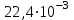 м3/моль - ге тең. Есептің шарты бойынша колбадағы оттегі қалыпты жағдайда болады, демек колбадағы оттегінің зат мөлшеррі мына формуламен табылады:
м3/моль - ге тең. Есептің шарты бойынша колбадағы оттегі қалыпты жағдайда болады, демек колбадағы оттегінің зат мөлшеррі мына формуламен табылады: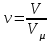 (4)
(4)(4) - ші формуладағы
 -дің өрнектегін (3)-ші формулаға қоямыз:
-дің өрнектегін (3)-ші формулаға қоямыз: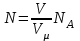 (5)
(5)(2) - ші және (5) - ші өрнектерді ескеріп (1)-ші өрнектегі молекулалардың ілгерілмелі қозғалысының энергиясы былай болады:
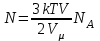 (6)
(6)Берілгне шамалардың мәндерін (6) - ші формулаға қойып есептейміз:
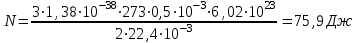
№3 есеп.
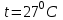 температура кезіндегі аммиктың
температура кезіндегі аммиктың 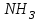 бір молекуласының орташа кинетикалық энергиясын және сол температурада осы молекуланың айналмалы қозғалысының орташа энерггиясын табыңдар.
бір молекуласының орташа кинетикалық энергиясын және сол температурада осы молекуланың айналмалы қозғалысының орташа энерггиясын табыңдар. Шещуі:
Молекуланың орташа толық энергиясы мына формуламен анықталады:
 (1)
(1)мұндағы
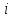 - молекуланың еркіндік дәреже саны; k - Больцман тұрақтысы; Т- газдың термодинамикалық температурасы:
- молекуланың еркіндік дәреже саны; k - Больцман тұрақтысы; Т- газдың термодинамикалық температурасы: 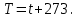
Аммиак молекулалары төрт атомды, содықтан еркіндік дәреже саны
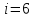 тең.
тең.Шамалардың мәндерін (1) формулаға қоямыз:
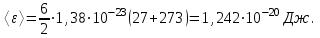 .
.Молекуланың айналмалы қозғалысының орташа энерггиясы мына формуламен анықталады:
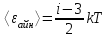 (2)
(2)мұндағы 3 саны молекуланы ілгерілмелі өозғалыстың еркіндік дәреже санын білдіреді.
(1) формулаға шамалардың мәндерін қойып есептейміз:
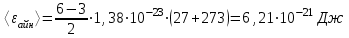
Есептер:




