ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 09.02.2024
Просмотров: 45
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
1.Суть гравиметрического анализа
2. Методы проведения гравиметрического анализа
3. Метод осаждения. Основные этапы и требования.
3.1 Расчет навески анализируемого образца и перевод ее в раствор.
3.2 Перевод определяемого вещества в форму осаждения
3.3 Фильтрование и промывание осадка
3.4 Получение весовой (гравиметрической) формы
Министерство образования и науки Российской Федерации
Федеральное государственное автономное учреждение высшего образования
ФГАОУ ВО «Уральский федеральный университет имени первого Президента России Б. Н. Ельцина» Институт химико-технологический
Факультет химическая технология
Кафедра аналитической химии
РЕФЕРАТ
по дисциплине «АХ и ФХМА»
На тему «Техника выполнения весового анализа. Расчеты в гравиметрии»
Выполнил: Рыбина Е. А.
Группа: Х-210004
Преподаватель: Иванова А. В.
Екатеринбург
2022
Оглавление
Введение 3
1.Суть гравиметрического анализа 4
2. Методы проведения гравиметрического анализа 5
2.1 Метод выделения 5
2.2 Метод отгонки 5
2.3 Метод осаждения 7
3. Метод осаждения. Основные этапы и требования. 8
3.1 Расчет навески анализируемого образца и перевод ее в раствор. 8
3.2 Перевод определяемого вещества в форму осаждения 10
3.3 Фильтрование и промывание осадка 13
3.4 Получение весовой (гравиметрической) формы 15
3.5 Расчет результатов анализа 17
Заключение 19
Список литературы 20
Введение
В аналитической химии методы количественного анализа делятся на титриметрический и гравиметрический анализы. Гравиметрический анализ отличается высокой точностью и отсутствием предварительной градуировке измерительных приборов, но при этом является достаточно трудоемким по сравнению с другими методами.
Гравиметрический анализ обычно делится на три метода: метод отгонки, метод выделения и метод осаждения.
Целью данной работы является рассмотрение основных аспектов в гравиметрическом анализе: основные методы анализа, расчетные формулы и определения.
В связи с данной целью задачами являются: подробное рассмотрение метода осаждения, его основные этапы, формулы и подробная характеристика каждого из этапов.
1.Суть гравиметрического анализа
Гравиметрией называют метод количественного анализа, заключающийся в точном измерении массы определяемого компонента пробы, выделенного в виде соединения известного состава или в форме элемента. Этот метод основан на законе сохранения массы веществ при химических превращениях.
К достоинствам гравиметрического анализа относят высокую точность (обычно погрешность составляет 0,1–0,2%) и простоту. С другой стороны, его проведение зачастую более трудоёмко и занимает больше времени по сравнению с другими методами. При анализе макрокомпонентов точность гравиметрического анализа редко удается превзойти с помощью любых других методов.
В ходе гравиметрического анализа определяемый компонент, как правило, селективно переводят в малорастворимую форму, затем осадок отделяют, высушивают либо прокаливают и точно взвешивают на аналитических весах.
Существуют две формы осадка в гравиметрическом анализе осаждаемая и весовая. Осаждаемая форма — соединение, осаждаемое из раствора и содержащее анализируемый элемент.
Весовая (гравиметрическая) форма — соединение, массу которого непосредственно измеряют взвешиванием.
Пример,
Al(OH)3 Al2O3 + H2O
Где,
Al(OH)3 – осаждаемая форма
Al2O3 – гравиметрическая форма
2. Методы проведения гравиметрического анализа
Различают три группы методов проведения гравиметрического анализа методы выделения, отгонки и методы осаждения.
2.1 Метод выделения
В методах выделения искомый компонент количественно выделяется в свободном состоянии из анализируемого вещества, после чего определяется его масса. Таким способом часто определяют компоненты сплавов.
При растворении определенной навески сплава в царской водке получают раствор, который содержит ионы Au3+ и Cu2+. Добавлением к полученному раствору пероксида водорода, который восстанавливает ионы золота до элементного золотая и не влияет на ионы Cu2+, все золото выделяют в элементном состоянии.
Золото, которое выделилось, отфильтровывают, промывают разбавленным раствором хлоридной кислоты от посторонних примесей, помещают вместе с фильтром в предварительно взвешенный фарфоровый тигель, высушивают, прожаривают для удаления летучих примесей и после охлаждения взвешивают. По массе золота, которое выделилось, рассчитывают его содержание в анализируемом сплаве.
2.2 Метод отгонки
Методы отгонки. Эти методы основаны на измерении точной массы выделившихся в процессе анализа газообразных продуктов. Определяемую часть отгоняют путем нагревания анализируемого вещества или действием соответствующих реагентов, которое сопровождается выделением летучих продуктов.
Вещества, определяемые методом отгонки:
-
карбонаты и углекислый газ в карбонатных породах; -
кристаллизационная вода в гидратах солей; -
бор в виде летучих эфиров борной кислоты, например, B(OCH3)3; -
2) мышьяк в видеAsCl3; -
германий в видеGeCl4; -
железо в виде FeCl3; -
ртуть в виде Hg и т. д.
Метод отгонки также применяют при определении ванадия, вольфрама, молибдена, олова, сурьмы, иода, фтора, осмия, серы, селена, теллура, кремния и других элементов. Отгонка SiF4– отделение кремниевой кислоты от других примесей (соединений титана, железа, щелочных и щелочноземельных металлов и др.).
Методы отгонки бывают прямые и косвенные.
Прямые методы отгонки – методы отгонки, при котором определяемое вещество отгоняют из смеси и затем определяют массу отогнанного вещества или определяемый летучий компонент поглощают специфическим поглотителем и по увеличению массы поглотителя вычисляют содержание определяемого компонента.
Пример, определение карбонатов и CO2 в карбонатных породах
CaCO3+H+=Ca2++CO2↑+H2O,
CO2+2NaOH=Na2CO3+H2O
(поглотитель в данном случае – натронная известь CaO+NaOH).

(2.2.1)
Процентное содержание карбоната вычисляют по формуле:
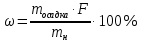
mосадка- весовая форма, г;
F–гравиметрический фактор,
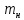 – навеска анализируемого вещества.
– навеска анализируемого вещества.
(2.2.2)
Гравиметрический фактор – это отношение молекулярной массы определяемого вещества к молекулярной массе весовой формы.
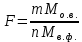
m, n – коэффициенты для того, чтобы уравнять количества атомов или молекул определяемого вещества в числителе и знаменателе.
Вещества-поглотители
: натронная известь CaO+NaOH (поглощаетCO2), хлорид кальцияCaCl2и оксид фосфора (V)P2O5(поглощают воду).
Косвенные методы отгонки – методы, при которых определяется масса остатка. Определяемое вещество отгоняют из точной навески анализируемого образца. После окончания отгонки образец снова взвешивают. Массу определяемого вещества находят по разности масс образца до и после отгона. Пример: определение кристаллизационной воды в кристаллогидрате хлорида бария:
BaCl2
 2H2O=BaCl2+2H2O↑.
2H2O=BaCl2+2H2O↑.Косвенные способы гравиметрических определений применяют при определении влажности материалов, кристаллизационной воды в кристаллогидратах, потери массы при прожаривании и т. п.
2.3 Метод осаждения
Методы осаждения основаны на выделении определяемого компонента в виде малорастворимого соединения из части исследуемого вещества известной массы (навески). Обычно навеску анализируемого образца (mнав), содержащего определяемое вещество (В), переводят в раствор и добавляют избыток реагента-осадителя (А). Образовавшийся осадок (форма осаждения ВbАa) отфильтровывают, промывают, высушивают (прокаливают) до постоянной массы (весовая форма С) и взвешивают на аналитических весах:
bB + aA BbAacC
Зная точную массу и состав весовой формы можно вычислить массу и массовую долю определяемого вещества в анализируемом образце.
Среди вышеперечисленных этот метод является наиболее значимым и универсальным. Его рассмотрим более подробно.
3. Метод осаждения. Основные этапы и требования.
Гравиметрический анализ методом осаждения включает в себя следующие основные этапы:
расчет навески анализируемого образца и перевод её в раствор;
перевод определяемого вещества в форму осаждения (осаждение);
отделение осадка от раствора (фильтрование) и удаление примесей (промывание); перевод формы осаждения в весовую (гравиметрическую) форму;
взвешивание весовой формы на аналитических весах и расчет результатов анализа.
Рассмотрим подробно каждый из этапов.
3.1 Расчет навески анализируемого образца и перевод ее в раствор.
Для того чтобы корректно рассчитать массу навески, необходимо знать формулу анализируемого вещества или хотя бы примерное содержание его в пробе. Чем меньше процентное содержание определяемого компонента в пробе
, тем больше должна быть навеска.
Масса навески зависит от того, кристаллический ли осадок получается в ходе анализа либо аморфный. Кристаллические осадки более плотные, чем аморфные. Масса и объем получаемого осадка должны быть оптимальными для выполнения необходимых операций. Опытным путем установлено, что оптимальная масса осадка (весовой формы) составляет около 0,5 г для кристаллических осадков и 0,1–0,3 г. для аморфных осадков.
Поскольку в гравиметрическом анализе допустимая ошибка взвешивания не должна превышать 0,1%, а лабораторные аналитические весы обеспечивают точность взвешивания до 0,0001 г, минимальная масса навески составляет 0,1 г.
Для расчета массы навески анализируемого образца (пробы) в методе отдельных навесок, когда вся навеска вещества целиком используется для анализа используется формула:
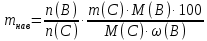


(3.1.2)
(3.1.1)
Если масса навески очень мала и относительная погрешность её взвешивания на аналитических весах превышает 0,1 %, то в этом случае следует применять метод аликвотных частей (пипетирования) и тогда расчет навески проводится по следующей формуле:
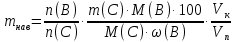
где: Vк – объём мерной колбы, мл;
Vп - объём пипетки (аликвоты), мл.
Для взятия навесок твердых веществ используются часовые стекла, специальные пробирки или бюксы, для жидкостей – капельницы, специальные колбы и др.
Техника взятия навески.
-
1-й способ. Вначале точно взвешивают пустой бюкс. После этого помещают на него необходимое количество анализируемого вещества и снова точно взвешивают бюкс. -
2-й способ. Поместив в бюкс необходимое количество вещества, точно взвешивают его, после чего навеску аккуратно переносят в стакан и снова взвешивают бюкс. Массу навески находят по разности.
Взяв навеску, приступают к ее растворению.
Растворение навески. В качестве растворителей применяют воду, кислоты (или их смеси), щелочи и различные окислители.
Если вещество нерастворимо в воде, прибегают к помощи других растворителей или даже к сплавлению. Органические растворители в весовом анализе не применяют.
3.2 Перевод определяемого вещества в форму осаждения
Соединение, в виде которого производят осаждение определяемого компонента, называется формой осаждения. Форма осаждения должна удовлетворять ряду требований:


