Файл: Контрольная работа по теории горения и взрыва Студентки 3 курса, специальность Пожарная безопасность.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 18.03.2024
Просмотров: 21
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Государственное автономное образовательное учреждение высшего образования
«Астраханский государственный архитектурно-строительный университет»
Кафедра ПБиВ
Заочное форма обучения
КОНТРОЛЬНАЯ РАБОТА
По теории горения и взрыва
Студентки 3 курса, специальность Пожарная безопасность
Факультет ИСиПБ группа зПБ-31-20
Шифр 20050120210 Ф.И.О. Гаврилова Дарья Олеговна
Дата сдачи контрольной работы «3» _декабря_______ 2022г.
Результаты проверки
Контрольной работы______________________________________
(зачтено, не зачтено)
Дата «___»__________20_______г.
Преподаватель___________________________________________
/Подпись, ФИО преподавателя/
Вариант 7
Задача №1
Условие: определить объем и состав продуктов горения образующихся при сгорании 1 кг вещества C₂H₄(OH)₂, если горение происходят при коэффициенте избытка воздуха ɑ = 1,4. Объем продуктов горения считать приведенным к нормальным условиям.
| Дано: C₂H₄(OH)₂ - этиленгликоль; m(C₂H₄(OH)₂) = 1 кг; ɑ = 1,4; н.у. | Решение: C₂H₄(OH)₂+2.5O₂+9.4N₂=2CO₂+3H₂O+9.4N₂
Vºᵦ = 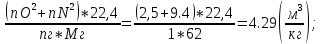
Vᵦ = Vºᵦ*ɑ = 4.29*1.4 = 6.606 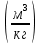 ; ;Δ Vᵦ = Vºᵦ*( ɑ - 1) = 4.29*(1.4 - 1) = 1.716 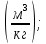
V(CO₂) = 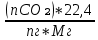 = = 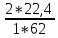 = 0.72 = 0.72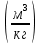 ; ;V(H₂O) = 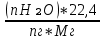 = = 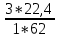 = 1.08 = 1.08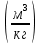 ; ;Vº(N₂) = 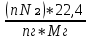 = = 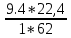 = 3.39 = 3.39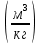 ; ;Vºпг = V(CO₂) + V(H₂O) + Vº(N₂) = 0.72 + 1.08 + 3.39 = 5.19 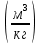 ; ;V(N₂) = Vº(N₂) + 0.79* Δ Vᵦ = 3.39 + 0.79*1.716 = 4.74 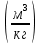 ; ;V(O₂) = 0.21* Δ Vᵦ = 0.21*1.716 = 0.36 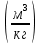 ; ;Vпг = Vºпг + Δ Vᵦ = 5.19 + 1.716 = 6.906 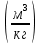 ; ;φ(CO₂) = 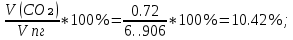 φ (H₂O) = 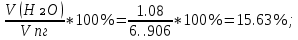 φ (N₂) = 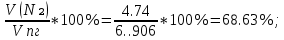 φ (О₂) = 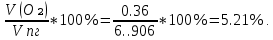 |
| Найти: V(CO₂) - ? V(H₂O) - ? V(N₂) - ? φ(CO₂) -? φ (H₂O) - ? φ(N₂) - ? |
Задача №2
Условие: определить объем и состав продуктов горения смеси газов, если горение происходит при коэффициенте избытка воздуха ɑ = 1.2.
| Дано: ɑ=1,2; φ(CH₄) = 35%; φ(C₅H₁₂) = 8%; φ(C₅H₁₀) = 19%; φ(CO₂) = 17%; φ(O₂) = 21% Найти: V(CO₂) - ? V(H₂O) - ? V(N₂) - ? φ(CO₂) -? φ (H₂O) - ? φ(N₂) - ? | Решение: CH₄+2O₂+7.52N₂=CO₂+2H₂O+7.52N₂ C₅H₁₂+8O₂+30.08N₂=5CO₂+6H₂O+30.08N₂ C₅H₁₀+7.5O₂+28.2N₂=5CO₂+5H₂O+28.2N₂
Vºᵦ = 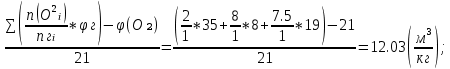
Vᵦ = Vºᵦ*ɑ = 12.03*1.3 = 14.43  ; ;Δ Vᵦ = Vᵦ - Vºᵦ = 14.43 - 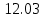 = 2.4 = 2.4
V(CO₂) = 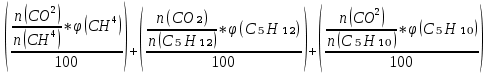 = = 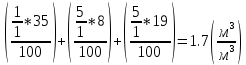 ; ;V(H₂O) = 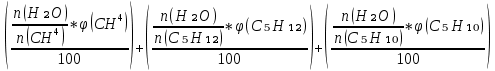 = = 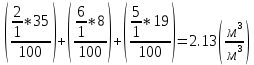 ; ;Vº(N₂) = 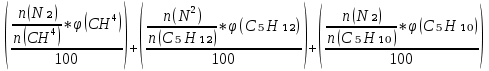 = = 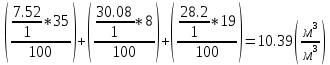 ; ;V(N₂) = Vº(N₂) + 0.79* Δ Vᵦ = 10.39 + 0.79*2.4 = 12.286 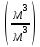 ; ;V(O₂) = 0.21* Δ Vᵦ = 0.21*2.4 = 0.504 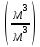 ; ;Vпг = V(CO₂) + V(H₂O) + Vº(N₂) + V(O₂) = 1.7 + 2.13 + 12.286 + 0.504 = 16.62 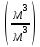 ; ;
φ(CO₂) = 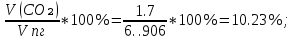 φ (H₂O) = 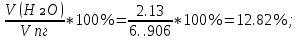 φ (N₂) =  φ (О₂) = 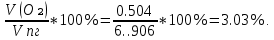 |
Задача №3
Условие: вычислить температуру горения вещества, если горение протекает при коэффициенте избытка воздуха ɑ, а доля потерь тепла излучение составляет ƞ.
| Дано: Керосин ω(C) = 78%; ω(H) = 13.7%; ω(O) = 0.3%; ω(S) = 0%; ω(N)= 0%; ω(W) = 8%; ω(зола) = 0%; ɑ=1,3; ƞ = 0.4 Найти: Тг - ? | Решение:
Qn = 339.4*C + 1257*H – 108.9*(O + N – S) – 25.1*(9*H + W) = 339.4*78 + 1257*13.7 – 108.9*(0.3 + 0 – 0) – 25.1*(9*13.7 + 8) = 40465.8( 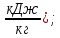
V(CO₂) = 1.86* 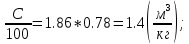 V(H₂O) = 11.2* 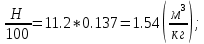 Vº(N₂) = 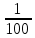 * *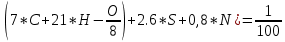 * *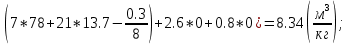
Vºᵦ = 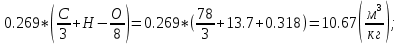
Тг = То + 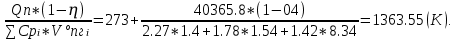 |
Задача №4
Условие: рассчитать адиабатическую температуру горения для стехиометрической смеси вещества А с воздухом (табл.4). Начальная температура горючей смеси Т0 = 273 К.
Для расчета рекомендуется использовать метод последовательных приближений.
| Дано: Глицерин C₃H₅(OH)₃ - глицерин; ΔНхр = -675.4 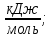 ΔН(CO₂) = -393.5 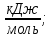 ΔН(H₂O) = -242 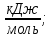 ɑ  = 1. = 1. Найти: Та - ? | Решение: 4C₃H₅(OH)₃+6.5O₂+24.44N₂=7CO₂+6H₂O+24.44N₂
V(CO₂) = 7  V(H₂O) = 6 V(H₂O) = 6 Vº(N₂) = 24.44 Vº(N₂) = 24.44 Δ Vᵦ = 0, т.к. ɑ = 1; Δ Vᵦ = 0, т.к. ɑ = 1;
Qn = (n*∑Hºобр.) – (m*∑ Hºисх.) = (7*(-393.5) + 4*(-242)) – 4*(-675.4) = -1000.9 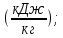
Qср = 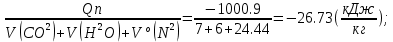
Q1 = H(CO₂)* V(CO₂) + H(H₂O)* V(H₂O) + H(N₂)* Vº(N₂) = 38.2*7 + 29.9*6 + 24.6*24.44 = 1048.024 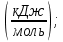 Q1 > Qn, берем Т2 меньше чем Т1, уточним Та, при Т2 = 700: Q2 = H(CO₂)* V(CO₂) + H(H₂O)* V(H₂O) + H(N₂)* Vº(N₂) = 32.8*7 + 25.8*6 + 21.3*24.44 = 904.972 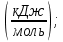 Q2 < Qn. Температура горения Та между 700 - 800ºС;
Та = Т2 + 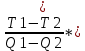 Qn - Qn - 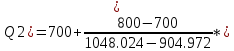 1000.9 - 1000.9 - 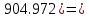 797 (К). 797 (К). |
| |
Задача №5
Условие: определить, какое количество вещества А (табл.5) может выгореть в закрытом помещении объемом Vп, если известно, что горение прекращается при содержании кислорода в помещении, равном
 Для расчета коэффициента избытка воздуха рекомендуется воспользоваться формулой
Для расчета коэффициента избытка воздуха рекомендуется воспользоваться формулой 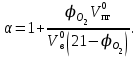
| Дано: C₆H₁₄ - гексан; Vп = 250 м³; φ(O₂) = 15% Найти: V(В) - ? | Решение: C₆H₁₄ +9.5O₂+35.72N₂=6CO₂+7H₂O+35.72N₂ V(CO₂) = 6  V(H₂O) = 7 V(H₂O) = 7 Vº(N₂) = 35.72 Vº(N₂) = 35.72
Vºпг = V(CO₂) + V(H₂O) + Vº(N₂) = 6 + 7 + 35.72 = 48.72 
Vºᵦ = 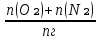 = = 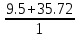 = 45.22 = 45.22  ; ;Δ Vᵦ = Vᵦ - Vºᵦ = 14.43 -  = 2.4 = 2.4
ɑ = 1 + 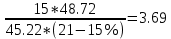
Δ Vᵦ = Vºᵦ *( ɑ - 1) = 45.228(3.69 – 1) = 121.64  V(N₂) = Vº(N₂) + 0.79* Δ Vᵦ = 35.72 + 0.79*121.64 = 131.81  ; ;
V(O₂) = 0.21* Δ Vᵦ = 0.21*121.64 = 25.54  ; ;
Vпг = V(CO₂) + V(H₂O) + Vº(N₂) + V(O₂) = 6 + 7 + 131.81 + 25.54 = 170.35  ; ;7) Определим V(В): V(В) = Vп – (Vпг + Δ Vᵦ) = 250 – (170.35 + 121.64) = 41.99  . . |
Задача №6
Условие: определить, какое количество вещества В (табл. 6) может выгореть в закрытом помещении объемом
Vп, если известно, что горение прекращается при содержании кислорода в помещении, равном
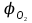 . Для расчета коэффициента избытка воздуха рекомендуется воспользоваться формулой
. Для расчета коэффициента избытка воздуха рекомендуется воспользоваться формулой 
| Дано: Соляровое масло; φ(C) = 86.5%; φ(H) = 12.8%; φ(O) = 0.3%; φ(S) = 0.4%; φ(N) = 0%; φ(W) = 0%; φ(O₂) = 12%; Vп = 650 м³. Найти: V(В) - ? | Решение:
Vºᵦ = 0.269*( 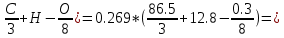 11.18 11.18 
V(CO₂) = 1.86* 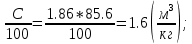 V(H₂O) = 11.2* 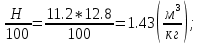 Vº(N₂) = 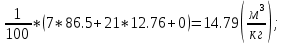
Vºпг = V(CO₂) + V(H₂O) + Vº(N₂) = 1.6 + 1.43 + 14.79 = 17.82 
ɑ = 1 + 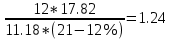
Δ Vᵦ = Vºᵦ *( ɑ - 1) = 11.18*(1.24 – 1) = 2.68  V(N₂) = Vº(N₂) + 0.79* Δ Vᵦ = 14.79 + 0.79*2.68 = 16.907  ; ;V(O₂) = 0.21* Δ Vᵦ = 0.56  ; ;
Vпг = V(CO₂) + V(H₂O) + V(N₂) + V(O₂) = 20.59  ; ;
V(В) = Vп – (Vпг + Δ Vᵦ) = 650 – (20.59 + 11.18) = 618.26  . .
φ(CO₂) =  φ (H₂O) =  φ (N₂) =  φ (О₂) =  |
Задача №7
Условие: определить, какое минимальное количество горючей жидкости (табл.7) (кг) должно испариться в закрытом помещении объемом Vп при нормальных условиях, чтобы создалась взрывоопасная концентрация горючих паров. Условно принять, что пары горючего равномерно распределены в объеме помещения. Нижний концентрационный предел распространения пламени рассчитать по предельной теплоте сгорания.

