ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 19.03.2024
Просмотров: 90
Скачиваний: 3
Органическое вещество играет большую роль в мобилизации биологически инертных форм многих биофильных элементов, переводя их в доступное для растений состояние.
Важную роль играет органическое вещество в продуцировании диоксида углерода, образование которого связано с микробиологическим разложением органических компонентов почвы. Непрерывное поступление диоксида углерода из почвы в приземный слой воздуха оказывает большое влияние на развитие растений и их фотосинтез, в процессе которого они усваивают огромное количество С02. От 40 до 70% всего диоксида углерода, пошедшего на создание урожая, поступает из почвы.
Санитарные функции. Эти функции органического вещества почвы исследованы менее детально, однако некоторые факты установлены достаточно точно. В частности, это относится к фунгистатичности почв. В богатых гумусом почвах преимущественное развитие получает сапрофитная микрофлора, повышающая их фунгистатич- ность — задержку прорастания грибов, обладающих фитопатогенными свойствами. В связи с этим окультуренные, хорошо гумусированные почвы характеризуются отчетливо выраженной фитосанитарной способностью, а при возделывании сельскохозяйственных культур в узкоспециализированных севооборотах они менее подвержены явлению «почвоутомления».
Органическое вещество почвы является важным фактором детоксикации пестицидов. С одной стороны, благодаря их сорбции и переводу в неактивное состояние, с другой — создавая благоприятные условия для развития микрофлоры, оно способствует их микробиологическому разложению. Активное участие принимают различные компоненты органического вещества почвы и в инактивации других загрязняющих веществ, в частности тяжелых металлов и радионуклидов. Не случайно допустимые уровни антропогенных нагрузок при поступлении в почву тяжелых металлов и других токсичных элементов, загрязняющих веществ органической природы (фенолы и др.), пестицидов оказываются значительно выше на хорошо гумусированных почвах, чем на почвах, бедных органическим веществом.
-
Почвенные коллоиды. Строение, состав, свойства.
Коллоиды представляют собой наиболее дисперсную часть твердой фазы почвы, размеры их лежат в пределах 0,001—0,2 мкм.
В коллоидной химии за верхнюю границу диаметра коллоидных частиц принимают величину 0,1 мкм, в почвоведении — 0,2 мкм. В общем, это условные границы и они не имеют принципиального характера. Существенно то, что начиная с этих размеров резко возрастает адсорбционная емкость почвенных частиц благодаря быстрому росту их удельной поверхности.
Коллоиды не только поглощают и удерживают ионы и органические вещества, но и служат цементом для более крупных частиц и агрегатов, влияя таким образом на структуру почвы, от которой зависит ее водно-воздушный режим.Коллоиды образуются в процессе выветривания и почвообразования либо путем раздробления крупных частиц до коллоидных размеров или же за счет соединения молекул и ионов до размеров коллоида. Содержание их в почве различно — от 1—2 до 30—40% к массе почвы. В воде они образуют коллоидные растворы или системы, состоящие из дисперсной фазы (масса коллоидных частиц) и дисперсионной среды (почвенный раствор).
Состав почвенных коллоидов. По вещественному составу коллоиды почвы бывают минеральные, органические и органо-минеральные. В большинстве своем минеральные коллоиды представлены вторичными минералами. Часть из них находится в кристаллическом состоянии. Это прежде всего глинистые минералы: монтмориллонит, каолинит, вермикулит, гидрослюды и др. Кроме них в коллоидной фракции всегда присутствует небольшая примесь тонкодисперсных первичных минералов, главным образом кварца и слюд, не проявляющих коллоидные свойства. Широко представлены в почвах, особенно влажных субтропических и тропических областей, минеральные коллоиды аморфной природы. Это аллофаны, коллоидные формы кремнезема, гидроксиды алюминия, железа и марганца.
Органические коллоиды состоят преимущественно из гумусовых веществ. В коллоидно-дисперсном состоянии могут находиться полисахариды, белки, лигнин и некоторые другие соединения, а также клетки наиболее мелких бактерий, диаметр которых лежит в пределах размеров коллоидных частиц.
Органо-минеральные коллоиды представлены гуматами кальция, продуктами взаимодействия гумусовых веществ с глинистыми минералами, осажденными формами полуторных оксидов и другими соединениями. В почвах присутствуют многочисленные комплексные минеральные и органо-минеральные соединения коллоидной природы, образующиеся при совместном осаждении двух или нескольких веществ. Сюда относятся кремне-алюминиевые и кремне-железистые образования, железисто-марганцевые, органо-железисто-марганце- вые и другие соединения. В большинстве почв преобладают минеральные коллоиды, составляющие 85—90% их общей массы.
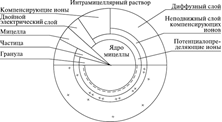
Строение коллоидов. Основу коллоида составляет ядро — внутренняя часть коллоида, представляющее собой аморфное или кристаллическое вещество различного химического состава. На поверхности ядра находится слой ионов, несущих заряд . Ионы, расположенные на поверхности ядра и несущие заряд, называются потенциалопределяющими, а ядро со слоем ионов — гранулой. Появление заряда у различных коллоидов связано с их химическим составом и структурой. У глинистых минералов наличие отрицательного заряда обусловлено свободными валентностями краевых ионов кислорода кристаллической решетки.
Возникновение заряда возможно за счет диссоциации ионов поверхностного слоя в окружающую среду. Это типично для коллоидов органической природы (гуминовые и фульвокислоты), коллоидных форм кремниевой кислоты, гидроксидов железа и алюминия. Так, в кислой среде коллоидный гидроксид железа приобретает положительный заряд вследствие диссоциации в раствор гидроксильного иона. Ион ОН- соединяется с водородом почвенного раствора в молекулу воды, а на поверхности коллоида остается некомпенсированный положительный заряд.
Между гранулой и окружающим раствором на границе раздела фаз возникает термодинамический потенциал, и под действием электростатических сил из раствора притягиваются ионы противоположного знака, образуя компенсирующий слой ионов. Вокруг ядра коллоида образуется двойной электрический слой, состоящий из слоя потенциалопре- деляющих и слоя компенсирующих ионов.
Часть ионов компенсирующего слоя прочно удерживается электростатическими силами и образует неподвижный слой, находящийся в непосредственной близости к межфазной поверхности на молекулярном расстоянии от поверхности ядра. Гранула вместе с неподвижным слоем компенсирующих ионов называется частицей. Другая часть ионов компенсирующего слоя благодаря тепловому движению, стремящемуся равномерно распределить их во всем объеме, удалена от поверхности ядра на расстояние, превышающее молекулярное. Эти ионы образуют диффузный слой, толщина которого в разбавленных растворах колеблется от 0,001 до 0,01 мкм. Концентрация ионов с зарядом, противоположным заряду коллоида, убывает по мере удаления от его поверхности, при этом уменьшается и связь ионов с коллоидом. На определенном расстоянии силы электростатического притяжения уравновешиваются силами теплового движения и концентрация ионов с различными зарядами выравнивается. Это расстояние и определяет толщину диффузного слоя. Между коллоидной частицей и окружающим раствором возникает электрокинетический или дзета-потенциал, под влиянием которого и находятся ионы диффузного слоя. Коллоидная частица вместе с диффузным слоем ионов называется мицеллой. Коллоидная мицелла электронейтральна, однако поскольку основная масса ее принадлежит грануле, заряд последней и рассматривается как заряд коллоида.
-
Свойства почвенных коллоидов.
Важнейшим свойством почвенных коллоидов является способность обменивать ионы, находящиеся в компенсирующем слое, на ионы того же знака, находящиеся в дисперсионной среде. Легко обмениваются ионы диффузного слоя, гораздо труднее — ионы неподвижного слоя. Коллоиды, имеющие в потен- циалопределяющем слое отрицательно заряженные ионы, называются ацидоидами. Они несут отрицательный заряд и способны к поглощению и обмену катионов. К ацидоидам относятся коллоидная кремниевая кислота, гуминовые и фульвокислоты, глинистые минералы.
Коллоиды, имеющие в потенциал определяющем слое положительно заряженные ионы, называются базоидами. Они несут положительный заряд и способны к поглощению и обмену анионов. К ним относятся гидроксиды железа и алюминия, а также белковые соединения.
Некоторые коллоиды способны менять знак заряда: в кислой среде они заряжены положительно, в щелочной — отрицательно. Такие коллоиды называются амфолитоидами или амфотерными коллоидами. Амфотерные коллоиды (гидроксиды алюминия, железа, белки), а также комплексные, состоящие из кристаллических коллоидов, покрытых пленкой аморфных веществ, имеют на поверхности функциональные группы, которые в зависимости от реакции раствора ведут себя то как кислоты, то как основания.При некотором значении pH, которое называется изоэлектрической точкой, коллоид посылает в окружающий раствор одинаковое количество катионов и анионов и становится электронейтральным.
Среди почвенных коллоидов преобладают ацидоиды, играющие важнейшую роль в поглощении почвой катионов. В почвах с сильнокислой реакцией среды, особенно сформированных на аллитной коре выветривания, заметно возрастает роль базоидов. Такие почвы обладают невысокой способностью поглощать катионы, но активно сорбируют анионы, особенно фосфат-ионы.
Наряду с поглощением ионов коллоиды способны притягивать к себе молекулы воды, или гидратироваться, что обусловлено проявлением поляризационных сил. С приближением к заряженной коллоидной частице электронейтральная оболочка воды деформируется. Хотя молекула воды остается в целом нейтральной, она приобретает форму диполя. Попадая в сферу электрического поля заряженной частицы, диполи приобретают строгую ориентировку, обращаясь к ней концами, несущими заряд, противоположный заряду частицы. Вокруг коллоида образуется связанная с ним пленка воды, мощность которой зависит от природы коллоида и величины заряда частицы. По количеству воды, которое удерживается коллоидами, они условно разделяются на гидрофильные и гидрофобные.


