Файл: Сборник задач по технологии и технике нефтедобычи Учеб, пособие для ву.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 20.03.2024
Просмотров: 249
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
СБОРНИК ЗАДАЧ
ПО ТЕХНОЛОГИИ И ТЕХНИКЕ НЕФТЕДОБЫЧИ
Допущено Министерством высшего и среднего специального образования СССР в качестве учебного пособия для студентов вузов, обучающихся по специальности «Технология и комплексная механизация разработки нефтяных и газовых месторождений»
МОСКВА „НЕДРА” 1984


| УДК 622.32 (075.8) Сборник задач по технологии и технике нефтедобычи: Учеб, пособие для ву- зов/И. Т. Мищенко, В. А. Сахаров, В. Г. Грон, Г. И. Богомольный — М.: Недра, 1984.— 272 с., ил. Рассмотрены задачи по определению свойств нефти, газа, воды и их смеси, а также характеристик призабойной зоны скважины по результатам исследования скважин, выбору оборудования и режимов работы скважин при фонтанном и механизированных способах эксплуатации, воздействию на при- забойную зону пласта, подземному ремонту скважин. Впервые предложены задачи по выбору способа эксплуатации скважин с использованием ранго- вого подхода, а также по эксплуатации в осложненных условиях скважин — искривленных, дающих продукцию с большим содержанием воды и нефть с высокой вязкостью. Для студентов вузов, обучающихся по специальности «Технология и ком- плексная механизация разработки нефтяных и газовых месторождений». Табл. 41, ил. 71, список лит.— 32 назв. -л | Инв. |
| Рецензенты: \ | BUiMiiOIViM >1Ш |
кафедра эксплуатации нефтяных и газовых месторождений Грозненского нефтяного института (зав. каф. А.\И. Гужов, д-р техн. наук);
А. А. Джавадян (Министерство нефтяной промышленности)
Игорь Тихонович Мищенко, Виктор Александрович Сахаров,
Владимир Григорьевич Грон, Григорий Исаакович Богомольный
СБОРНИК ЗАДАЧ ПО ТЕХНОЛОГИИ
И ТЕХНИКЕ НЕФТЕДОБЫЧИ
Редактор издательства Н. Е. Игнатьева
Технический редактор Е. С. Сычева
Корректор К- С. Торопцева
И Б № 5805
Сдано в набор 16.05.84. Подписано в печать 02.10.84. Т—20106. Формат 60Х90‘/1Й'
Бумага книжно-журнальная. Гарнитура «Литературная». Печать высокая-
Уел.-п. л. 17,0. Уел. кр.-отт. 17,0. Уч.-изд.л. 17.36 Тираж 3250 экз. Зак. 1131/110—6’
Цена 90 коп.
Ордена «Знак Почета» издательство «Недра». 103633, Москва, К-12, Третьяковский проезд, 1/19
Ленинградская типография № 4 ордена Трудового Красного Знамени Ленинградского объединения «Техническая книга» им. Евгении Соколовой Союзполиграфпрома при Государственном комитете СССР по делам издательств, полиграфии и книжной торговли. 191126, Ленинград, Социалистическая, 14
2504030300—501
043(01)—84
238—85
© Издательство «Недра», 1984
-
ОПРЕДЕЛЕНИЕ ФИЗИЧЕСКИХ СВОЙСТВ ГАЗА, НЕФТИ И ВОДЫ, А ТАКЖЕ МНОГОФАЗНЫХ СИСТЕМ (НЕФТЬ—ВОДА—ГАЗ) ПРИ РАЗЛИЧНЫХ ТЕРМОДИНАМИЧЕСКИХ УСЛОВИЯХ
ОСНОВНЫЕ ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ СОСТОЯНИЯ ВЕЩЕСТВА
Физическое состояние вещества определяется тремя параметрами: давлением, температурой и удельным объемом [8].
Давление — это сила, действующая по нормали на единицу поверхности.
Единица давления в СИ: [р] — Н/м2 = паскаль (Па).
Абсолютное давление р — давление, отсчитываемое от абсолютного нуля. Если оно больше барометрического (атмосферного)
р0, т. е. р>Ро,
Р — Рв Риг (1*1)
где ря — избыточное давление; если р<р0,
Р — Рв — Рв> (1-2
где рв — показания вакуумметра, измеряющего разрежение. В расчетах всегда следует пользоваться абсолютным давлением. Однако в технике измеряют избыточное давление, так как измерительные приборы, если они не изолированы от атмосферы, показывают только это давление.
Температура характеризует тепловое состояние вещества, т. е. энергию, с которой движутся его молекулы.
Единица температуры в СИ: [Г]— кельвин (К).
Она измеряется как по термодинамической шкале Кельвина, так и по международной стоградусной шкале в градусах Цельсия (°С). Если Т - температура, измеряемая по шкале Кельвина (К), или абсолютная температура, t — температура, измеряемая в градусах Цельсия (°С), 70 = 273,15 К — нулевая точка по шкале Цельсия (точка затвердевания воды), то
T = t + T0 = t + 273,15. (1.3)
Удельный объем — объем единицы массы вещества
v = Vim = 1/р, (1.4)
где V, т, р — объем, масса, плотность вещества соответственно.
В нефтегазодобывающей практике различают:
нормальный объем — объем при нормальных условиях: давлении р = р0 = 0,101325 МПа и температуре Т = Т0 = 273,15 К =
= 0 °С;
3
стандартный объем — объем при стандартных условиях: дав-
лении р
= рст = 0,101325 МПа и температуре Т = Гст =
= 293,15 К = 20 °С*.
РАСЧЕТ ФИЗИЧЕСКИХ СВОЙСТВ ПРИРОДНОГО
И НЕФТЯНОГО ГАЗОВ
Состав газа и его использование для нахождения
физических характеристик
Результатом исследования пластовых проб газа и нефти яв-
ляется в первую очередь их компонентный количественный состав,
зная который можно рассчитать практически все физико-химиче-
ские свойства нефти и газа, используемые в расчетах.
Количество вещества п характеризует число структурных эле-
ментов, содержащихся в данной системе (атомы, молекулы и дру-
гие частицы).
Единица количества вещества в СИ: [п ] = моль.
-
моль — такое количество вещества, в котором содержится
столько же структурных элементов, сколько атомов в 12 г изотопа
углерода-12.
Согласно закону Авогадро, 1 кмоль любого газа занимает при
нормальных условиях объем 22,4 м3, называемый нормальным
молярным объемом. Соответственно стандартный молярный объем
равен 24,05 м3.
Компонентный состав нефтяного газа мо-
жет быть выражен в молярных, массовых долях или в процентах.
Молярная доля компонента в смеси газов при нормальных усло-
виях практически совпадает с объемной этого компонента.
Объемный молярный состав газа можно пересчитать в массовый [201
где G; — массовая доля (доли единицы или проценты) компонента в смеси; //, — объемная (молярная) доля компонента в смеси; М, — молекулярная масса г'-го компонента; k — число компонентов.
При этом, если объемный (молярный) состав задан в процентах, то его принимают за 100 моль. Тогда доля каждого компонента в процентах будет выражать число его молей. И наоборот, если состав задан в массовых долях или процентах, его пересчитывают в объемные (молярные) доли или проценты по уравнению
где Ni = Gi/Mi — число молей i-ro компонента в смеси.
Если массовый состав смеси выражен в процентах, то его принимают за 100 кг и для определения числа молей каждого компо
* В ряде зарубежных стран стандартной температурой является 15,6 °С.
Gi = у iMi (ytMi),

(1.5)

(1.6)
4
нента необходимо массу (численно равную процентному содержанию в смеси) разделить на его молекулярную массу. Часто при расчетах необходимо знать средние молекулярную массу и плотность и относительную плотность (по воздуху) попутного газа.
Средняя молекулярная масса газа по данным его объемного (молярного) состава.
k
Л*Г= £ (yiMi)l№, (1.7)
t=i
если объемная доля у с задана в процентах,
_ k
Л*г= £ (шМд,
i = 1
если объемная доля yL задана в долях единицы. Средняя молекулярная масса газа по данным его массового состава
Л?г=100 / £ (Gc/Mi), (1.8)
/ i = i
если массовая доля <3( задана в процентах,
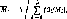
если массовая доля G,- задана в долях единицы.
Средняя плотность газа по вычисленной средней молекулярной массе при нормальных условиях
Pro = Мг/22,414; (1.9)
при стандартных условиях
ргст = Мг/24,05. (1.10)
Относительная плотность газа по воздуху
Рг = рго/1,293 = ргст/1.205 = ЛГ г/28,98, (1.11)
где 1,293 — плотность воздуха при нормальных условиях, кг/м®; 1,205 — то же, при стандартных условиях, кг/м®.
В табл. 1.1 [10] приведены некоторые физические параметры компонентов природных газов, часто используемые при технических расчетах.
Задача 1.1. Пересчитать объемный состав нефтяного газа, выделенного при однократном разгазировании в условиях t


