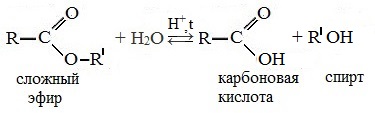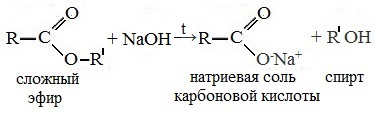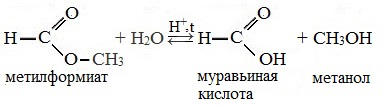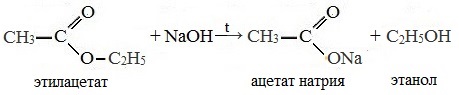Файл: Урок Тема Сложные эфиры. Гидролиз сложных эфиров водой и раствором щелочи. Сложные эфиры в природе. Цель.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 28.03.2024
Просмотров: 8
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
| Дата: | УРОК № | |
| Тема | Сложные эфиры. Гидролиз сложных эфиров водой и раствором щелочи. Сложные эфиры в природе. | |
| Цель | Рассмотреть класс сложных эфиров. Образование названий сложных эфиров. Изомерию, физические и химические свойства. Дать представление об областях применения сложных эфиров. Развивать устойчивый интерес к предмету, логическое мышление. Воспитывать этическое поведение на уроке. | |
| Оборудование | | |
| Тип урока | Изучения нового материала | |
| Методы | Лекция, объяснение | |
| Ход урока: | ||
| I Организационный этап. | Приветствие, перекличка, сообщение темы урока | |
| II Актуализация опорных знаний | ||
| Что такое спирты? Что такое карбоновые кислоты? Как называется реакция между спиртом и карбоновой кислотой? | ||
| III Изучение нового материала | ||
Сложные эфиры
CnH2nO2
Производные карбоновых или неорганических кислот, в которых атом водорода в гидроксильной группе замещён радикалом, называются сложными эфирами. Обычно общую формулу сложных эфиров обозначают как два углеводородных радикала, присоединённых к карбоксильной группе – CnH2n+1-COO-CnH2n+1 или R-COOR’
ироко используют четыре типа названий сложных эфиров: из четырех слов, из двух слов, из одного слова и по номенклатуре ИЮПАК
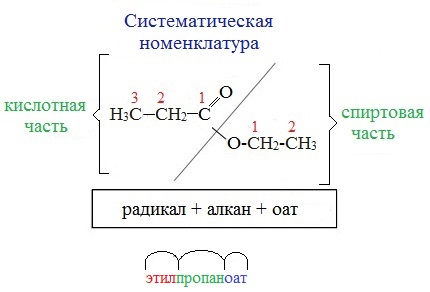
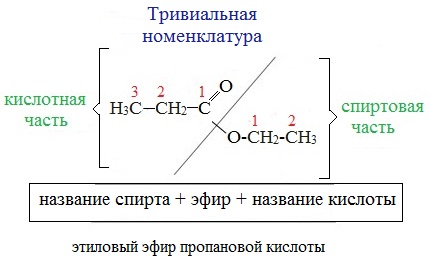
| По систематической номенклатуре (номенклатуре ИЮПАК) | По тривиальной номенклатуре (из 4-х слов) |
| сложные эфиры называют, прибавляя в качестве приставки название спиртового радикала к названию кислоты, в котором вместо окончания –овая кислота используют суффикс –оaт | названия сложных эфиров производят от названий кислот и спиртов, остатки которых входят в их состав, с добавлением слова эфир |
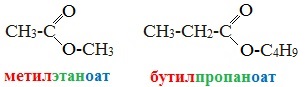 |  |
 |  |
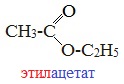
| Из одного слова | Из двух слов |
| Также названия сложных эфиров образуются путем прибавления к названию аниона кислоты приставки с названием углеводородного радикала спирта | Название можно так же составить, складывая названия кислотной и спиртовой частей, к которым добавляется окончание «ый» и слово «эфир» |
  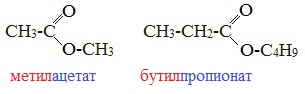 | 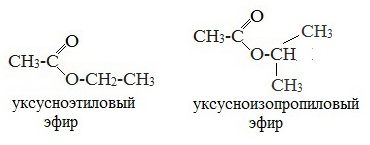 |
Изомерия сложных эфиров | ||
| Изомерия углеродной цепи | Изомерия положения сложноэфирной группировки –СО–О– | Межклассовая изомерия |
| начинается по кислотному остатку с бутановой кислоты, по спиртовому остатку – с пропилового спирта, например, метилбутирату изомерны метилизобутират, пропилацетат и изопропилацетат. | Этот вид изомерии начинается со сложных эфиров, в молекулах которых содержится не менее 4 атомов углерода, например этилацетат и метилпропионат, этилпропионат и метилбутират. | метилацетату изомерна пропановая кислота, а метилформиату уксусная кислота |
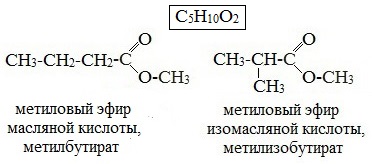 | 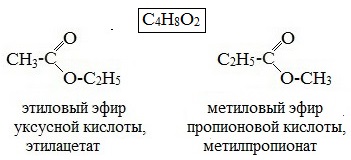 | 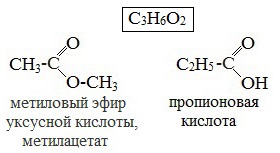 |
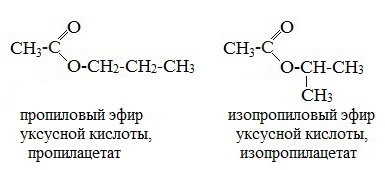 | 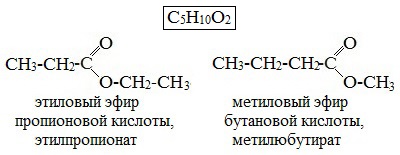 | 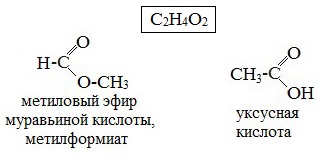 |
| Для сложных эфиров, содержащих непредельную кислоту или непредельный спирт, возможны еще два вида изомерии: изомерия положения кратной связи и цис- , транс-изомерия | ||
| Физические свойства. |
| Когда число атомов С в исходных карбоновой кислоте и спирте не превышает 6–8, соответствующие сложные эфиры представляют собой бесцветные маслянистые жидкости, чаще всего с фруктовым запахом. Они составляют группу фруктовых эфиров. |
| Если в образовании сложного эфира участвует ароматический спирт (содержащий ароматическое ядро), то такие соединения обладают, как правило, не фруктовым, а цветочным запахом. |
| Все соединения этой группы практически нерастворимы в воде, но легко растворимы в большинстве органических растворителей. |
| При увеличении размеров органических групп, входящих в состав сложных эфиров, до С15— С30 соединения приобретают консистенцию пластичных, легко размягчающихся веществ. Эту группу называют восками, они, как правило, не обладают запахом. |
| Воски не смачиваются водой, растворимы в бензине, хлороформе, бензоле. |
| Третья группа – жиры. В отличие от предыдущих двух групп на основе одноатомных спиртов ROH, все жиры представляют собой сложные эфиры, образованные из трехатомного спирта глицерина НОСН2–СН(ОН)–СН2ОН. Карбоновые кислоты, входящие в состав жиров, как правило, имеют углеводородную цепь с 9–19 атомами углерода. Животные жиры (коровье масло, баранье, свиное сало) – пластичные легкоплавкие вещества. Растительные жиры (оливковое, хлопковое, подсолнечное масло) – вязкие жидкости. |
| Сложные эфиры низших карбоновых кислот и спиртов представляют собой летучие жидкости, многие из которых обладают приятным цветочным или фруктовым запахом. Они практически нерастворимы в воде и имеют более низкие температуры кипения, чем изомерные им карбоновые кислоты. Это связанно с тем, что в молекулах сложных эфиров отсутствуют межмолекулярные водородные связи. |
| Химические свойства | ||||||||
| Большинство реакций сложных эфиров связано с нуклеофильной атакой по карбонильному атому углерода и замещением алкоксигруппы. 1. Реакция гидролиза (омыления)Сложные эфиры легко гидролизуются (омыляются) на исходный спирт и кислоту водой (обратимо) или щелочами (необратимо, так как образующаяся карбоновая кислота превращается в соль).
2. Реакция горенияГорение сложных эфиров происходит с образованием углекислого газа и воды: | ||||||||
| Получение: | ||||||||
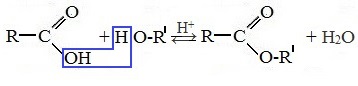 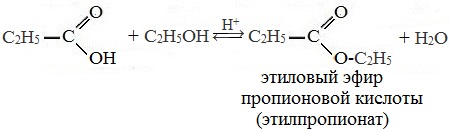 |
Применение
| Этилформиат и этилацетат используются как растворители целлюлозных лаков. |
| Сложные эфиры применяются для производства пластмасс, резины в качестве пластификаторов. Из восков изготавливают политуры, смазки, пропиточные составы для бумаги (вощеная бумага) и кожи, они входят и в состав косметических кремов и лекарственных мазей. |
| В конце XIX — начале ХХ века, когда органический синтез делал свои первые шаги, было синтезировано и испытано фармакологами множество сложных эфиров. Они стали основой таких лекарственных средств, как салол, валидол и др. Как местнораздражающее и обезболивающее средство широко использовался метилсалицилат, в настоящее время практически вытесненный более эффективными средствами. |
| Сложные эфиры на основе низших спиртов и кислот используют в пищевой промышленности при создании фруктовых эссенций, а сложные эфиры на основе ароматических спиртов – в парфюмерной (изготовление мыла, духов, кремов) промышленности. |
| Многие сложные эфиры используются в качестве растворителей, например этилацетат, который используется в качестве растворителя лаков и красок, в органическом синтезе, а также при изготовлении лекарственных средств. |
| Сложные эфиры непредельных спиртов используются для изготовления лаков и красок, так как вступают в реакции присоединения по двойной связи и образуют полимеры. Например, винилацетат - сложный эфир уксусной кислоты и винилового спирта CH3−C(O)−O−CH=CH2 при полимеризации образует поливинилацетат, который используется для изготовления кожезаменителя, его еще называют винилкожей или дермантином. Винилацетат используется для производства поливинилацетатных смол, клеев и красок. |
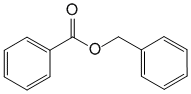 бензилбензоат (бензиловый эфир бензойной кислоты) (бензилбензоат). бензилбензоат (бензиловый эфир бензойной кислоты) (бензилбензоат). Бесцветная маслянистая жидкость со слегка ароматическим запахом, острого и жгучего вкуса. Практически нерастворима в воде, смешивается со спиртом, эфиром и хлороформом. Применение: чесотка (мазь, гель и эмульсия), педикулез (мазь). |
| IV Обобщение и систематизация знаний | |
 | |
| V Домашнее задание | § 30 (Сложные эфиры) изучить, решить задачи 1-2 стр.129 |
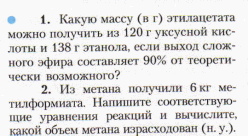 | |
| VI Подведение итогов | Выставление ученикам оценок за работу на уроке. |
| Воски бывают растительные, животные, ископаемые и синтетические. | |
| Растительные воски | Пальмовый воск находится в углублениях кольчатого ствола восковой пальмы, откуда его соскабливают. Одно дерево дает 12 кг воска. |
| Японский воск добывают из лакового дерева, произрастающего в Японии и Китае. | |
| Растительные воски покрывают тонким слоем листья, стебли, плоды и защищают их от размачивания водой, высыхания, вредных микроорганизмов, иногда в качестве резервных липидов входят в состав семян (например, «масло» жожоба). | |
| Животные воски | Пчелиный воск наиболее известный из этого вида восков. Он содержит сложный эфир пальмитиновой кислоты и мирицилового спирта (мирицилпальмитат, пальмитиномирициловый эфир): CH3(CH2)14–CO–O–(CH2)29CH3 |
| Миристилпальмитат, локализованный в углублениях костей черепа кашалота, является проводником звуков при эхолокации. | |
| Шерстяной (шерстный) воск – ланолин – обильно покрывает шерсть животных | |
| Спермацет содержится в костных черепных углублениях некоторых видов китов, особенно кашалотов. На 90% состоит из пальмитиноцетилового эфира. | |
| К воскам относятся кожное сало и ушная сера. | |
| Воск бактерий покрывает поверхность кислотоупорных бактерий, например, туберкулезных, обеспечивая их устойчивость к внешним воздействиям. | |
| Из пчелиного воска пчелы строят соты, шерстяной (ланолин) предохраняет шерсть и кожу животных от влаги, засорения и высыхания. | |
| Ископаемые воски | Торфяной воск получают экстракцией бензином при 800 С верхового битуминозного торфа. |
| Буроугольный воск (монтан-воск) извлекают бензином из бурого битуминозного угля. | |
| Горный воск (озокерит) – минерал из группы нефтяных битумов. | |
| Синтетическим воски | получают на основе нефтяных и смоляных парафинов и их производных. |