ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 28.03.2024
Просмотров: 4
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
1 тарау. Бірлік жүйесі
1963 жылдың 1 қаңтарынан бастап Халықаралық бірліктер жүйесі (SI) енгізілді, онда негізгі бірліктер ретінде:
ұзындық бірлігі – метр (м);
масса бірлігі – килограмм (кг);
температура бірлігі - Кельвин дәрежесі (к);
уақыт бірлігі – секунд (с).
1-кестеде ең көп қолданылатын бірліктер және олардың мөлшері бар.
Кесте 1.
Ең көп таралған шамалардың өлшем бірліктері
| Шамалардың атауы | Әріптік белгілер | Қысқартылған белгілер | Бірліктердің мөлшері |
| Үдеу | a, g | м/с2 | (1 м/с):(1 с) |
| Күш | P | Н | (1 кг):(1 м/с2) |
| Тығыздық | ρ | кг/м3 | (1 кг):(1 м3) |
| Меншікті көлем | v | м3/кг | (1 м3):(1 кг) |
| Қысым | p | Н/м2 | (1 Н):(1 м2) |
| Жұмыс, жылу, энергия | I,L,q, Q | Дж | (1 Н):(1 м) |
| Қуат | N | Вт | (1 Дж):(1 с) |
Практикада физикалық шамалардың бірліктері пайдаланылады: қуат - киловатт (1 кВт = 1000 Вт), жұмыс, жылу, энергия - килоджоуль (1 кДж = 1000 Дж), күш
1 Н (1 Ньютон) Ньютонның екінші заңы бойынша 1 кг денемен 1 м/с2 үдеумен байланысатын күш ретінде анықталады.
Тәжірибеде қолданылатын жүйелік емес бірліктер:
қысым:
1 бар = 100 000 Н/м2 = 750 мм сын. бағ. = 1,02 кгс/см2 = 1,02 атм;
1 атм (физикалық атмосфера) = 760 мм сын. бағ. = 101 325 Н/м2 = 1,0332 кг/см2 = 10 332 кг/м2 = 10 332 мм су бағ.;
1 ат (техникалық
атмосфера) = 735,6 мм сын. бағ. = 98 100 Н/м2 = 1 кг/см2 = 10 000 кг/м2 = 10 000 мм су бағ.;
1 ккал = 4,1868 кДж;
жұмыс:
1 кгс·м = 9,81 Дж.
Жылу есептеулерінде киломоль (кмоль) заттар кеңінен қолданылады, яғни μ кг заттар, мұндағы μ – молекулалық салмақ.
Барлық термодинамикалық теңдеулерде абсолютті қысым қолданылады:


және абсолюттық температура, °K
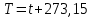
мұндағы
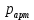 ,
, 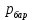 ,
, 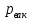 -манометрмен, барометрмен, вакуумметрмен өлшенген қысымдар,
-манометрмен, барометрмен, вакуумметрмен өлшенген қысымдар, 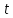 -температура,
-температура,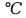 .
.Газ күйінің теңдеуі
Идеал газдың күй теңдеуі келесі теңдеумен ұсынылуы мүмкін:
1 кг газ үшін
 (1)
(1)М кг газ үшін
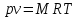 (2)
(2)киломоль газ үшін
 (3)
(3)Мұндағы
 – газ қысымы Н/м2;
– газ қысымы Н/м2; –газ көлемі м3;
–газ көлемі м3;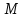 –газ массасы кг;
–газ массасы кг;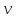 – газдың меншікті көлемі м3 / кг;
– газдың меншікті көлемі м3 / кг;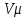 – 1 кмоль газдағы қысым м3/кмоль;
– 1 кмоль газдағы қысым м3/кмоль; – 1 кг газ үшін газ тұрақтысы Дж/(кг·град);
– 1 кг газ үшін газ тұрақтысы Дж/(кг·град);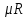 – 1 кмоль газдағы әмбебап газ тұрақтысы Дж/(кмоль·град), 8314,3 Дж/(кмоль·град)тең.
– 1 кмоль газдағы әмбебап газ тұрақтысы Дж/(кмоль·град), 8314,3 Дж/(кмоль·град)тең. Газ тұрақтысының мәндерін теңдеуден есептеуге болады
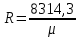
Дж/(кмоль·град) (4)
мұндағы
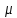 – газдың молекулалық салмағы;
– газдың молекулалық салмағы;Есептеуде тығыздық пен меншікті көлемді анықтау үшін теңдеулер жиі қолданылады:
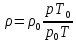
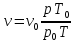
мұндағы "0" индексі бар шама қалыпты физикалық күйдегі газдардың параметрлері болып табылады (қалыпты физикалық деп 760 мм сын.бағ. қысым кезінде газдардың күйі қабылданады және температура 0 °C = 273 °K).
Осы жағдайларда тығыздық пен меншікті көлемді келесі тәуелділіктермен анықтауға болады:
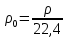 м3/кг, (5)
м3/кг, (5) м3/кг. (6)
м3/кг. (6) Есептер
-
Қазандықтағы абсолютті бу қысымын анықтаңыз, егер манометр ρ = 1,3 барды көрсетсе, ал сынап барометріндегі атмосфералық қысым В= 680 мм болса, температура t = 25 °C.
Шешуі

Барометрдің көрсеткіштері сынап температурасында t = 25 °C. Бұл көрсеткіш 0 °C-қа жетуі керек.
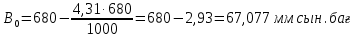
Егер біз басқа теңдеуді қолдансақ, бізде бірдей нәтиже болады:
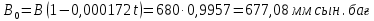
Қазандықтағы абсолютті бу қысымы

-
Сынап барометріндегі ауа қысымы 0 °C температурада 770 мм құрайды. Бұл қысымды бар және Н/м2 арқылы көрсетіңіз.
Шешуі
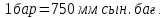
Демек,

-
Белгілі бір жағдайларда метанның 1 м3 массасы 0,7 кг құрайды. Осы жағдайларда метанның тығыздығы мен меншікті көлемін анықтаңыз.
Жауабы:
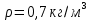 ;
; 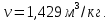
-
Si-дегі Этан С2Н6 газ константасы 277,6 Дж/(кмоль·град) тең. Қалыпты физикалық жағдайда газдың молекулалық салмағын, оның тығыздығын және меншікті көлемін анықтаңыз.
Жауабы:
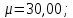
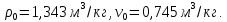
-
Пневматикалық жұмыс үшін ауасы бар сыйымдылығы 12 м3 резервуарда қысым 22 ° C ауа температурасы кезінде манометрмен 8 атм құрайды. Ауаның бір бөлігін жұмысқа пайдаланғаннан кейін оның қысымы 4 атм, ал температура 17 ° C дейін төмендеді. Барометрлік қысым болса, қанша ауа жұмсалғанын анықтаңыз.
болса, қанша ауа жұмсалғанын анықтаңыз.
Жауабы:
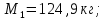
 жұмсалған ауа 54,3 кг.
жұмсалған ауа 54,3 кг.-
Манометр бойынша 118 атм қысымда және -8 °С температурада оттегі бар баллон температурасы +28 °С бөлмеге ауыстырылды.
Газды осы температураға дейін қыздырса, цилиндрде қандай қысым болады?
Атмосфералық қысым 1 кгс/см2.
Жауабы: манометр бойынша 143 ат.
-
Жарылысты болдырмау үшін баллондағы газдың рұқсат етілген қысымы манометр бойынша 150 кгс / см2 құрайды. Бұл цилиндрде 135 кгс/см2 қысымда және 18 °C температурада газ бар.Газды қандай температураға дейін қыздыруға болады?
Жауабы: 50 °C дейін.
-
Егер ауаның температурасы 22 °С болса, абсолютті қысым 1,15 бар болған кезде 8000 кг/сағ ауаны беру үшін құбырдың диаметрін анықтаңыз.
Жауабы: 510 мм.
-
Газдың температурасын анықтаңыз, егер абсолютті қысым 5 кгс/см2 1 моль көлемі 15 м3-ге тең болса.
Жауабы: 611 °C.
-
Ыдыстағы сұйықтық деңгейін өлшеу үшін схемада көрсетілген құрылғы қолданылады. сур-1
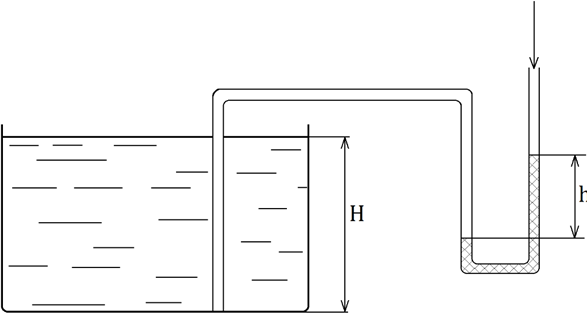
Сур-1. 10 есепті шешу схемасы
Егер h = 220 мм сын.бағ және бензиннің тығыздығы ρ = 840 кг/м3.болса, резервуардағы бензин деңгейін анықтаңыз.
Жауабы: 3,56 м.
2 тарау. Газ қоспалары
Идеал газдардың газ қоспасының қысымы компоненттердің парциалды қысымының қосындысына тең, ал оның массалық құрамы әр компоненттің массалық үлесімен анықталады. Кез келген i -ші газ үшін массалық үлес
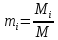 (7)
(7)Мұндағы
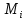 i -ші газ массасы
i -ші газ массасы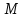 - барлық қоспаның жалпы массасы
- барлық қоспаның жалпы массасы 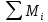
Әрқашан
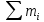 .
.Егер қоспадағы газдар қоспаның қысымына әкелсе, яғни қоспадағы әрбір газ тұрақты температурада (изотермиялық) қоспаның қысымына дейін қысылған болса, онда i -ші компоненттің жаңа болжамды көлемі формула бойынша анықталады.
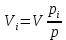
мұндағы i -ші компоненттің ішінара көлемі
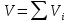
Тәжірибеде және есептеулерде жиі қолданылатын қоспаның көлемдік құрамы компоненттердің көлемдік үлестерімен анықталады, яғни i -ші компонент үшін
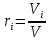
Әрқашан
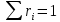 .
.Бірдей қысым мен температурада кез-келген газдың моль көлемі бірдей болғандықтан, моль құрамы көлемді құраммен бірдей болады.
Егер қоспаның көлемі немесе моль құрамы берілсе, онда оның көрінетін молекулалық салмағы формула бойынша анықталады
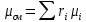
Қоспаның тығыздығы да анықталады:
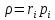
Осыдан кейін қоспаның газ тұрақтысын анықтауға болады, атап айтқанда:
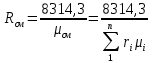
Ішінара қысым теңдеумен анықталады

Егер қоспа массалық құраммен берілсе, онда қоспаның газ тұрақтысы келесідей анықталады:
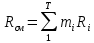
содан кейін теңдеу арқылы көрінетін молекулалық салмақты табуға болады
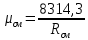
Парциальное давление компонентов определяется по формуле
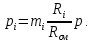
Қажет болған жағдайда газ қоспасын көлемдік құрамнан массалық құрамға және кері қайта есептеу формулалар бойынша жүргізіледі: