ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 11.04.2024
Просмотров: 12
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
| Бағалау критерийлері | |||
| | |||
| Орындалатын жұмыстар | Тапсырманың сипаттамасы | Дескрипторлар | |
| 1.Химиялық диктант | Дәптерлерінде барма? | 1.Сұрақтың барлығы дұрыс | |
| 2. Екеуі дұрыс емес | |||
| 3. Төртеуі дұрыс емес | |||
| 2.Мәтінмен жұмыс. | Мәтінмен танысып, негізгі түйінді мәселені табу, түсінікті жеткізу | 1.Мәтінмен танысып, негізгі түйінді мәселені таба білді, түсінікті жеткізді. | |
| 2.Мәтінмен танысып, негізгі түйінді мәселені таба алмады, толық жеткізі алмады | | ||
| 3.Өзімен – өзі отырды | | ||
| 3. Кубизм әдісі | Тақырып бойынша берілген сұрақтарға дұрыс жауап беру | 1.Барлығына дұрыс жауап берді. | |
| 2.Біреуіне дұрыс жауап бермеді. | | ||
| 3.Мүлдем жауап бере алмады. | | ||
| 4. «Кім жүйрік» | Топпен бірге берілген есептерді дұрыс шешу | 1.Есептер дұрыс шығарылған | |
| 2.Есеп дұрыс шығарылмаған | | ||
| 3.Тапсырма орындалмаған | | ||
| 5.«Білгенге маржан» | Оқушыларға берілген сұрақтарға топпен бірге жауап беру. Дәптерлерінде барма? | 1. Сұрақтарға дұрыс жауап берді | |
| 2.тапсырма дәптерге жазылмаған. | | ||
| 3.Тапсырма орындалмаған. | | ||
Бағалау парағы
| № | Критерийлер | Дискрипторлар | ||
| | | иә | жоқ | кейде |
| 1 | Зейінін толық шоғырландыра алдыма? | | | |
| 2 | Берілген ақпараттарға толық көңіл аудардыма? | | | |
| 3 | Пәнаралық байланысты іске асыра алдыма? | | | |
| 4 | Түсінгенін жақсы ынтамен айта алды ма? | | | |
| 5 | Топ мүшелерімен ақпараттармен бөлісе алды ма? | | | |
| 6 | Оқиғаны өмірмен байланыстыра білді ме? | | | |
| 7 | Оқушының өз мүмкіндігіне, қабілетіне сенімі болды ма? | | | |
| 8 | Талантты және дарынды балалар анықталды ма? | | | |
| 9 | Туындаған сұрақтар негізінде ерекше ынтамен кері байланыс жасай алды ма? | | | |
| 10 | Оқушылардың ынтасынан «Блум таксономиясының» жоғарғы деңгейі көрінді ме? | | | |
8 – 10 ұпай – «5»; 6 – 7 ұпай – «4»; 4 – 5 ұпай – «3»; 1 – 3 ұпай – «2».
Сабақ барысында қойылатын сұрақтар:
Химиялық диктант
-
Р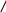 еакцияны аяқта:
еакцияны аяқта:
Cu + Mg(NO3)2 →
-
Теріс зарядты электрод. (Катод) -
Стандартты жағдайдағы электродтың потенциалы не деп аталады? (Стандартты электродтық потенциал) -
Платина тығыздығы нешеге тең? (21,5 г/см3) -
10000С –ден төмен балқитын металдар не деп аталады? (Оңай балқитындар) -
Металдарды жеңіл және ауыр деп қандай қасиетіне байланысты бөледі? (Тығыздығына) -
Периодтық жүйедегі галогендер орналасқан топ. (VII топ, А негізгі топша)
8.Стандартты жағдайдағы температура нешеге тең? (298 К)
Жаңа материалды меңгерту
І топ. s – элементтердің жалпы сипаттамасы
s – элементтер өздерінің валенттік электрондарын оңай береді де, күшті тотықсыздандырғыштық қасиет көрсетеді. Бұл қасиет ІІ топтың элементтеріне қарағанда І топтың элементтерінде айқынырақ байқалады. Атомдардан электрондарды үзіп алу энергиясы сыртқы электрондардың саны артқанда өседі және атом радиусы артқанда кемиді.
Ядродан қашықтаған сайын ядромен валенттілік электрондардың байланысы әлсірейді, сондықтан бұл металдардың химиялық белсенділігі топтарда артады. Бұл элементтердің сипаттамаларын салыстыру көрсеткендей, цезий атомынан сыртқытэлектрон жеңіл үзіледі, сондықтан цезий ең белсенді металл және өте күшті тотықсыздандырғыш.
ІІ топ. сілтілік металдардың физикалық қасиеттері
Сілтілік металдардың физикалық қасиеттері көбінесе кристалдық тор құрылысының ерекшелігіне тәуелді.
Барлық сілтілік металдар күмістей ақ түсті, олар жұмсақ. Бұл металдар жеңіл балқиды. Балқу температурасы литийден цезийге қарай төмендейді, себебі атомдардың шамасының артуынан кристалдық тордағы металл атомдарының байланыс энергиясы кемиді.
Барлық сілтілік металдар жылу мен электр тогын жақсы өткізеді.
ІІІ топ. Сілтілік металдардың химиялық қасиеттері
Химиялық қасиеттері бойынша сілтілік металдар бір – біріне өте жақын. Олар – ең жақсы тотықсыздандырғыштар және басқа металдарға қарағанда белсенділігі өте жоғарылар. Олардың тотықсыздандырғыштық қасиеті литийден цезийге қарай өседі, өйткені кристалдағы химиялық байланыстың беріктігі және атомнан электронды үзіп алып, катиондар түзуге қажетті энергия кемиді.
Сілтілік металдар тікелей барлық бейметалдармен, сумен, қышқылдармен әрекеттеседі.
Кубизм әдісі
-
Сілтілік металдарды атаңдар. (Литий, натрий, калий, рубидий, цезий, франций) -
Натрий және калий қосылыстарын ашқан химиктер. (Ағылшын химигі Г.Дэви және неміс химигі Р.Бунзен) -
№87 элементті ашқан химик. (Француз химигі М.Пере) -
Натрийдің балқу температурасы. (97,70С) -
Жер қыртысында болмайтын радиоактивті элемент. (Франций) -
Элементтердің таралуы бойынша калий нешінші орында? (7)
«Кім жүйрік»
І топ. ІІ топша элементінің 13,05 г күкірт қышқылымен әрекеттескенде (қ.ж.) 3,36 л сутек газын бөліп шығарған. Белгісіз металды тап.
Me + H2SO4 = MeSO4 + H2
13,05 г ―3,36 л
Х ― 22,4 л
Х = 87 Sr
ІІ топ. ІІ топша элементінің 27,4 г күкірт қышқылымен әрекеттескенде (қ.ж.) 4,48 л сутек газын бөліп шығарған. Белгісіз металды тап.
Me + H2SO4 = MeSO4 + H2
27,4 г ―4,48 л
Х ― 22,4 л
Х = 137 Ва
ІІІ топ. ІІ топша элементінің 1,2 г күкірт қышқылымен әрекеттескенде (қ.ж.) 1,12 л сутек газын бөліп шығарған. Белгісіз металды тап.
Me + H2SO4 = MeSO4 + H2
1,2 г ―1,12 л
Х ― 22,4 л
Х = 24 Мg
«Білгенге маржан»
І топ. Мына айналымдарды жүзеге асыр:
Li3N→Li→Li2O→LiOH→Li2SO4
1) 2Li3N → 6Li + N2
2) 4Li + O2 = 2Li2O
3) Li2O + H2O = 2LiOH
4) 2LiOH + H2SO4 = Li2SO4 + 2H2O
ІІ топ. Массасы 4,6 г сілтілік металл йодпен әрекеттескенде массасы 30 г осы металдың йодиді түзіледі. Реакция үшін қандай сілтілік металл алынған?
2Мe + I2 = 2MeI
4,6 г ―30 г
Х ―х * 127
4,6 г*(х * 127) = х * 30 г
4,6 х + 584,2 = 30 х
584,2 = 30 х – 4,6 х
584,2 = 25,4 х
Х = 584,2 / 25,4
Х = 23
Д/ж: Аr(Na) = 23
ІІІ топ. ІІ – А топша элементінің 2 грамы тұз қышқылының құрамынан 1,12 л Н2 бөліп шығарса, ол қай элемент болғаны?
Me + 2HCl = MeCl2 + H2
2 г ―1,12 л
Х ― 22,4 л
Х = 40 Са
Қосымша материалдар:
І топ. №6 есеп.
Ұнтақ түрінде алынған мырыш пен алюминийді күкіртпен аздап қыздырғанда тұтанады. Осы реакцияның теңдеуін жазыңыз. Әрбір металдың 0,5 молімен реакцияға түсетін күкірттің массасын есептеңдер.
Б
 ер: Шешуі:
ер: Шешуі: ʋ( Zn) = 0.5 моль 1) Zn+S→ZnS
ʋ (Al) = 0.5 моль
 т/к: m (S) =? ʋ (Zn) = 0.5 моль
т/к: m (S) =? ʋ (Zn) = 0.5 мольМ (S)= 32 г/моль
0,5моль – х
1моль – 32г/моль
х = 16 г (S)
2) 2Al + 3S→Al2S3
0.5 моль – х
2 моль – 3 моль
х=0,75 моль
m= M*ʋ= 0.75 моль*32 г/моль = 24 г
І
 І топ. №7 есеп. Құрамында 65% мырыш және 35% мыс бар 10 г құйманы артық мөлшерде алынған тұз қышқылына салады. Реакция аяқталғаннан кейін алынған ерітіндіні суалтты. Қандай тұз түзілді? Оның массасы қандай?
І топ. №7 есеп. Құрамында 65% мырыш және 35% мыс бар 10 г құйманы артық мөлшерде алынған тұз қышқылына салады. Реакция аяқталғаннан кейін алынған ерітіндіні суалтты. Қандай тұз түзілді? Оның массасы қандай?Берілгені: Шешуі:
m(Zn)= 10 г Zn + 2HCl = ZnCl2 + H2
ω
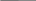 (Zn)=65% 10г хг
(Zn)=65% 10г хгω
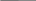 (Cu)=35% 65 136
(Cu)=35% 65 136 т
 /к m(тұз)=? Х =20,92 г ZnCl2
/к m(тұз)=? Х =20,92 г ZnCl2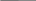 20,92 г ZnCl2 100%
20,92 г ZnCl2 100% Хг 65%
Хг 65%Х=13,6г ZnCl2
ІІІ топ. №8 есеп. Мыс хлоридінің ерітіндісіне массасы 5,6 г темір пластинкасын салды. Темір толық еріді. Бөлінеген мыстың массасы қанша?

Бер: Шешуі:
m( Fe) =5,6г CuCl2 + Fe →FeCl2 + Cu
 М ( Fe) = 56 г/моль М (Сu) = 64 г/моль
М ( Fe) = 56 г/моль М (Сu) = 64 г/мольт/к: m (Cu) = ? 5.6 г – х
56 г/ моль – 64 г/моль
X=6.4г
-
Литий ең ауыр металл. (жоқ) -
Тығыздығы ең көп металл осмий (ия) -
Натрийдің валенттілігі ІІІ тең. (жоқ) -
Ең жеңіл газ сутегі (ия) -
Сынап – сұйық металл. (ия) -
Алюминий қосылыстарында - 3 тотығу дәрежесін көрсетеді. (жоқ) -
Калий сілтілік металл (ия)
Сұрақ қойылады, жауап берген оқушыға жауапқа байланысты мақал - мәтел құрастыруы керек.
1.СаО молекулалық массасы қай элемент атомына сәйкес келеді? /Темір/
Мақал: Темірді қызған кезде соқ.
2. І Б топшада орналасқан с. а. м. 108 болатын элемент? /Күміс/
Мақал: Тағасының күмісіне мақтанба, атыңның жүрісіне мақтан.
3. Н2О / Су/ Мақал: Су ішкен құдығыңа түкірме.
4. ІҮ А топшасындағы рет саны 82 болатын элемент? /Қорғасын/
Мақал: Қойдың сүті қорғасын, қойды ұрған оңбасын.
5. Қанға қызыл түс беретін металл? /Темір/
Мақал: Ағаш кессең ұзын кес қысқартуға оңай, темір кессең қысқа кес, ұзартуға оңай.
6. Сұйық металл? /Сынап/
Мақал: Көз бұлақ, көңіл – сынап.
1.Барлық бейметалдар – р элементтер.(Иә)
2. І –ІІ топтың негізгі топша элементтері s- элементтеріне жатама?(Иә)
3. р- элементтерінің металдық қасиеті жоғары.(Жоқ)
4. d - элементтерінің қосымша топша металдары қиын балқитын металдар.(иә)
5.Хром, молибден немесе вольфрам - өз периодындағы (VІ топ, қосымша топша) ең оңай балқитын элементтер.( жоқ)
Мынадай айналуларды жүзеге асыруға болатын реакция теңдеулерін жазыңдар:
Са → СаО → Са(ОН)2 →СаСl2
-
2Ca + O2 =2CaO -
CaO + H2O = Ca(OH)2 -
Ca(OH)2 + CuCl2 = CaCl2 + Cu(OH)2
Үйге тапсырма:
