Файл: Теория к разделу элементы содержания 8 (Тепловые явления).docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 26.04.2024
Просмотров: 4
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Теория к разделу «ЭЛЕМЕНТЫ СОДЕРЖАНИЯ № 8»
(Тепловые явления)
I
-
Вещество состоит из частиц. -
Частицы беспорядочно (хаотически) и непрерывно движутся. -
Частицы взаимодействуют друг с другом силами притяжения и отталкивания.
Молекула – наименьшая частица вещества, обладающая химическими свойствами данного вещества. (Простые одноатомные молекулы имеют размер порядка 10–10 м.)
Атом – наименьшая частица, обладающая свойствами химических элементов, входящих в состав данного вещества.
Движение молекул доказывают:
| Диффузия | Броуновское движение |
| явление проникновения двух или нескольких соприкасающихся веществ друг в друга (наиболее быстро протекает в газе, наиболее медленно - в тв. телах) | это тепловое движение мельчайших микроскопических частиц, взвешенных в жидкости или газе |
II
Любое вещество при определенных условиях может находиться в различных агрегатных состояниях – твердом, жидком и газообразном.
| | Газы | Жидкости | Твёрдые тела |
| Особенности строения |
|
|
|
| Схема строения | 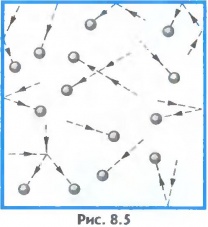 | 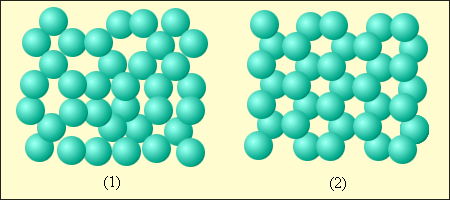 | 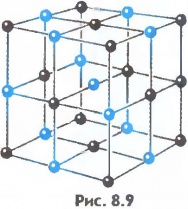 |
| Движение молекул | Беспорядочно по всему объёму с большими скоростями. | Колебания около положения равновесия с перескоками. | Колебания около положений равновесия. |
| Форма | Не сохраняют | Не сохраняют | Сохраняют |
| Объём | Занимают весь предоставленный объём | Сохраняют | Сохраняют |
Идеальный газ — математическая модель газа, в которой предполагается, что:
-
потенциальной энергией взаимодействия частиц газа можно пренебречь по сравнению с их кинетической энергией; -
суммарный объём частиц газа пренебрежимо мал; -
между частицами нет дальнодействующих сил притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги.
III
Тепловые явления – явления, связанные с нагреванием или охлаждением тел.
Тепловое движение - непрерывное хаотическое движение частиц вещества.
Температура t, 0C: (термометр - прибор для измерения температуры)
-
физическая величина, характеризующая состояние теплового равновесия системы тел: все тела системы, находящиеся друг с другом в тепловом равновесии, имеют одну и ту же температуру; -
физическая величина, характеризующая степень нагретости тела.
Абсолютная температура обозначается буквой Т {\displaystyle T}ТТТттттЕ , измеряется в Кельвинах {\displaystyle (K)} К и отсчитывается по абсолютной шкале (Кельвина). Абсолютная термодинамическая шкала является основной шкалой в физике и в уравнениях термодинамики.
Температура тела зависти от скорости движения молекул!
Внутренняя энергия равна сумме кинетических энергий беспорядочного движения Ек и потенциальных энергий взаимодействия друг с другом Еп всех молекул тела:
U= Екм +Епм, Дж
-
зависит от температуры тела, агрегатного состояния и т. д.; -
не зависит ни от движения тела, ни от его положения.
Внутренняя энергия тела может изменяться:
-
при совершении работы (над телом U ↑, само тело U↓); -
без совершения работы - теплопередача - процесс изменения внутренней энергии без совершения работы.
Способы теплопередачи:
| Теплопроводность | Конвекция | Излучение |
| передача U от одного тела к другому или от одной его части к другой в результате теплового движения и взаимодействия частиц | перенос энергии потоками жидкости или газа (происходит перенос вещества) | перенос энергии электромагнитными волнами, может происходить и в вакууме |
IV
Количество теплоты Q [Дж] - энергия, которую тело получает или теряет при теплопередаче.
| Название процесса | Суть процесса | Формула | Смысл величин |
| Нагревание (охлаждение) | Тело получает или отдаёт Q | Q = сm (tк - tн) | С - удельная теплоемкость вещества, Дж/кг0С, Уде́льная теплоёмкость— физическая величина, численно равная количеству теплоты, которое необходимо передать 1 кг данного вещества для того, чтобы его температура изменилась на 1 0С. m – масса тела, кг tк и tн – конечная и начальная температуры, 0С |
| Q = сm (tн - tк) | |||
| Сгорание топлива | Выделяется Q | Q = qm | q – удельная теплота сгорания топлива, Дж/кг Уде́льная теплота́ сгора́ния то́плива — физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг. |
| Плавление (кристаллизация) | Тело получает или отдаёт Q | Q = λm | λ - удельная теплота плавления, Дж/кг Уде́льная теплота́ плавле́ния (кристаллиза́ции) — количество теплоты, которое необходимо сообщить кристаллическому веществу массой 1 кг, чтобы перевести его из твёрдого состояния в жидкое при температуре плавления (то же количество теплоты выделяется при кристаллизации вещества). |
| Парообразование (конденсация) | Тело получает или отдаёт Q | Q = Lm | L - удельная теплота парообразования, Дж/кг Удельная теплота парообразования и конденсации — физическая величина, показывающая, какое количество теплоты необходимо сообщить 1 кг вещества, взятому при температуре кипения, чтобы перевести его из жидкого состояния в газообразное (равна теплоте, выделяемой при конденсации пара, взятого при температуре кипения, в жидкость). |
Фазовый переход - переход из одного агрегатного состояния в другое.
1. Парообразование – процесс перехода вещества из жидкого состояния в газообразное. 2 способа:
| Испарение | Кипение |
| процесс вылета молекул из жидкости. Скорость испарения зависит от: рода жидкости, температуры жидкости, площади поверхности жидкости, скорости ветра. | процесс образования по всему объёму жидкости пузырьков, наполненные паром, которые растут, всплывают на поверхность и лопаются при определённой температуре. |
|
|
2. Конденсация - переход вещества из газообразного состояния в жидкое (процесс возврата молекул пара в жидкость).
3. Плавле́ние — переход тела из кристаллического твёрдого состояния в жидкое.
4. Кристаллизация (отвердевание) — процесс перехода вещества из жидкого (газообразного) состояния в твёрдое кристаллическое с образованием кристаллической решетки.
Вещества отвердевают при той же t , при которой плавятся!
Динамическое равновесие между жидкостью и паром – состояние, при котором число молекул, покидающих жидкость за некоторое время, равно числу молекул, возвращающихся из пара в жидкость за то же время.
Насыщенный пар - пар, находящийся в динамическом равновесии со своей жидкостью.
Влажность воздуха - содержание водяного пара в воздухе. Измеряется психрометром.
Характеризуют рядом величин:
-
Парциальное давление водяного пара - давление, которое производил бы водяной пар, если бы все остальные газы отсутствовали. -
Относительная влажность воздуха - выраженное в процентах отношение парциального давления водяного пара, содержащегося в воздухе при данной температуре, к давлению насыщенного пара при той же температуре.
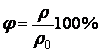
Точка росы - температура, при которой пар данного давления становится насыщенным (и относительная влажность становится равной 100%).


