Файл: Оборудование Весы, штатив, песчанная баня, прибор, состоящий из двухгорлой колбыреактора, воздушного холодильника, приёмника, колпачка, газоотводной трубки, мерная пробирка.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 28.04.2024
Просмотров: 11
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
| Техника выполнения опыта | |
| Оборудование: | Весы, штатив, песчанная баня, прибор, состоящий из: двухгорлой колбы-реактора, воздушного холодильника, приёмника, колпачка, газоотводной трубки, мерная пробирка |
| Реактивы (концентрации и как их приготовить, если необходимо): | Смесь этилового спирта и концентрированной серной кислоты (по 8-10 мл каждого вещества), 5-6 мл воды, 5 г бромида натрия (или бромида калия) |
| Информация о приборе, в котором проводится опыт (рисунок прибора, с обозначением, составных частей и описанием принципа действия) |         2 4 3 1 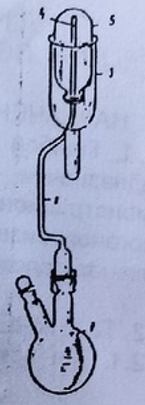 Прибор состоит из: 1-двухгорлая колба реактора, 2-воздушный холодильник, 3-приёмник с суженной нижней частью, 4-газоотводная трубка, 5-колпачок |
| Техника выполнения опыта. Последовательность операций |
|
| Техника безопасности и экологическая грамотность при проведении опыта |
|
| Время проведения опыта | 5-10 минут |
Заполняется с обратной стороны листа
| Методика проведения опыта | |
| Цель и задачи опыта | Цель: получить бромэтан методом непрямого галогенирования спиртов. Задачи: 1. Ознакомить учеников со способом непрямого галогенирования спиртов. 2. Закрепить знания по способам получения галогеналканов и химическим свойствам спиртов. 4. Выработать навыки обращения с химической посудой, реактивами. |
| Вопросы, подготавливающие учащихся к восприятию опыта: (актуализация знаний, постановка учебной проблемы) | Какие способы получения галогеналканов вам знакомы? Можно ли из спирта и советующих реактивов, содержащих галоген, получить галогеналкан? |
| Методические приемы, направленные на организацию наблюдения учащихся Вопросы учителя: Способы сочетания слова и действий учителя | Метод «Преднамеренная ошибка». Выводится на слайд фотография установки для получения, учитель начинает собирает, но неправильно, дети замечают и реагируют. 1)Почему сначала наливают спирт, а потом – кислоту? 2) Зачем для проведения опыта необходима концентрированная H2SO4? Учитель сначала сообщает школьникам сведения о таких свойствах, процессах или закономерностях, которые они не смогут познать непосредственно восприятием, а затем демонстрирует опыт. |
| Вопросы, подводящие к выводу Запись уравнений химических реакций (и их комментирование) | Зная какие реактивы будут смешаны между собой, можете ли предположить какие продукты протекающих реакций будут? Химизм процесса: С2Н5ОН + НО—SO3Н → С2Н5 – О – S03H + Н2О этилсерная кислота КВr + H2SO4 → НВr + KHSO4 (обратимая реакция) гидросульфат калия С2Н5 – О – S03H + HBr → C2H5Br + H2SO4 бромистый этил Побочный процесс: 2HBr + H2SO4 → Br2 + 2H2O +SO2 Наиболее удобным способом получения галогеналкалов является замещение гидроксильной группы спиртов R—ОН на галоген. Получение галогенопроизводных из спиртов применяется в больших масштабах, так как спирты – легкодоступные и хорошо изученные соединения. Вода в данной системе смещает равновесие в сторону исходных веществ, поэтому добавляют серную кислоту, так как она образует прочные гидраты, действуя при этом водопоглотителем. |
| Теоретическое обоснование результатов эксперимента Обобщение наблюдений Формулировка выводов | Данная реакция-реакция нуклеофильного замещения гидроксильной группы на галоген. Многие важные реакции спиртов осуществляются путем атаки a-атома углерода (электрофильного центра) нуклеофилом. В результате происходит разрыв связи С-О и замещение гидроксильной группы. Бромэтан – это прозрачная, слегка желтоватого цвета жидкость, токсичен, маслянистой структуры. При получении бромэтан скапливается на дне склянки, то есть тяжелее воды. Путем непрямого галогенирования этилового спирта, то есть взаимодействием этилсульфата с бромоводородом, мы получили бромэтан, который имеет следующие физические свойства: прозрачная жидкость слегка желтого цвета, токсичен. |


