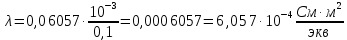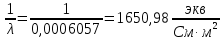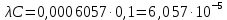Файл: Определение степени диссоциации слабого электролита.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.02.2024
Просмотров: 12
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
ПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ РОССИИ

МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ
ФЕДЕРАЦИИ
Федеральное государственное бюджетное образовательное учреждение высшего
образования
«САНКТ-ПЕТЕРБУРГСКИЙ ГОРНЫЙ УНИВЕРСИТЕТ»
Кафедра общей и физической химии
Лабораторная работа №1
По дисциплине:Химия, часть 2
Тема: Определение степени диссоциации слабого электролита
кондуктометрическим способом
Выполнили: ст. группы НБШ – 21 /Федорова А.Р./
(должность) (подпись) (Ф.И.О)
Проверил: доцент / Сергеев В.В. /
(должность) (подпись) (Ф.И.О)
РЕФЕРАТ
Вопрос диссоциации электролитов в растворе занимал многих ученых, в том числе Вант-Гоффа и Аррениуса. Было замечено, что изотонический коэффициент iвыражается не целыми числами, как это могло быть, если бы электролиты на ионы диссоциировали полностью, а дробными, которые с разбавлением раствора, возрастая, приближаются к целым числам.
Как объяснил Аррениус, в растворе лишь часть электролита диссоциирует на ионы. Он ввел понятие степени диссоциации электролита для количественного описания данного явления.
Позднее установили, что электролиты можно разделить на сильные и слабые, причем для первых понятие степени диссоциации неприменимо: они распадаются на ионы в растворе практически без остатка, а отклонение изотонического коэффициента обуславливается взаимным притяжением противоположных ионов друг к другу.
Так как слабые электролиты диссоциируют частично, то в растворе устанавливается динамическое равновесие между ионами и недиссоциированными молекулами. К слабым электролитам относятся едва ли не все органические кислоты и основания, например амины, малорастворимые и нерастворимые неорганические вещества, некоторые растворимые кислоты (Н2СО3, H2S, HCN) и основания (NH4OH).
Метод кондктометрического анализа заключается в исследовании зависимости концентрации электролита от электропроводности раствора. Кондуктометрическое титрование, одна из разновидностей кондуктометрии, – способ определения содержания вещества по излому кривой титрования. Связь между электропроводностью раствора и концентрацией веществав 1885 году ввел немецкий физик Кольрауш.
Различные методы кондуктометрии могут быть использованы практически для любых реакций и сред, например, высокочастотное кондуктометрическое титрование характеризуется отсутствием контакта электродов со средой, что применяется при исследованиях алкалоидов и фармацевтичеких препаратов.
В настоящее время существуют методики, основанные на методе кондуктометрии, для определения количества поваренной соли в сычужном сырье (пищевая промышленность), малых количеств углерода в сталях металлов и даже для изучения фитопланктона, концентрации и размеров клеток с помощью кондутометрического цитометра.
ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ
В настоящем отчете применяются следующие термины с соответсвтующими определениями:
| Степень диссоциации | - отношение числа его молекул, распавшихся в данном растворе на ионы,к общему числу его молекул в растворе. |
| Слабый электролит | - электролиты, частично диссоциирующие в водном растворе с установлением динамического равновесия между ионами и недиссоциированными молекулами в растворе. |
| Кондуктометрическое титрование | - метод анализа, основанный на определении эквивалентного объема титранта путем последовательного измерения электрической проводимости анализируемого раствора после добавления очередной порции взаимодействующего с ним титранта. |
| Удельная электропроводность | - мера способности вещества проводить электрический ток. |
| Концентрация | - величина, количественно характеризующая содержание компонента относительно всей смеси. |
| Титрант | - раствор определенного реагента известной концентрации, который вступает в реакцию с аналитом пробы. |
| Кривая титрования | - кривая титрования – это график зависимости концентрации (или логарифма концентрации) формы определяемого компонента от доли титрования, объема или количества молей добавленного титранта. |
| Нормальная концентрация | - количество эквивалентов данного вещества в 1 литре смеси. |
| Эквивалентная электропроводность | - это мера проводимости всех ионов, образующихся при диссоциации1 эквивалента электролита при данной концентрации |
ОСНОВНАЯ ЧАСТЬ
Цель работы
Получить зависимость удельной электропроводности от содержания слабого электролита в растворе, проанализировать концентрацию раствора слабой кислоты методом кондуктометрического титрования.
Используемое оборудование
Кондуктометр; магнитная мешалка; химический стакан объемом 100 мл – 5 шт.; химический стакан объемом 50 мл – 1 шт.; химический стакан объемом 250 мл – 1 шт.; мерные колбы объемом 250 мл – 4 шт.; мерная пипетка объемом 50 мл – 1 шт.; мерная пипетка объемом 10 мл – 1 шт.; бюретка для титрования объемом 25 мл – 1 шт.; гидроксид натрия – раствор 1 моль/л; слабая кислота – СН3СООН– раствор 1 моль/л.
Ход эксперимента
Приготовить 4 последовательно разведенных раствора уксусной кислоты. Отобрать пробы в стакан и измерить кондуктометром удельную электропроводность растворов, начиная с самого разбавленного, полностью погружая электроды в раствор и промывая их соответсвующим исследуемым раствором перед каждым измерением.
Для получения данных построения кривой титрования подготовить бюретку, залить в нее раствор щелочи и довести нижний мениск жидкости до нуля, отобрать пробу (аликвоту) уксусной кислоты в химический стакан 250 мл, поставить его на магнитную мешалку, погрузить в стакан электрод, дистиллированной водой довести уровень жидкости в стакане до полного покрытия ею электродов, включить магнитную мешалку, определить показания кондуктометра, через каждые 2 минуты добавлять к кислоте 1 мл раствора щелочи и записывать показания прибора, продолжать титрование до 20 мл использованного раствора щелочи.
Содержание протокола
Таблица 1 – Результаты исследования
| Наименование слабого электролита | уксусная кислота |
| Химическая формула слабого электролита | 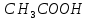 |
| Ориентировочное значение концентрации слабого электролита 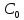 , моль/л , моль/л | 0,5 |
| Концентрация титранта 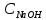 , моль/л , моль/л | 1 |
| Объем пробы слабого электролита, взятого для титрования 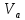 , мл , мл | 10 |
Таблица 2 – Зависимость удельной электропроводности от концентрации слабого электролита
| № колбы | Концентрация, моль/л (по ориентировочному значению) | Удельная электропроводность χ, мкСм/см |
| 1 | 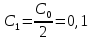 | 605,7 |
| 2 | 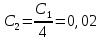 | 282,7 |
| 3 | 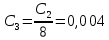 | 129,8 |
| 4 | 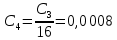 | 55,12 |
Таблица 3 – Индивидуальное контрольное задание
| № п/п | 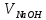 ,мл ,мл | Удельная электропроводность χ, мкСм/см |
| 1 | 0 | 1453,7 |
| 2 | 1 | 1555,9 |
| 3 | 2 | 1723 |
| 4 | 3 | 1819 |
| 5 | 4 | 2229 |
| 6 | 5 | 2593 |
| 7 | 6 | 3165 |
| 8 | 7 | 3466 |
| 9 | 8 | 3944 |
| 10 | 9 | 4358 |
| 11 | 10 | 4746 |
| 12 | 11 | 5345,0 |
| 13 | 12 | 6549,0 |
| 14 | 13 | 8032,0 |
| 15 | 14 | 9118,0 |
| 16 | 15 | 10510,0 |
| 17 | 16 | 11281,0 |
| 18 | 17 | 12450,0 |
| 19 | 18 | 13460,0 |
Продолжение таблицы 3
| 20 | 19 | 14580,0 |
| 21 | 20 | 15830,0 |
Обработка результатов
1 Построение и исследование кривой кондуктометрического титрования
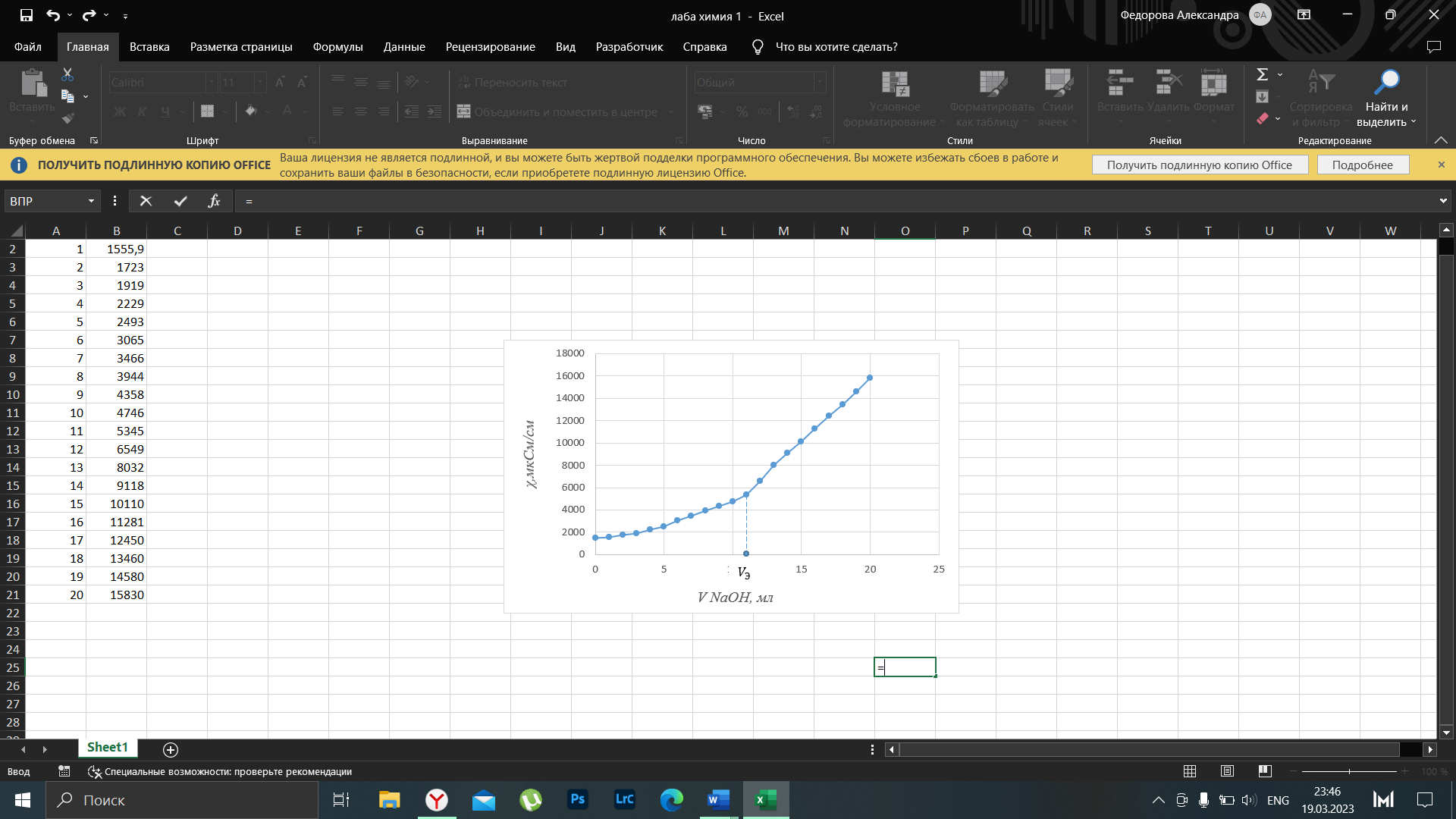
Рисунок 1 – Обработанное изображение кондуктометрической кривой титрования.
По графику эквивалентный объем щелочи
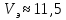 мл.
мл.Точное значение концентрации слабого электролита вычисляется по формуле:
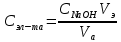 | (1) |
где
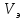 – эквивалентный объем щелочи, определенный по кривой титрования, мл;
– эквивалентный объем щелочи, определенный по кривой титрования, мл;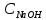 – концентрация раствора щелочи, экв./л;
– концентрация раствора щелочи, экв./л;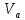 – объем аликвоты слабого электролита, мл.
– объем аликвоты слабого электролита, мл.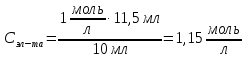
2 Определение константы и степени диссоциации слабого электролита
2.1 Вычисление эквивалентной электропроводности каждого раствора по
формуле:
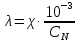 | (2) |
где
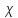 – удельная электропроводность, См/м;
– удельная электропроводность, См/м;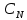 – нормальная концентрация раствора слабого электролита, экв/л.
– нормальная концентрация раствора слабого электролита, экв/л.Пример расчета эквивалентной электропроводности для СN=0,1экв/л. Для последующих значений вычисления проведены аналогично.