ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.02.2024
Просмотров: 87
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
сдавливаются сосуды и нервы, что усугубляет нарушения трофики тканей у тяжелобольных, страдающих сердечно-сосудистыми, онкологическими, инфекционными или нервными болезнями.
Б. Колликвационный (влажный) некроз
Характеризуется расплавлением мертвой ткани. Он развивается в тканях, относительно бедных белками и богатых жидкостью, где имеются благоприятные условия для гидролитических процессов. Лизис клеток происходит в результате действия собственных ферментов (аутолиз). Типичным примером влажного колликвационного некроза является очаг серого размягчения (ишемический инфаркт) головного мозга.
Исход некроза.
Благоприятные исходы некроза:
Неблагоприятные исходы некроза:
Апоптоз, или запрограммированная смерть клетки, представляет собой процесс, посредством которого внутренние или внешние факторы, активируя генетическую программу, приводят к гибели клетки и ее эффективному удалению из ткани. Морфологически апоптоз проявляется гибелью единичных, беспорядочно расположенных клеток, что сопровождается формированием округлых, окруженных мембраной телец (“апоптотические тельца”), которые тут же фагоцитируются окружающими клетками.
Это энергозависимый процесс, посредством которого удаляются нежелательные и дефектные клетки организма. Он играет большую роль в морфогенезе и является механизмом постоянного контроля размеров органов. При снижении апоптоза происходит накопление клеток, пример – опухолевый рост. При увеличении апоптоза наблюдается прогрессивное уменьшение количества клеток в ткани, пример – атрофия.
Морфологические проявления апоптоза
Апоптотические клетки выглядят как округлые или овальные скопления интенсивно эозинофильной цитоплазмы с плотными фрагментами ядерного хроматина. Поскольку сжатие клетки и формирование апоптотических телец происходит быстро и также быстро они фагоцитируются, распадаются или выбрасываются в просвет органа, то на гистологических препаратах он обнаруживается в случаях его значительной выраженности. К тому же апоптоз – в отличие от некроза – никогда не
сопровождается воспалительной реакцией, что также затрудняет его гистологическое выявление.
Сравнительная характеристика некроза и апоптоза
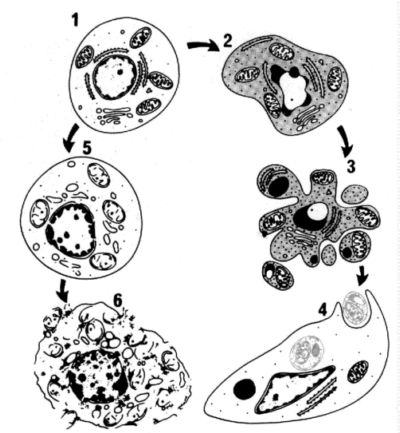
Рис. 1. Последовательность ультраструктурных изменений при апоптозе (справа) и некрозе (слева)
1 – нормальная клетка; 2 – начало апоптоза; 3 – фрагментация апоптотической клетки; 4 – фагоцитоз апоптотических телец окружающими клетками; 5 – гибель внутриклеточных структур при некрозе; 6 – разрушение клеточной мембраны.
Апоптоз принимает участие в следующих физиологических и патологических процессах:
Регуляция апоптоза
Апоптоз это генетически контролируемая смерть клетки. В настоящее время выявлено большое число генов, которые кодируют вещества, необходимые для регуляции апоптоза.
Апоптоз может регулироваться:
Лекция №3. Дисторофии
Дистрофия (от греч. dys – нарушение и trophо – питаю) – это количественные и качественные структурные изменения в клетках и/или межклеточном веществе органов и тканей, обусловленные нарушением обменных процессов. При дистрофиях в результате нарушения трофики в клетках или в межклеточном веществе накапливаются различные продукты обмена (белки, жиры, углеводы, минералы, вода). Морфологическая сущность дистрофий выражается в:
Таким образом, дистрофия является морфологическим выражением нарушений метаболизма клеток и тканей.
Среди механизмов поддержания нормальной трофики выделяют клеточные и внеклеточные.
Клеточные механизмы обеспечиваются структурной организацией клетки и ее ауторегуляцией, обеспечивающейся генетическим кодом.
Внеклеточные механизмы трофики обеспечиваются транспортными (кровь, лимфа) и интегративными (нервная, эндокринная, гуморальная) системами ее регуляции.
Непосредственной причиной развития дистрофий могут служить:
Морфогенез дистрофий
Среди механизмов, ведущих к развитию характерных для дистрофий изменений, различают инфильтрацию, декомпозицию (фанероз), извращенный синтез и трансформацию.
Инфильтрация – избыточное проникновение продуктов обмена из крови и лимфы в клетки или межклеточное вещество и/или нарушение включения их в метаболизм с последующим накоплением. Например, инфильтрация белком эпителия проксимальных канальцев почек при нефротическом синдроме, инфильтрация липопротеидами интимы аорты и крупных артерий при атеросклерозе.
Декомпозиция (фанероз) – распад сложных в химическом отношении веществ. Например, распад липопротеидных комплексов и накопление в клетке жира в свободном состоянии (жировая дистрофия кардиомиоцитов при дифтерийной интоксикации). Распад полисахаридно-белковых комплексов лежит в основе фибриноидных изменений соединительной ткани при ревматических болезнях.
Трансформация – переход одного вещества в другое. Такова, например, трансформация углеводов в жиры при сахарном диабете, усиленная полимеризация глюкозы в гликоген и др.
Извращенный синтез – это синтез в клетках или в тканях веществ, не встречающихся в них в норме. К ним относятся: синтез аномального белка амилоида в клетке и образование аномальных белково-полисахаридных комплексов амилоида в межклеточном веществе, синтез белка алкогольного гиалина гепатоцитом, синтез гликогена в эпителии узкого сегмента нефрона при сахарном диабете.
Классификация.
В зависимости от локализации нарушений обмена:
Б. Колликвационный (влажный) некроз
Характеризуется расплавлением мертвой ткани. Он развивается в тканях, относительно бедных белками и богатых жидкостью, где имеются благоприятные условия для гидролитических процессов. Лизис клеток происходит в результате действия собственных ферментов (аутолиз). Типичным примером влажного колликвационного некроза является очаг серого размягчения (ишемический инфаркт) головного мозга.
Исход некроза.
Благоприятные исходы некроза:
-
лизис; -
организация, на месте некроза в таких случаях образуется рубец (рубец на месте инфаркта). -
инкапсуляция; -
петрификация; -
оссификация; -
образование кисты.
Неблагоприятные исходы некроза:
-
гнойное (септическое) расплавление очага омертвения; -
секвестрация - это формирование участка мертвой ткани, который не подвергается аутолизу и организации. Секвестры обычно возникают в костях при воспалении костного мозга - остеомиелите. Вокруг такого секвестра образуется секвестральная капсула и полость, заполненная гноем; -
мутиляция - отторжение некротизированных тканей.
Апоптоз, или запрограммированная смерть клетки, представляет собой процесс, посредством которого внутренние или внешние факторы, активируя генетическую программу, приводят к гибели клетки и ее эффективному удалению из ткани. Морфологически апоптоз проявляется гибелью единичных, беспорядочно расположенных клеток, что сопровождается формированием округлых, окруженных мембраной телец (“апоптотические тельца”), которые тут же фагоцитируются окружающими клетками.
Это энергозависимый процесс, посредством которого удаляются нежелательные и дефектные клетки организма. Он играет большую роль в морфогенезе и является механизмом постоянного контроля размеров органов. При снижении апоптоза происходит накопление клеток, пример – опухолевый рост. При увеличении апоптоза наблюдается прогрессивное уменьшение количества клеток в ткани, пример – атрофия.
Морфологические проявления апоптоза
Апоптотические клетки выглядят как округлые или овальные скопления интенсивно эозинофильной цитоплазмы с плотными фрагментами ядерного хроматина. Поскольку сжатие клетки и формирование апоптотических телец происходит быстро и также быстро они фагоцитируются, распадаются или выбрасываются в просвет органа, то на гистологических препаратах он обнаруживается в случаях его значительной выраженности. К тому же апоптоз – в отличие от некроза – никогда не
сопровождается воспалительной реакцией, что также затрудняет его гистологическое выявление.
Сравнительная характеристика некроза и апоптоза
| Признак | Апоптоз | Некроз |
| Индукция | Активируется физиологическими или патологическими стимулами | Различная в зависимости от повреждающего фактора |
| Распространенность | Одиночная клетка | Группа клеток |
| Биохимические изменения | Энергозависимая фрагментация ДНК эндогенными эндонуклеазами. Лизосомы интактные. | Нарушение или прекращение ионного обмена. Из лизосом высвобождаются ферменты. |
| Распад ДНК | Внутриядерная конденсация с расщеплением на фрагменты | Диффузная локализация в некротизированной клетке |
| Целостность клеточной мембраны | Сохранена | Нарушена |
| Морфология | Сморщивание клеток и фрагментация с формированием апоптотических телец с уплотненным хроматином | Набухание и лизис клеток |
| Воспалительный ответ | Нет | Обычно есть |
| Удаление погибших клеток | Поглощение (фагоцитоз) соседними клетками | Фагоцитоз нейтрофилами и макрофагами |

Рис. 1. Последовательность ультраструктурных изменений при апоптозе (справа) и некрозе (слева)
1 – нормальная клетка; 2 – начало апоптоза; 3 – фрагментация апоптотической клетки; 4 – фагоцитоз апоптотических телец окружающими клетками; 5 – гибель внутриклеточных структур при некрозе; 6 – разрушение клеточной мембраны.
Апоптоз принимает участие в следующих физиологических и патологических процессах:
-
запрограммированном разрушении клеток во время эмбриогенеза (включая имплантацию, органогенез); -
гормон-зависимой инволюции органов у взрослых, например, отторжение эндометрия во время менструального цикла, атрезии фолликулов в яичниках в менопаузе и регрессия молочной железы после прекращения лактации; -
удалении некоторых клеток при пролиферации клеточной популяции; -
гибели отдельных клеток в опухолях, в основном при ее регрессии, но также и в активно растущей опухоли; -
гибели клеток иммунной системы, как В-, так и Т-лимфоцитов, после истощения запасов цитокинов, а также гибели аутореактивных Т-клеток при развитии в тимусе; -
патологической атрофии паренхиматозных органов после обтурации выводных протоков, что наблюдается в поджелудочной и слюнных железах, почках; -
гибели клеток, вызванных действием цитотоксических Т-клеток, например, при отторжении трансплантата и болезни “трансплантат против хозяина”; -
повреждении клеток при некоторых вирусных заболеваниях, например, при вирусном гепатите, когда фрагменты апоптотических клеток обнаруживаются в печени, как тельца Каунсильмана.
Регуляция апоптоза
Апоптоз это генетически контролируемая смерть клетки. В настоящее время выявлено большое число генов, которые кодируют вещества, необходимые для регуляции апоптоза.
Апоптоз может регулироваться:
-
внешними факторами, -
автономными механизмами.
Лекция №3. Дисторофии
Дистрофия (от греч. dys – нарушение и trophо – питаю) – это количественные и качественные структурные изменения в клетках и/или межклеточном веществе органов и тканей, обусловленные нарушением обменных процессов. При дистрофиях в результате нарушения трофики в клетках или в межклеточном веществе накапливаются различные продукты обмена (белки, жиры, углеводы, минералы, вода). Морфологическая сущность дистрофий выражается в:
-
увеличении или уменьшении количества каких-либо веществ, содержащихся в организме в норме (например, увеличение количества жира в жировых депо); -
изменении качества, то есть физико-химических свойств веществ, присущих организму в норме (например, изменение тинкториальных свойств коллагеновых волокон при мукоидном набухании и фибриноидных изменениях); -
появлении обычных веществ в необычном месте (например, накопление жировых вакуолей в цитоплазме клеток паренхиматозных органов при жировой дистрофии); -
появлении и накоплении новых веществ, которые не присущи для него в норме (например, белка амилоида).
Таким образом, дистрофия является морфологическим выражением нарушений метаболизма клеток и тканей.
Среди механизмов поддержания нормальной трофики выделяют клеточные и внеклеточные.
Клеточные механизмы обеспечиваются структурной организацией клетки и ее ауторегуляцией, обеспечивающейся генетическим кодом.
Внеклеточные механизмы трофики обеспечиваются транспортными (кровь, лимфа) и интегративными (нервная, эндокринная, гуморальная) системами ее регуляции.
Непосредственной причиной развития дистрофий могут служить:
-
Токсические вещества (в том числе токсины микроорганизмов). -
Физические и химические агенты: высокая и низкая температуры, определенные химические вещества (кислоты, щелочи, соли тяжелых металлов, многие органические вещества), ионизирующая радиация. -
Приобретенная или наследственная ферментопатия (энзимопатия). -
Вирусы. -
Нарушения функции энергетических и транспортных систем, обеспечивающих метаболизм и структурную сохранность тканей (клеток), при которых имеет место:-
Гипогликемия. Низкий уровень глюкозы в крови (гипогликемия) приводит к недостаточному производству молекул аденозинтрифосфата (АТФ), что наиболее выражено в головном мозге. -
Гипоксия: Недостаток кислорода в клетках (гипоксия) может возникать при:
-
-
обструкции дыхательных путей или болезни, предотвращающей оксигенацию крови в легких; -
ишемии, или нарушении тока крови в тканях в результате общих или местных нарушений циркуляции крови; -
анемии (то есть, при снижении уровня гемоглобина в крови), что приводит к снижению транспорта кислорода кровью; -
нарушении структуры гемоглобина (например, при отравлении угарным газом (СО)), при этом образуется метгемоглобин, не способный к переносу кислорода; это приводит к такому же результату, что и при анемии.
-
Нарушения эндокринной и нервной регуляции: -
Заболевания эндокринных органов (тиреотоксикоз, диабет, гиперпаратиреоз и т.д.) -
Болезни центральной и периферической нервной систем (нарушенная иннервация, опухоли головного мозга).
Морфогенез дистрофий
Среди механизмов, ведущих к развитию характерных для дистрофий изменений, различают инфильтрацию, декомпозицию (фанероз), извращенный синтез и трансформацию.
Инфильтрация – избыточное проникновение продуктов обмена из крови и лимфы в клетки или межклеточное вещество и/или нарушение включения их в метаболизм с последующим накоплением. Например, инфильтрация белком эпителия проксимальных канальцев почек при нефротическом синдроме, инфильтрация липопротеидами интимы аорты и крупных артерий при атеросклерозе.
Декомпозиция (фанероз) – распад сложных в химическом отношении веществ. Например, распад липопротеидных комплексов и накопление в клетке жира в свободном состоянии (жировая дистрофия кардиомиоцитов при дифтерийной интоксикации). Распад полисахаридно-белковых комплексов лежит в основе фибриноидных изменений соединительной ткани при ревматических болезнях.
Трансформация – переход одного вещества в другое. Такова, например, трансформация углеводов в жиры при сахарном диабете, усиленная полимеризация глюкозы в гликоген и др.
Извращенный синтез – это синтез в клетках или в тканях веществ, не встречающихся в них в норме. К ним относятся: синтез аномального белка амилоида в клетке и образование аномальных белково-полисахаридных комплексов амилоида в межклеточном веществе, синтез белка алкогольного гиалина гепатоцитом, синтез гликогена в эпителии узкого сегмента нефрона при сахарном диабете.
Классификация.
В зависимости от локализации нарушений обмена:

