ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 08.02.2024
Просмотров: 7
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Практическая работа №7
Тема: Расчет термодинамических процессов
Цель работы: Научиться рассчитывать термодинамические процессы
Студент должен знать:
- термодинамические процессы и их характеристики;
Уметь:
- производить расчёты термодинамических процессов.
Теоретическое обоснование
Последовательно изменение состояния тела, происходящее в результате энергетического взаимодействия рабочего с окружающей его средой, называется термодинамическим процессом. В термодинамическом процессе обязательно изменяется хотя бы один параметр состояния.
Простейшими или термодинамическими процессами являются:
Изохорный(v = const), изобарный(P = const), изотермический (T = const) и адиабатный (процесс без внешнего теплообмена) .
Для расчётов термодинамических процессов используют первый закон термодинамики, которому можно дать такую формулировку: в термодинамическом процессе подведенная теплота в общем случае расходуется на изменение внутренней энергии и на совершение внешней работы:
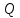 =
= 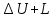
Для 1 кг вещества выражение закона термодинамики запишется так:
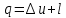
Или в дифференциальной форме:
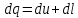
Следует обратить внимание на то, что хотя величины входящие в уравнение первого закона термодинамики имеют одинаковую размерность, физические понятия определяющие эти величины глубоко различны. Внутренняя энергия представляет собой энергию, накопленную телом (системой), а работа и теплота – энергию, которая сообщается или отнимается от тела в каком-либо процессе.
Задачей расчёта любого термодинамического процесса является установление закономерностей изменения параметров состояния рабочего тела, и выявления особенностей превращения энергии.
Расчёт проводится в следующем порядке:
- записывается уравнение процесса
;
- устанавливается зависимость между параметрами в процессе;
- определяется неизвестные параметры;
- определяется работа в процессе;
- определяется теплота, необходимая для осуществления процесса;
- определяется изменение энтальпии и энтропии между начальным и конечным состояниями процесса.
Соотношение параметров в изохорном процессе:
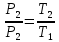
Изменение внутренней энергии определяется по формуле:
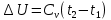 , (кДж/кг)
, (кДж/кг)Где
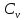 -
- 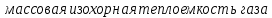 (Дж/кгК).
(Дж/кгК).В изохорном процессе dV = 0 и термодинамическая работа не совершается L=0. Поэтому вся теплота расходуется на изменение внутренней энергии, т.е.
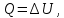 (Дж)
(Дж)Изменение энтальпии может быть найдено из общего выражения для всех процессов:
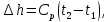 (Дж/кг)
(Дж/кг)Где Ср – изобарная массовая теплоёмкость (кДж/кг*К)
Изменение энтропии с учётом того, что V1 = V2
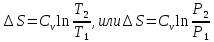
Соотношение параметров в изобарном процессе:
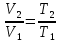
Работа в процессе, отнесенная на 1 кг газа определяется по формуле:
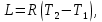 (Дж/кг)
(Дж/кг)Если в изобарном процессе изменяется температура 1 кг на 1К, то 1 = R, т.е. газовая постоянная – это работа 1 кг газа в изобарном процессе при изменении температуры на 1К.
Количество теплоты в изобарном процессе:
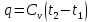 , (Дж/кг)
, (Дж/кг)Изменение энтальпии:
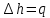
Изменение энтропии:
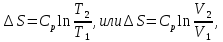 (Дж/кг)
(Дж/кг)Уравнение изометрического процесса:
PV = RT = const
Соотношение параметров:
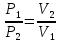
Изменение внутренней энергии и энтальпии:
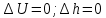
Т.к. dT = 0. Следовательно, вся подведенная в процессе теплота расходжуется только на работу. Раьота в процессе определяется по формуле:
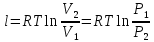
Теплоту в процессе можно определить также используя энтропию:
q = T(S2 – S1)
Т.е. в изометрическом процессе достаточно определить теплоту или работу, т.к.
q = l
Изменение энтропии при T1 = T2 определяется по формуле:
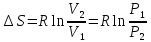
Уравнение адиабатного процесса:
PVk = const
Где k – показатель адиабаты.
Соотношение параметров, полученные из уравнения процесса:
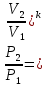
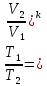
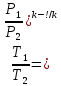
Выражение для работы в процессе может быть получено из первого закона термодинамики, с учётом того, что q=0:
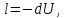 или
или 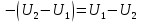
Т.е. в адиабатном процессе работа совершается за счёт убыли внутренней энергии. Работу можно определить по формулам:
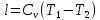
Или с учётом
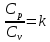
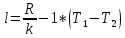
Подставим из уравнения состояния T1 и Т2:
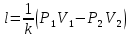
Или
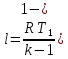
Изменение энтальпии находится по общему выражению.
Изменение энтропии равно 0, т.к. dq = 0
dS = dq/T = 0
Следовательно, в адиабатном процессе s = const. Поэтому обратимый адиабатный процесс называется изоэнтропийным.
Ход работы
1. Ознакомиться с теоретическим положением.
2. Произвести расчёт термодинамического процесса заданного преподавателем.
3. Проанализировать полученные результаты.
4. Ответить на контрольные вопросы.
Задача № 1
Рассчитать термодинамический процесс изотермического сжатия газа азота при заданных параметрах.
| Вариант | Р1,МПа | Р2,МПа | T1 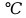 |
| 1 2 3 4 5 6 7 8 9 10 | 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 0.4 0.5 | 10 30 20 40 50 60 70 80 90 50 | 25 34 46 47 68 70 13 25 30 45 |
Задача № 2
Рассчитать изохорный процесс для кислорода при заданных параметрах.
| Вариант | V1, м3 | Р1,МПа | T2 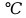 |
| 1 2 3 4 5 6 7 8 9 10 | 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 0.4 0.5 | 10 30 20 40 50 60 70 80 90 50 | 125 134 146 147 168 170 113 125 130 145 |
Задача № 3
Рассчитать адиабатный процесс сжатия водорода при заданных параметрах.
| Вариант | V1, м3 | Р1,МПа | T2 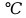 |
| 1 2 3 4 5 6 7 8 9 10 | 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 0.4 0.5 | 10 30 20 40 50 60 70 80 90 50 | 125 134 146 147 168 170 113 125 130 145 |
В каком термодинамическом процессе
- не совершается работа?
-не происходит теплообмен
-не изменяется внутренняя энергии?
Содержание отчета:
-
Тема, номер и цель работы. -
Расчёт термодинамических процессов по заданию варианта. -
Ответы на контрольные вопросы.
Контрольные вопросы:
-
Перечислите основные термодинамические процессы -
Сформулируйте первый закон термодинамики. -
Опишите порядок расчёта термодинамического процесса.
Литература
1. Брюханов, О.Н. Основы гидравлики, теплотехники и аэродинамики[Текст]: учеб. / О.Н. Брюханов и др. - М.: НИЦ ИНФРА-М, 2014. - 254 с.(ЭБС Znanium.com). Режим доступа: http://znanium.com/catalog.php?item=bookinfo&book=420324
2. Гидравлика, пневматика и термодинамика [Электронный ресурс]: курс лекций / В.М. Филин; под ред. В.М. Филина. - М.: ИД ФОРУМ: НИЦ ИНФРА-М, 2015. - 320 с.
(ЭБС Znanium.com). Режим доступа: http://znanium.com/catalog.php?item=bookinfo&book=478661


