Файл: Учебник для 10 классов общеобразовательных школ естественноматематического направления. А. Мектеп. 2019 1 часть Ход занятия.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 08.02.2024
Просмотров: 6
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
КГУ «Карагандинский индустриально-технологический колледж»
План учебного занятия
Тема занятия: Теории кислот и оснований
Наименование модуля /дисциплины : Химия
Подготовил педагог: Смайлова Г.Б.
«___»__________ 20___ года
1. Общие сведения
Курс, группы __________________
Тип занятия: Комбинированный урок
2. Цели, задачи: выявить особенности органических соединений, с точки зрения теории Бренстеда-Лоури (протолитическая теория) и теории Льюиса, научиться определять различия между теориями и отличительные особенности. Усвоение понятий кислота и основание с точки зрения разных теорий. Уметь писать уравнения реакций,
3. Ожидаемые результаты: Объяснять условия ионного равновесия в растворах электролитов и определять скорость протекания химической реакции.
4. Необходимые ресурсы: М.К.Оспанова, К.С.Аухадиева, Т.Г. Белоусова. Учебник для 10 классов общеобразовательных школ естественно-математического направления. А.Мектеп. 2019 1 часть
5. Ход занятия
Организационный момент
- Приветствовать студентов, отметить отсутствующих.
- Проверить подготовленность студентов к учебному занятию
Обьяснение нового материала: Определение кислот и оснований было предложено шведским химиком Аррениусом в конце XIX в рамках теории диссоциации.
-
Кислота – вещество, которое диссоциирует в воде с образованием ионов водорода. -
Основание – вещество, которое диссоциирует в воде с образованием гидроксид-ионов.
Данные определения иногда являются ограниченными и иногда неточными. Так, ион водорода Н+ не существует в воде, поскольку Н+ – голый протон, такая концентрация положительного заряда позволяет ему быстро реагировать с неподелённой парой на кислороде в молекуле воды:
Н2О + Н+ = Н3О+ (гидроксоний).
Кроме того, некоторые соединения не содержат ионов гидроксила ОН-, но все же обладают основными свойствами, например аммиак NH3. Поэтому существует более общее определение кислот и оснований, предложенное Брёнстедом и Лоури в начале XX века и широко используется в наши дни.
-
Кислота (acid) Брёнстеда-Лоури – донор протонов Н+. -
Основание (base) Брёнстеда-Лоури – ацептор протонов.
Затем на основе электронных представлений Льюисом было еще более расширено понятие кислоты и основания.
-
Кислота Льюиса – молекула или ион, имеющие вакантные электронные орбитали, вследствие этого они способны принимать электронные пары. -
Основание Льюиса – молекулы или ионы, способные быть донором электронных пар.
Кислоты и основания между собой классифицируются по способности отдавать Н+ или ОН-, т.е. по способности диссоциировать, или, проще говоря, по силе. Сильные кислоты легко отдают протон, по существу 100% кислоты диссоциирует на ионы. Слабая кислота диссоциирует с трудом, только небольшая её часть распадается на ионы. Точно такие же рассуждения применимы и для оснований.
Количественно способность к диссоциации выражается отношением числа продиссоциированных частиц (Nдисс.) к исходному числу частиц (Nисх.) и называется степенью диссоциации (
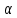 ):
):  | (16) |
Если α=1, то все исходные частицы в растворе распались на ионы, такие электролиты сильные. Если α<1, то только часть частиц распалась на ионы, такие электролиты слабые.
Процесс электролитической диссоциации протекает обратимо, поэтому можно применять принцип Ле Шателье. Разбавление раствора будет смещать равновесие в сторону увеличения степени диссоциации. Таким образом, диссоциация слабых электролитов в разбавленных растворах протекает лучше, чем в концентрированных. Применение закона действующих масс к электролитической диссоциации слабых электролитов позволяет получить выражение для константы диссоциации (К).
Рассмотрим, равновесие в водном растворе слабого электролита – уксусной кислоты:
CH3COOH
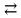 СH3COO- + H+
СH3COO- + H+Запишем выражение для константы химического равновесия данного процесса:
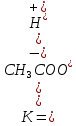
Поскольку константа равновесия не зависит от концентрации, поэтому константы диссоциации электролитов можно найти в справочных таблицах, для уксусной кислоты Ка=1,8·10-5, значение очень маленькое, это означает, что она будет посылать в раствор мало ионов и, соответственно, будет являться слабой. Это можно доказать, посчитав степень ее диссоциации, например в 0,1 М растворе:
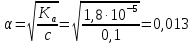 , что составляет всего 1,3 %. Т.е. только 1,3% всех молекул кислоты будут распадаться на ионы. Здесь α – степень диссоциации кислоты, а выражение для расчета степени диссоциации – есть закон разбавления Оствальда:
, что составляет всего 1,3 %. Т.е. только 1,3% всех молекул кислоты будут распадаться на ионы. Здесь α – степень диссоциации кислоты, а выражение для расчета степени диссоциации – есть закон разбавления Оствальда:| Ka ≈ c·α2, откуда 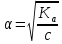 | (18) | | |||||||||||||||||
| Для кислот, имеющих больше одного атома водорода в своем составе, очевидно, что процесс диссоциации – это ступенчатый процесс, и каждая ступень характеризуется своей константой диссоциации (табл. 3). | Таблица. 3. Константа и степень диссоциации ортофосфорной кислоты
| ||||||||||||||||||
В водных растворах слабых оснований рассуждения идентичны, например диссоциация NH
4OH:
NH4OH
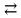 NH4+ + OH-.
NH4+ + OH-.Выражение для константы диссоциации водного раствора аммиака:
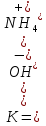
Общие выражения для расчета констант диссоциации кислоты
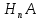 (19) и основания
(19) и основания 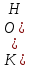
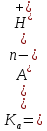 | (19) |
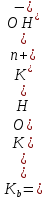 | (20) |
Закрепление: Давайте подведем итог сегодняшней беседы и сделаем небольшой вывод.
Кислотно-основные взаимодействия чрезвычайно распространены в природе и находят широкое применение в научной и производственной практике.
Теоретические представления о кислотах и основаниях имеют важное значение в формировании всех концептуальных систем химии и оказывают разностороннее влияние на развитие многих теоретических концепций во всех основных химических дисциплинах.
Классификация кислот. Соотнесите:
Тип кислот: Формула вещества:
-
Кислородсодержащие а) H2SiO3 -
бескислородные б) HCOOH -
одноосновные в) H2SO4 -
двухосновные г) HBr -
сильные д) HNO3 -
слабые
Домашнее задание: Изучите теоретический материал, и просмотрите записи в тетради.


