Файл: Отчет по лабораторной работе 1 По дисциплине Химия (наименование учебной дисциплины, согласно учебному плану).docx
Добавлен: 18.03.2024
Просмотров: 14
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Cr(OH)3 + OH- 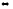 [Cr(OH)3]
[Cr(OH)3]
(осадок растворился)
Опыт 5.
NH4Cl + NaOH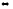 NH4OH + NaCl
NH4OH + NaCl
/ \
NH3 H2O
NH4+ + OH -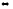 NH4OH
NH4OH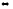 NH3(аммиак) + H2O
NH3(аммиак) + H2O
(прозрачный раствор, с резким запахом аммиака)
Ответы на вопросы:
Объясните появление запаха на основе уравнения реакции.
Опыт 6.
CuSO4 + 5NH3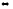 [Cu (NH3) 5] SO4
[Cu (NH3) 5] SO4
(получился темно-синий раствор)
Опыт 7(А).
Na2CO3 + H2SO4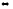 Na2SO4 + H2O + CO2 ↑
Na2SO4 + H2O + CO2 ↑
(бесцветный раствор, активное выделение углекислого газа)
Вывод: В ходе лабораторной работы ознакомились с практическими выводами теории электролитической диссоциации, с реакциями в растворах малорастворимых оснований, изучили свойства амфотерных гидроксидов, образование малодиссоциированных соединений, комплексных соединений и газов.
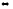 [Cr(OH)3]
[Cr(OH)3](осадок растворился)
Опыт 5.
NH4Cl + NaOH
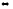 NH4OH + NaCl
NH4OH + NaCl/ \
NH3 H2O
NH4+ + OH -
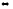 NH4OH
NH4OH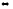 NH3(аммиак) + H2O
NH3(аммиак) + H2O(прозрачный раствор, с резким запахом аммиака)
Ответы на вопросы:
Объясните появление запаха на основе уравнения реакции.
Опыт 6.
CuSO4 + 5NH3
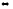 [Cu (NH3) 5] SO4
[Cu (NH3) 5] SO4(получился темно-синий раствор)
Опыт 7(А).
Na2CO3 + H2SO4
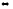 Na2SO4 + H2O + CO2 ↑
Na2SO4 + H2O + CO2 ↑(бесцветный раствор, активное выделение углекислого газа)
Вывод: В ходе лабораторной работы ознакомились с практическими выводами теории электролитической диссоциации, с реакциями в растворах малорастворимых оснований, изучили свойства амфотерных гидроксидов, образование малодиссоциированных соединений, комплексных соединений и газов.