Добавлен: 20.03.2024
Просмотров: 43
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Как и все летучие органические вещества, чистый формальдегид может находиться в одном из трех состояний- твердом, жидком или газообразном. Однако в этих состояниях фактически формальдегид может присутствовать в виде целого ряда модификаций, принципиально различающихся и по химическим, и тем более по физическим свойствам.
Во всем мире производится около 8 млн. тонн формальдегида в год. Формальдегид применяется в медицине, косметологии, но наиболее широкое применение он получил в промышленности, в частности для производства полимерных материалов. Формальдегид играет большую роль в фундаментальных реакциях и промышленном органическом синтезе, поэтому производство формальдегида является актуальной темой, требующей изучения и развития.
1. ФИЗИКО-ХИМИЧЕСКИЕ, ТЕХНОЛОГИЧЕСКИЕ СВОЙСТВА ФОРМАЛЬДЕГИДА
Формальдегид (СН2=О) (метаналь, муравьиный альдегид) - бесцветный газ с резким раздражающим запахом, хорошо растворим в воде, метаноле, этаноле и других полярных растворителях. При низких температурах смешивается в любых соотношениях с толуолом, диэтиловым эфиром, этилацетатом, хлороформом. Формальдегид горючий и токсичный газ. Предел взрыва ёмкости смесей с воздухом 7-73% (по объему). Формальдегид оказывает раздражающее действие на слизистые оболочки глаз, верхние дыхательные пути, вызывает дерматит. Формальдегид оказывает также общетоксическое, аллергическое и мутагенное действие на организм человека.
Смертельная доза 37% водного раствора формальдегида (формалина) составляет 10-50 г.
Основные физико-химические константы формальдегида приведены в таблице 1.
Таблица 1 - Физико-химические характеристики формальдегида
| | | | | |
| Показатель | Обозначение | Единица измерения | Значение | |
| Молекулярная масса | М | а.е.м. | 30,03 | |
| Плотность при -20 оС | с | г/см3 | 0,8153 | |
| Температура плавления | Т пл | оС | - 118 | |
| Температура кипения | Т кип | оС | - 19,5 | |
| Давление паров при -79,6 оС | Р | мм.рт.ст. | 20 | |
| Стандартная энтальпия образования | ДНообр. | кДж/моль | - 115,9 | |
| Энтальпия плавления | ДНопл. | кДж/моль | 23,3 | |
| Энтальпия испарения | ДНоисп. | кДж/моль | 23,3 | |
| Энтальпия сгорания | ДНосг. | кДж/моль | 570,8 | |
| Стандартная энергия образования Гиббса | ДоG | | - 110,0 | |
| Стандартная энергия образования | Sо | Дж/моль • К | 218,8 | |
| Стандартная мольная теплоёмкость | Сор | Дж/моль • К | 35,35 | |
| Предельно допустимая концентрация | | | | |
| в воздухе рабочей зоны | ПДК | мг/м3 | 0,5 | |
| максимально-разовая | | мг/м3 | 0,035 | |
| среднесуточная | | мг/м3 | 0,003 | |
2. ПРОИЗВОДСТВО ФОРМАЛЬДЕГИДА ОКИСЛИТЕЛЬНЫМ ДЕГИДРИРОВАНИЕМ МЕТАНОЛА
Вследствие этого и, следовательно, малого выхода формальдегида технологический процесс прямого окисления метана становится экономически невыгодным. Основная масса формальдегида производится поэтому из метанола по двум методам: окислительным дегидрированием и окислением.
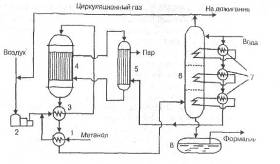
1, 3 -- теплообменники, 2 -- турбокомпрессор, 4 -- реактор, 5 -- котел-утилизатор, 6 --абсорбер, 7 -- выносные теплообменники, 8 -- сборник формалина
Съем тепла и тепловой режим в реакторе обеспечивается хладоагентом, циркулирующим через котел-утилизатор 5. Реакционная смесь, выходящая из реактора 4, охлаждается в теплообменниках 3 и 1и поступает в абсорбер 6, орошаемый водой. Тепло абсорбции отводится и утилизируется в выносных теплообменниках 7, подогревающих обессоленную воду, подаваемую на абсорбцию и питающую котел-утилизатор 5, вырабатывающий технологический пар. Образующийся формалин выводится из нижней части абсорбера и поступает в сборник 8. Часть отходящих из верхней части абсорбера б газов смешивается с воздухом перед входом его в реактор для снижения взрывоопасности смеси воздуха с парами метанола, а остальное количество их направляется в печь для дожигания (на схеме не указана) и выбрасывается в атмосферу. Из нижней части абсорбера вытекает формалин-водныйраствор формальдегида, содержащий 37,6% НСНО и около 10% СН3ОН. Метиловый спирт стабилизирует формальдегид, предотвращая его полимеризацию. Формалин направляют на склад как товарную продукцию. Для получения концентрированного формальдегида формалин подвергают ректификации. Производство формальдегида по этой схеме работает по замкнутому циклу и в нем отсутствуют отходы, сточные воды и вредные газовые выбросы.
3.АВТОМАТИЗАЦИЯ ПРОЦЕССА ПРОИЗВОДСТВА ФОРМАЛЬДЕГИДА ОКИСЛИТЕЛЬНЫМ ДЕГИДРИРОВАНИЕМ МЕТАНОЛА.
В технологический режим процесса производства формальдегида окислительным дегидрированием метанола для контроля основных параметров процесса, необходимо использовать различные датчики такие как давления, температуры, расхода, мощности и т.д. На каждом входе и выходе колонны должны стоять расходомеры, измеряющие расход входящих и выходящих потоков. Расходомеры регулируют величину расхода, относительно заданной, подавая сигнал задвижке, которая регулирует поток. Также вверху каждой колонны расположены манометры для того, чтобы следить за давлением внутри колонны, которое не должно отходить от нормы. Вверху и
внизу каждой колонны расположены термометры, они нужны для поддержания оптимальной температуры в колоннах.
4.ПРОИЗВОДСТВО ФОРМАЛЬДЕГИДА
Окислительное дегидрирование метанола представляет гетерогенно-каталитический процесс, протекающий в газовой фазе на твердом катализаторе. В этом процессе совмещены экзотермическая реакция окисления метанола:
СНзОН + 0,5 O2 = НСНО + Н2O - ?Н1 , ?Н1 = - 156,ЗкДж (д)
и эндотермическая реакция его дегидрирования:
СНзОН - НСНО + Н2 - ?Н2 , ?Н2 = 85,3 кДж (е)
При соотношении реакций (д) и (е) равным 0,55:0,45 тепловой эффект процесса достаточен для возмещения потерь тепла системы в окружающую среду и для нагревания исходных продуктов до нужной температуры. Если это отношение соблюдается, а в исходной паровоздушной смеси содержится около 45% об. метанола, что лежит за верхним пределом взрываемости ее (34,7%), процесс можно проводить в реакторах адиабатического типа, не имеющих поверхностей теплообмена.
В качестве катализаторов процесса окислительного дегидрирования используют медь (в виде сетки или стружки) и серебро, нанесенное на пемзу. Одновременно с основными реакциями (д, е) протекают побочные реакции глубокого окисления (в, г), а также реакции дегидрирования и гидрирования, приводящие к образованию смеси продуктов: СН 3ОН > НСНО >СО; СН3ОН + Н2 > СН4 + Н2O
5. ПРОИЗВОДСТВО ФОРМАЛЬДЕГИДА ОКИСЛЕНИЕМ МЕТАНОЛА
В этом методе, метанол окисляется в избытке воздуха при температуре 350--430°С и атмосферном давлении на окисном железо-молибденовом катализаторе состава Мо3•Fе 2(МоO4)з. Этот катализатор имеет высокую активность и малочувствителен к каталитическим ядам.
Технологический процесс прямого окисления отличается от ранее описанного процесса окислительного дегидрирования высокой степенью конверсии метанола (0,99), селективностью по формальдегиду, достигающей 96% и высокой экзотермичностью. Поэтому для окисления метанола в нем используют трубчатые реакторы с интенсивным охлаждением циркулирующей в межтрубном пространстве водой или другими хладоагентами. К достоинствам метода относятся также низкие расходные коэффициенты по сырью и энергии.
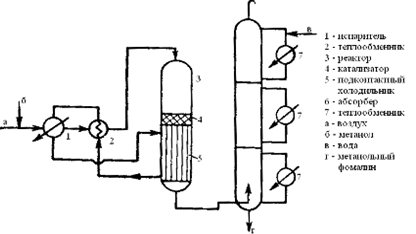
технологическая схема производства формальдегида окислительной конверсией метанола на серебряном катализаторе.
На схеме производства формальдегида на катализаторе серебро, на носителе метанол, содержащий 20-25% воды, поступает в испаритель 1, где испаряется в токе воздуха. Паровоздушная смесь перегревается до 1100С в теплообменнике 2 и подается в верхнюю часть реактора 3. При пуске системы слой катализатора в реакторе разогревается до 250-3000С с помощью специальных электроподогревателей, а после «зажигания» слоя (для контроля за этим явлением в некоторых реакторах установлено смотровое окошко) температура катализатора поддерживается на заданном уровне за счет тепла реакции. Пройдя с высокой скоростью через слой катализатора, реакционная смесь охлаждается в подконтактном холодильнике 5, выполненном как одно целое с реактором. Далее газообразные продукты реакции поступают в абсорбер 6, где из них извлекают формальдегид и непрореагировавший метанол. Абсорбер, представляющий собой тарельчатую колонну, разделён на три секции. Нижняя секция орошается формалином, средняя - раствором, содержащим 15-20% формальдегида, а верхняя - чистой водой. Из низа абсорбера выходит товарный формалин. В случае необходимости формалин подвергают обезметаноливанию.
6. ПРИМЕНЕНИЕ ФОРМАЛЬДЕГИДА
Производство полимеризационных материалов и поликонденсационных продуктов бесспорно является наиболее важным направлением использования формальдегида. Получают следующие материалы: мочевиноформальдегидные смолы и концентрат, фенолоформальдегидные смолы, полиформальдегид (полиацетальные смолы), меламинные смолы, пентаэритрит, уротропин (гексамин), этиленгликоль, 1,4-бутандиол, 4,4-дифенилметаидиизоцианат (MDI).
При получении этих материалов формальдегид может применяться либо непосредственно в виде мономера (сополимера), либо в качестве сырья для синтеза полимеризующего продукта. Значительная часть формальдегида используется и непосредственно, в виде водно-метанольного раствора или низкомолекулярного полимера (параформ), в качестве консерванта, дубителя, инсектицида и т.п. формальдегид окисление метан кислород
Традиционно одним из наиболее массовых потребителей формальдегида является производство пластических масс и смол. Различают следующие типы этих материалов на основе формальдегида: фенолоформальдегидные (продукт конденсации с фенолом); аминоформальдегидные (конденсация с карбамидом или меламином); полиформальдегид и т.д.
С учетом назначения выпускаемого изделия широко практикуется введение в рецептуру небольших добавок различных реагентов
, придающих основному продукту те или иные эксплуатационные свойства - спиртов, кислот, эфиров, аминов и т.д. Поэтому подлинный механизм образования многих материалов весьма сложен и не всегда полностью изучен. Специфичны и многообразны также технология и аппаратурное оформление синтеза полимерных смол и пластмасс, в связи с чем это производство, по существу, выделяется в самостоятельную отрасль промышленности.
ВЫВОД
В ходе учебной практики было рассмотрено производство формальдегида окисленным дегидрированием метанола. Описаны свойства формальдегида, его влияние на человека и окружающую среду, основные физико-химические и технологические свойства формальдегида, положенные в основу получения формальдегида, тип процесса и вариант технологического режима.
Приведена и описана технологическая схема получения формальдегида окисленным дегидрированием метанола.
СПИСОК ЛИТЕРАТУРЫ
1. Лебедев Н.Н. , Монаков М.Н., Швец В.Ф. Теория технологических процессов основного органического и нефтехимического синтезов. - М.: Химия, 1984.
2. Мухленов И.П. и др. Общая химическая технология (часть 1, Теоретические основы химической технологии). - М.: «Высшая школа», 1984.
3. Мухленов И.П. и др. Общая химическая технология (часть 2, Важнейшие химические производства), - М.: «Высшая школа», 1984.
4. Юкельсон И.И. Технология основного органического синтеза. - М.: Химия, 1968.

