ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 26.04.2024
Просмотров: 28
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
1.Основные свойства ферментов. Примеры.
Зависимость активности ферментов от температуры. Температура может влиять по-разному на активность фермента. При высоких значениях температуры может происходить денатурация белковой части фермента, что негативно сказывается на его активности. При определенных (оптимальных) значениях температура может влиять на скорость образования фермент-субстратного комплекса, вызывая увеличение скорости реакции. Температура, при которой каталитическая активность фермента максимальна, называется температурным оптимумом фермента. Различные клеточные ферменты имеют собственные температурные оптимумы, которые определяются экспериментально. Для ферментов животного происхождения температурный оптимум находится в интервале 40 - 50°С
Зависимость активности фермента от рН-среды.Большинство ферментов проявляет максимальную активность при значениях рН, близких к нейтральным. Лишь отдельные ферменты "работают" в сильно кислой или сильно щелочной среде. Например, активность пепсина - фермента, гидролизующего белки в желудке, - максимальна при рН 1,5 - 2,5. В щелочной среде "работают" ферменты, локализованные в кишечнике. Изменение оптимального для данного фермента значения рН-среды может привести к изменению третичной стурктуры фермента, что скажется на его активности. С другой стороны, при изменении рН может измениться ионизация субстрата,что повлияет на образование фермент-субстратного комплекса.
Специфичность действия ферментов -одно из главных их свойств. Специфичность- это избирательность фермента по отношению к субстрату (или субстратам). Специфичность действия ферментов объясняется тем, что субстрат должен подходить к активному центру как "ключ к замку". Это образное сравнение сделано Э.Фишером в 1894 г. Он рассматривал фермент как жесткую структуру, активный центр которой представляет собой "слепок" субстрата. Однако этой гипотезой трудно объяснить групповую специфичность ферментов, т.к. конфигурация "ключей" (субстратов), подходящих к одному "замку", слишком разнообразна. Такое несоответствие получило объяснение в 50-е гг. XX в. в гипотезе Д. Кошланда. Она получила название гипотезы "вынужденного соответствия".
По гипотезе Д. Кошланда, молекула фермента не жесткая, а гибкая, эластичная, поэтому информация фермента и его активного центра может изменяться при присоединении субстрата или других лигандов. В момент присоединения (рис. 10) субстрат "вынуждает" активный центр фермента принять соответствующую форму. Это можно сравнить с "перчаткой" и "рукой".
Гипотеза "вынужденного соответствия" получила экспериментальное подтверждение. Эта гипотеза позволяет также объяснить причину превращения близких аналогов субстратов.
Различают несколько видов специфичности.
-
Стереохимическая субстратная специфичность-фермент катализирует превращение только одного стереоизомера субстрата. Например, фумаратгидратаза катализирует присоединение молекулы воды к кратной связи фумаровой кислоты, но не к ее стереоизомеру - малеиновой кислоте. -
Абсолютная субстратная специфичность-фермент катализирует превращение только одного субстрата. Например, уреаза катализирует гидролиз только мочевины. -
Групповая субстратная специфичность-фермент катализирует превращение группы субстратов сходной химической структуры. Например, алкогольдегидрогеназа катализирует превращение этанола и других алифатических спиртов, но с разной скоростью.
Влияние на активность ферментов активаторов и ингибиторов.К числу факторов, повышающих активность ферментов, относятся катионы металлов и некоторые анионы. Чаще всего активаторами ферментов являются катионы Mg2+, Mn2+, Zn2+, K+ и Со2+, а из анионов - Сl-. Катионы действуют на ферменты по-разному. В одних случаях они облегчают образование фермент-субстратного комплекса, в других - способствуют присоединению кофермента к апоферменту, либо присоединяются к аллостерическому центру фермента и изменяют его третичную структуру, в результате чего субстратный и каталитический центры приобретают наиболее выгодную для осуществления катализа конфигурацию.
2.Дайте определение изоформентам. Диагностическое значение определения активности изоферментов.
Изоферменты, или изоэнзимы — это различные по аминокислотной последовательности изоформы или изотипы одного и того же фермента, существующие в одном организме, но, как правило, в разных его клетках, тканях или органах.Они катализируют одну и ту же реакцию, но отличаются по некоторым функциональным свойствам в силу отличий по:
- аминокислотному составу;
- электрофоретической подвижности;
- молекулярной массе;
- кинетике ферментативных реакций;
- способу регуляции;
- стабильности и др.
Примеры изоферментов: глюкокиназа и гексокиназа.
Изучение появления изоферментов ферментов в сыворотке крови может представлять интерес в диагностике органических и функциональных поражений органов и тканей. По изменению содержания изоферментов в сыворотке крови можно судить как о топографии патологического процесса, так и о степени поражения органа или ткани.
3 Строение ферментов. Каталитический, адсорбционный и аллостерический центры. Механизм действия ферментов.
Благодаря ферментам биохимические реакции протекают с огромной скоростью. Скорость ферментативных реакций в десятки тысяч раз (а иногда и в миллионы) выше скорости реакций, идущих с участием неорганических катализаторов. Вещество, на которое оказывает свое действие фермент, называют субстратом.
Ферменты — глобулярные белки, по особенностям строения ферменты можно разделить на две группы: простые и сложные.Простые ферменты являются простыми белками, т.е. состоят только из аминокислот. Сложные ферменты являются сложными белками, т.е. в их состав помимо белковой части входит группа небелковой природы — кофактор. У некоторых ферментов в качестве кофакторов выступают витамины. В молекуле фермента выделяют особую часть, называемую активным центром.Активный центр — небольшой участок фермента (от трех до двенадцати аминокислотных остатков), где и происходит связывание субстрата или субстратов с образованием фермент-субстратного комплекса. По завершении реакции фермент-субстратный комплекс распадается на фермент и продукт (продукты) реакции. Некоторые ферменты имеют (кроме активного) аллостерические центры — участки, к которым присоединяются регуляторы скорости работы фермента (аллостерические ферменты).
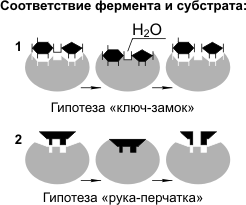
Для реакций ферментативного катализа характерны: 1) высокая эффективность, 2) строгая избирательность и направленность действия, 3) субстратная специфичность, 4) тонкая и точная регуляция. Субстратную и реакционную специфичность реакций ферментативного катализа объясняют гипотезы Э. Фишера (1890 г.) и Д. Кошланда (1959 г.).
Э. Фишер (гипотеза «ключ-замок») предположил, что пространственные конфигурации активного центра фермента и субстрата должны точно соответствовать друг другу. Субстрат сравнивается с «ключом», фермент — с «замком».
Д. Кошланд (гипотеза «рука-перчатка») предположил, что пространственное соответствие структуры субстрата и активного центра фермента создается лишь в момент их взаимодействия друг с другом. Эту гипотезу еще называют гипотезой индуцированного соответствия.
В составе как простого, так и сложного фермента, выделяют субстратный, аллостерический и каталитический центры.
Каталитический центрпростого фермента представляет собой уникальное сочетание нескольких аминокислотных остатков, расположенных на разных участках полипептидной цепи. Образование
47
каталитического центра происходит одновременно с формированием третичной структуры белковой молекулы фермента. Чаще всего в состав каталитического центра простого фермента входят остатки серина, цистеина, тирозина, гистидина, аргинина, аспарагиновой и глутаминовой кислот.
Субстратный центрпростого фермента - это участок белковой молекулы фермента, который отвечает за связывание субстрата. Субстратный центр образно называют "якорной площадкой", где субстрат прикрепляется к ферменту за счет различных взаимодействий между определенными боковыми радикалами аминокислотных остатков и соответствующими группами молекулы субстрата. Субстрат с ферментом связывается посредством ионных взаимодействий, водородных связей; иногда субстрат и фермент связываются ковалентно. Гидрофобные взаимодействия также играют определенную роль при связывании субстрата с ферментом. В простых ферментах субстратный центр может совпадать с каталитическим; тогда говорят об активном центрефермента. Так, активный центр амилазы - фермента, гидролизующего α-1,4-гликозидные связи в молекуле крахмала - представлен остатками гистидина, аспарагиновой кислоты и тирозина; ацетилхолинэстеразы, гидролизующей сложноэфирные связи в молекуле ацетилхолина, остатками гистидина, серина, тирозина и глутаминовой кислоты. В активном центре карбоксипептидазы А, гидролизующей определенные пептидные связи в молекуле белка, локализованы остатки аргинина, тирозина и глутаминовой кислоты.
Аллостерический центрпредставляет собой участок молекулы фермента, в результате присоединения к которому какого-то низкомолекулярного вещества изменяется третичная структура белковой молекулы фермента, что влечет за собой изменение его активности. Аллостерический центр является регуляторным центром фермента.
В сложных ферментах роль каталитического центра выполняет кофермент, который связывается с апоферментом в определенном участке - кофермент связывающем домене. Понятия субстратного и аллостерического центров для сложного фермента и для простого аналогичны.
Мультимолекулярные ферментные системы. Их роль . Примеры

5.Физический смысл константыМихаэлиса
Основной физический смысл константы Михаэлиса - в определении скорости биохимической (ферментативной) реакции (сродство фермента к субстракту) .
Эта зависимость снижается при повышении кислотности среды и температуры. Оптимум рН для большинства ферментов находится между 5,0 и 9,0.
Скорость превращения субстрата с образованием продукта Р пропорциональна концентрации фермент-субстратного комплекса [ES]. При малых концентрациях субстрата в растворе имеется некоторое число свободных молекул фермента Е, не связанных в комплекс ES. Поэтому при увеличении концентрации субстрата концентрация комплексов растет, следовательно, растет и скорость образования продукта. При больших концентрациях субстрата все молекулы фермента связаны в комплекс ES (явление насыщения фермента) , поэтому дальнейшее повышение концентрации субстрата практически не увеличивает концентрацию комплексов и скорость образования продукта остается постоянной.
Таким образом, становится ясен физический смысл максимальной скорости ферментативной реакции. Vmax - это скорость, с которой реагирует фермент, полностью существующий в виде фермент-субстратного комплекса.
Константа Михаэлиса численно соответствует такой концентрации субстрата, при которой стационарная скорость равна половине максимальной.
Данная константа характеризует константу диссоциации фермент-субстратного комплекса:


