ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 28.04.2024
Просмотров: 42
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Нақшаи кор:
-
Маҳлулҳои коллоидӣ ва хусусиятҳои умумии маҳлулҳои он ........... 2 -
Суспенсоидҳо – маҳлулҳои коллоидӣ .................................................. 3 -
Коллоидҳои молекулавӣ, сафедаҳо ...................................................... 4 -
Маҳлулҳои коллоидӣ бо усулҳои тавсифшуда ................................... 6 -
Сохтори заррачаҳои коллоидӣ .............................................................. 7
Маҳлулҳои коллоидӣ
Хусусиятҳои умумии маҳлулҳои коллоидӣ ва усулҳои тайёр кардани онҳо.
Агар ягон фаза ба суфтакунӣ (дисперссия) дучор шуда, дар фазаи дигар баробар тақсим карда шавад, он гоҳ системаи ҳосилшуда дисперс номида мешавад; фазае, ки ба дисперсия дучор мешавад, фазаи дисперси (ФП) ва фазае, ки дар он DP таксим мешавад, мухити дисперси (ДС) номида мешавад.
Аз рӯи андозаи зарраҳои DF, системаҳои пароканда ба ду намуд тақсим мешаванд:
1. Системаҳои дағалона пароканда. Диаметри заррачахои ДФ аз 10—5 см (100 нм) зиёд аст. Аз рӯи ҳолати ҷамъшавии ДФ системаҳои дағал пароканда ба суспензияҳо (ДФ сахт) ва эмульсияҳо (моеъи ДФ) тақсим мешаванд. Мисоли суспензия гили дар об омехташуда, мисоли эмульсия шир мебошад. Системаҳои дағал пароканда ноустувор буда, ҳангоми истодан худ ба DF ва DS ҷудо мешаванд.
2. Системаҳои майда пароканда (микрогетерогенӣ) ё маҳлулҳои коллоидӣ. Маҳлулҳои коллоидӣ дар байни системаҳои дағал ва маҳлулҳои ҳақиқӣ мавқеи фосилавиро ишғол мекунанд, ки дар он моддаҳои ҳалшуда ба молекулаҳо ва ионҳо тақсим мешаванд ва фазаи инфиродӣ ташкил намедиҳанд. Ҷудошавии маҳлулҳои коллоидӣ ба синфи алоҳидаи объектҳои химиявӣ бо ду сабаб вобаста аст:
а). маҳлулҳои коллоидӣ бо майдони хеле калони мушаххаси фазаи пароканда тавсиф карда мешаванд
ки дар он S - сатҳи зарраҳо, V ҳаҷми онҳо; Ҳамин тариқ, сатҳи 1 см3 зарраҳои диаметрашон 10-6 см 600 м2 аст.
б). дар системаҳои микрогетерогенӣ қисми зиёди зарраҳои молекулавӣ ё атомии модда дар интерфейс ҷойгир буда, дорои энергияи зиёдатии сатҳ аст; Равшан аст, ки дар натичаи ин хосиятхои модда дар чукурии фаза ва сатхи он як хел нахоханд буд.
Дар хакикат, дар системахои коллоидй мо бо холати принципан нави модда сару кор дорем, ки мавзуи омузиши фанни алохидаи химиявй — химияи коллоидй мебошад. Химияи коллоидӣ химияи физикии системаҳои пароканда ва падидаҳои рӯизаминӣ мебошад.
Микрогетерогенные системы могут быть классифицированы по ряду признаков.
Аз руи холати агрегацияи фазахои дисперси ва мухити дисперси. Дар ин асос 9 синфҳои системаҳои дисперсиро ҷудо кардан мумкин аст:
| Класс | ДФ/ДС | Система |
| 1 | Т/Ж | Коллоидные растворы твердых веществ (золи) |
| 2 | Ж/Ж | Эмульсии |
| 3 | Г/Ж | Пены |
| 4 | Т/Т | Сплавы, стекла, минералы |
| 5 | Ж/Т | Студни (гели), капиллярные системы |
| 6 | Г/Т | Минералы, пористые системы |
| 7 | Т/Г | Аэрозоли |
| 8 | Ж/Г | Аэрозоли |
| 9 | Г/Г | Флуктуации плотности разряженных газов |
Аз руи кувваи таъсири мутакобилаи заррахои фазаи дисперсй. Фарқ кардан
а) системаҳои озод пароканда (солҳо), ки заррањои онњо бо ҳамдигар суст амал мекунанд;
б) системаҳои дисперсии бо ҳам алоқаманд (гелҳо), ки зарраҳои онҳо бо ҳамдигар сахт таъсир мекунанд.
Аз руи табиати хиссачахои фазаи дисперсй. Дар робита ба ин, се гурӯҳи маҳлулҳои коллоидӣ мавҷуданд.
Суспенсоидҳо – маҳлулҳои коллоидӣ, ки дар онњо фазаи дисперсӣ торчаи булурии худро нигоњ медорад. Зарраҳои коллоидӣ дар ин ҳолат хурдтарин кристаллҳои DF мебошанд. Суспенсоидҳо моддаҳоеро ташкил медиҳанд, ки дар ҳалкунандаи додашуда ҳал намешаванд. Ба ин махлулхои коллоидии металлхо, оксидхо, гидроксидхои кам халшаванда ва намакхо мисол шуда метавонанд. Суспенсоидҳо одатан чандон устувор нестанд ва метавонанд дар шароити тағйирёбанда вайрон шаванд. Онҳо худ аз худ ба вуҷуд намеоянд. Зарраҳои суспенсоид аз филтрҳои коғазӣ мегузаранд, аммо дар мембранаҳои нимгузаранда нигоҳ дошта мешаванд. Консентратсияи максималии суспенсоидҳо хурд мебошанд (ба миқдори 0,1 ват.%); заррачахои фазаи дисперсй нисбат ба мухити дисперси гайрифаъол буда, суст гидрат мешаванд.
Коллоидҳои ассотсиативӣ ё мицеллярӣ, ки аз моддаҳои сатҳи фаъол (сурфактҳо) ба вуҷуд меоянд. Сурфактантҳо моддаҳое мебошанд, ки метавонанд дар интерфейс ҷамъ шуда, шиддати сатҳро паст кунанд. Молекулаҳои чунин моддаҳо дорои гурӯҳи функсионалии ба осонӣ гидратшаванда (гидрофилӣ) ва радикали дарозмуддати гидратнашаванда (гидрофобӣ) мебошанд. Намунаи сурфактант намакҳои натрий ё калийи кислотаҳои карбоксилии олӣ (собунҳо), ки гурӯҳи гидрофилии онҳо гурӯҳи карбоксил мебошад (расми 68, а). Ҳангоми дар об ҳал шудани ионҳои кислотаҳои карбон майл доранд, ки радикалҳои карбогидридҳоро «пинҳон» намуда, ассотсиатсияҳо (микеллаҳо) ба вуҷуд меоранд, ки дар онҳо гурӯҳҳои гидрофобӣ дар дохили зарра ва гидрофобӣ ба берун нигаронида шудаанд. Чунин ассотсиатсияҳо метавонанд ду намуд бошанд: мицеллаҳои глобулярӣ (расми 68б) ва мицеллаҳои ламелӣ (расми 68в). Маҳлулҳои коллоидҳои миселлярӣ метавонанд ба таври худкор ба вуҷуд оянд. Устувории онҳо нисбат ба суспенсоидҳо хеле баландтар аст.
б) в)
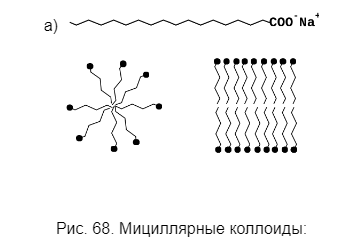
а) молекулаи сурфактант аст;
б) митселли глобулярӣ;
в) мицеллаҳои пластикӣ
Коллоидҳои молекулавӣ, ки маҳлулҳои пайвастагиҳои макромолекулярӣ (сафедаҳо, полимерҳо) мебошанд, ки молекулаҳои онҳо андозаи зарраҳои коллоидӣ доранд. Дар асл, ин гуна маҳлулҳо дурустанд, аммо аз рӯи андозаи зарраҳо, онҳо хосиятҳои маҳлулҳои коллоидиро доранд. Маҳлулҳои пайвастагиҳои макромолекулярӣ устувории номаҳдуд доранд. Агар аз чунин маҳлул ҳалкунанда хориҷ карда шавад, он гоҳ пайвастагии баландмолекулярии ҷудошударо бо илова кардани ҳалкунанда боз ба ҳолати маҳлули коллоидӣ интиқол додан мумкин аст. Аз ин рӯ, коллоидҳои молекулавӣ баръакс номида мешаванд.
Маҳлулҳои коллоидӣ баъзе хосиятҳои хос доранд. Ҳамин тариқ, хосияти хоси маҳлулҳои коллоидӣ қобилияти пароканда кардани нур мебошад. Андозаи заррачаҳои коллоидӣ ба дарозии мавҷи нури намоён наздиканд, бинобар ин ҳангоми гузаштан аз маҳлули коллоидӣ нур пароканда мешавад. Дар натиља мушоњида ба мањлул ба самти перпендикуляр ба шуоъњои рўшноӣ нигариста, конуси равшанро мебинад (эффекти Фарадей-Тиндал). Шиддати паҳншавии рӯшноӣ ба қувваи чоруми дарозии мавҷҳо баръакс мутаносиб аст
Аз ин сабаб, системаҳои коллоидӣ нурҳои қисми кабуди спектрро ва аз ҳама камтар - сурхро сахт пароканда мекунанд. Аз ин сабаб, конуси Тиндалл кабуд аст.
Андозаи хурди заррачаҳои коллоидӣ инчунин ба он вобаста аст, ки онҳо дар ҳаракати доимии бесарусомонӣ (ҳаракати Браунӣ) мебошанд: дар ҳар лаҳзаи вақт натиҷаи бархӯрди заррачаҳои коллоидӣ бо молекулаҳои ҳалкунанда ба сифр баробар нест. ки зарра бо рохи шикаста харакат мекунад.
Азбаски маҳлулҳои коллоидӣ дар байни системаҳои дағал пароканда ва маҳлулҳои ҳақиқӣ мавқеи фосилавӣ доранд, онҳоро бо ду роҳ ба даст овардан мумкин аст: ё тавассути суфта кардани зарраҳои DF ба андозаи зарраҳои коллоидӣ (усулҳои дисперсия) ё бо роҳи муттаҳид кардани атомҳо, ионҳо ва молекулаҳои алоҳида ба заррачаи коллоидӣ (усулҳои конденсатсия). Бо усули дисперсий махлули коллоидиро ба даст оварда, моддаеро, ки одатан дар шакли суспензия гирифта мешавад, ё ба таври механики бо истифода аз осиёбхои ба ном коллоид, ё бо таъсири УЗИ майда карда мешавад. Усулҳои конденсатсионӣ бештар гуногунанд. Байни конденсатсияи физикӣ ва химиявӣ фарқ кунед. Дар ҳолати конденсатсияи физикӣ гузариши фазавӣ барои ба даст овардани маҳлули коллоидӣ истифода мешавад. Ҳамин тавр, масалан, маҳлули коллоидии натрийро дар бензол тавассути зуд хунук кардани омехтаи буғҳои натрий ва бензол ба даст овардан мумкин аст (усули конденсатсияи буғ). Маҳлули коллоидии сулфурро бо усули ивазкунандаи ҳалкунанда ба даст овардан мумкин аст: маҳлули тофтаи сулфур дар этанол, ки маҳлули ҳақиқӣ аст, ба миқдори зиёди об, ки сулфур ҳал намешавад ва ба ҳолати коллоидӣ мегузарад, ворид карда мешавад. Барои ба даст овардани маҳлулҳои коллоидӣ бо усулҳои конденсатии химиявӣ реаксияҳои гуногуни пайдоиши пайвастагиҳои суст ҳалшаванда истифода мешаванд. Барои ба вучуд овардани мањлули коллоидї, на боришот, реаксияро дар мањлулњои хеле мањлул гузаронида, яке аз реактивњоро аз њад зиёд гирифта мегиранд. Ҳамин тариқ, маҳлули коллоидии сулфати барийро тавассути илова кардани миқдори ками маҳлули хлориди барий ба маҳлули 0,001М сулфати натрий ба даст овардан мумкин аст. Маҳлули коллоидии сулфур тавассути реаксияи маҳлулҳои моеъи тиосульфати натрий ва кислотаи сулфат мувофиқи муодила ба даст оварда мешавад.
Na2S2O3 + H2SO4 = Na2SO4 + SO2 + S + H2O
золь
Барои ба даст овардани маҳлули коллоидии гидроксиди оҳан (III) реаксияи гидролизӣ истифода мешавад: маҳлули FeCl3 -ро ба оби ҷӯшон қатра-қатра илова мекунанд; мувофиқи муодила ташкил карда шудааст
FeCl3 + 3H2O = Fe(OH)3 + 3HCl
золь
гидроксиди оҳан (III) боришот наборад, балки ба ҳолати коллоидӣ мегузарад.
Дар вакти ба даст овардани махлулхои коллоидии металлхо бештар усули камони электрики истифода мешавад, ки хусусиятхои усулхои дисперси ва конденсатиро ба хам мепайвандад. Масалан, барои ба даст овардани мањлули коллоидии тилло электродњои тиллоиро ба мањлули хеле мањлули карбонати натрий ё гидроксид меандозанд ва ба онњо фарќияти потенсиалие, ки барои ба амал овардани камони электр кифоя аст, меандозанд. Дар ҳарорати камони барқ металли электродҳо бухор шуда, ба ҳолати атомӣ табдил меёбад; буғҳои металлӣ, ки дар маҳлул зуд хунук мешаванд, конденсатсия шуда, зарраҳои коллоидиро ташкил медиҳанд.
Маҳлулҳои коллоидӣ, ки бо усулҳои тавсифшуда ба даст оварда мешаванд, одатан дорои ифлосиҳои ҳалшаванда мебошанд. Якчанд усулҳо барои тоза кардани ифлосиҳои пасти молекулавӣ истифода мешаванд. Усули асосии диализ ба истифодаи мембранаҳое асос ёфтааст, ки аз молекулаҳо ва ионҳо гузаранда, вале аз зарраҳои коллоидӣ гузаранда нестанд. Зарферо, ки девораш нимногузар аст, бо махлули коллоидй пур карда, ба оби равон меандозанд; Аз сабаби ба об паҳн шудани ифлосиҳои каммолекулярӣ ҳал тадриҷан аз ин ифлосиҳо озод мешавад. Агар диализ дар майдони электрики (электродиализ) гузаронида шавад, тозакунии золҳоро аз ифлосиҳои ионӣ суръат бахшидан мумкин аст. Усули дигари тоза кардани маҳлулҳои коллоидӣ ультрафилтратсия аст: филтр кардани ҳали зери фишор тавассути филтрҳои сахти маҳлул.
Сохтори заррачаҳои коллоидӣ.
Сохтори заррачаи коллоидии суспенсоидро бо мисоли маҳлули коллоидии сулфати барий, ки бо усули конденсатсияи химиявӣ ҳангоми таъсири мутақобилаи хлориди барий бо сулфати натрий зиёд гирифта шудааст, дида мебароем:
BaCl2 + Na2SO4 = BaSO4 + 2NaCl
зиёда аз сол
Ҳангоми таъсири мутақобилаи реактивҳо ионҳои Ba2+ ва SO хурдтарин кристаллҳои сулфати барийро (агрегатҳо) ташкил медиҳанд. Агар консентратсияи реактивҳо баланд бошад, ин агрегатҳо зуд афзоиш ёфта, боришот мешаванд. Аммо дар консентратсияи паст ва дар мављудияти зиёдатии яке аз реактивњо дар система равандњои адсорбсионї ба вуљуд омада, аз калон шудани кристаллњо монеъ мешаванд. Адсорбсия раванди стихиявии зиёдшавии консентратсияи заррачаҳо дар интерфейс мебошад. Агрегатхои хосилшуда аз
махлул ионхои муайянро адсорб мекунанд; бо истифода аз коидаи Фаянс-Панетт муайян кардан мумкин аст, ки кадоме аз ионхо дар сатхи агрегат концентрация мешаванд: дар сатхи чисмхои сахт ионхое мебошанд, ки ба торчаи булурии он дохил мешаванд ё дар ин торхо ягон ионро иваз карда метавонанд. аввал адсорб карда мешавад. Ин ионҳоро ионҳои муайянкунандаи потенсиал меноманд. Дар ҳолати баррасишаванда, маҳлул дорои ионҳои натрий ва ионҳои сулфатӣ мебошанд, ки ҳангоми диссоциатсияи сулфати натрий ба вуҷуд меоянд.
Na2SO4 = 2Na+ + SO
Аён аст, ки ионҳои сульфат дар рӯи агрегатҳо адсорб мешаванд. Агрегатсия бо ионҳои потенсиали муайянкунандаи адсорбшуда ядрои заррачаи коллоидиро ташкил медиҳад
[│BaSO4│m∙nSO ]
ки дар он шумораи воњидњои формула дар маљмўъ (m) арзиши чанд њазорро ифода мекунад ва n<
Ядрои дорои заряди манфӣ аз маҳлул ионҳои аломати муқобилро, ки контрионҳо меноманд, ҷалб мекунад. Дар мавриди баррасишаванда катионхои натрий хамчун контрионхо амал мекунанд. Концентрацияи контрионхо дар наздикии сатхи ядро, аз як тараф, бо кам шудани энергияи система, ки ба процесси концентрацияи контрионхо мусоидат мекунад ва аз тарафи дигар, бо афзоиши энтропияи системае, ки ба ин процесс маъкул нест. Дар натиља 2n катионњои натрий, ки барои љуброни заряди ядро заруранд, ду ќабати контрионњоро ташкил медињанд: ќабати адсорбсионї, ки бо сатњи сахт пайваст аст ва қабати диффузї, ки муќобили ионњояшон њаракатнокии муайян доранд ва сахт нестанд. ба ядро пайваст. Контрионҳои қабатҳои адсорбсия ва диффузӣ дар ҳолати мувозинати динамикӣ қарор доранд. Дар шароити тагйирёбанда ионхо метавонанд аз кабати адсорбсия ба кабати диффузи ва баръакс гузаранд. Ядро бо қабати адсорбсияи контрионҳо гранулро ташкил медиҳад, ки қисми паймоне аз заррачаи коллоидӣ мебошад. Гранул ва қабати диффузии контрионҳо зарра ё мицеллаи дурусти коллоидиро ташкил медиҳанд. Агар аз 2n ионҳои натрий 2(n-x) ба қабати адсорбсия ва 2х ба қабати диффузӣ дохил шаванд, мицелла сулфати барий чунин менамояд:
{[│BaSO4│m·nSO ]2(n-x)Na+}2x-2xNa+
│ гранул │
│ мисел │
Ҳамин тариқ, мицелла умуман аз ҷиҳати электрикӣ бетараф аст, аммо гранула заряд дорад; Махз хамин заряд ба калон шудани заррачахои коллоидй рох намедихад ва устувории зарраро таъмин мекунад. Схемаи сохтори заррачаи коллоидии сулфати барий, ки бо зиёдатии ионхои сульфат ба даст оварда шудааст, дар расм нишон дода шудааст. 69.
