ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 29.04.2024
Просмотров: 108
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
не образуются при диссоциации соединения
44. Размерность концентрации в уравнении pH = -lgC(H+)
45. Кислую реакцию среды имеет раствор
46. Молекулярному уравнению реакции
FeCl3 + 3NaOH = Fe(OH)3 + 3NaCl соответствует ионное уравнение
47. Наибольшее значение рН наблюдается в растворе
48. Если концентрация хлорид-ионов в водном растворе хлорид алюминия (AlCl3) равна 0,6 моль/л, то концентрация соли составляет ___ моль/л.
49. Концентрация ионов H+ в чистой дистиллированной воде при 200С равна ___ моль/л.
50. Для водных растворов солей Na2SO4 и Na2SiO3 верно, что
1) в обоих растворах среда щелочная
2) только во втором растворе среда щелочная
3) только во втором растворе среда кислая
4) в обоих растворах среда кислая
6. Окислительно-восстановительные
1. Коэффициент перед молекулой восстановителя в уравнении реакции
КMnO4 + Na2SO3 + H2SO4 → MnSO4 + Na2SO4 + K2SO4 + H2O равен …
2. Общая сумма коэффициентов в уравнении реакции
Mn(NO3)2 + PbO2 + HNO3 → HMnO4 + …
равна
3. Сера проявляет окислительные свойства в реакции …
а) S + Cl2 б) S + Fe в) S + HNO3 г) S + O2
4. Восстановителем в реакции H2S + SO2 S + H2O является …
а) H2O б) H2S в) SO2 г) S
5. Коэффициент перед молекулой окислителя в уравнении реакции
C + H2SO4(КОНЦ) CO2 + SO2 + H2O равен…
а) 3 б) 1 в) 4 г) 2
6. Окислителем в реакции
KMnO4 + KNO2 + H2SO4 K2SO4 + MnSO4 + KNO3 + H2O
является
а) MnSO4 б) KNO2 в) KMnO4 г) H2SO4
7. Восстановительные свойства оксида серы (IV) проявляются в реакции
а) SO2 + H2O б) SO2 + KMnO4 + H2O
в) SO2 + NaOH г) SO2 + H2S
8. Общая сумма коэффициентов в уравнении реакции
Fe + HNO3(КОНЦ) -(t0) Fe(NO3)3 + NO2 + H2O равна
а) 10 б) 14 в) 9 г) 12
9. Восстановителем в реакции H2S + O2 S + H2O является
а) H2O б) H2S в) SO2 г) S
10. Окислительные свойства оксида серы (IV) проявляются в реакции
а) SO2 + KMnO4 + H2SO4 б) SO2 + O2
в) SO2 + H2S г) SO2 + Ca(OH)2
11. Сумма коэффициентов в уравнении реакции
KOH + Cl2 KCl + KClO3 + H2O равна
а) 18 б) 12 в 10 г) 16
12. Коэффициент пред молекулой восстановителя в уравнении реакции
K2Cr2O7 + NaNO2 + H2SO4 Cr2(SO4)3 + NaNO3 + K2SO4 + H2O
а) 1 б) 6 в) 2 г) 3
13. Коэффициент перед формулой восстановителя в уравнении реакции
KNO2 + H2SO4 + KI K2SO4 + NO + I2 + H2O равен …
а) 3 б) 4 в) 1 г) 2
14. Сульфит натрия, Na2SO3, может проявлять в окислительно-восстановительных реакциях свойства
15. В реакции 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O оксид азота (1V)
1) восстанавливается
2) окисляется
3) окисляется и восстанавливается одновременно
4) не изменяет степени окисления
16. В реакции
2KMnO4 + 5Na2SO3 + 3H2SO4 = MnSO4 + K2SO4 + 5Na2SO4 + 3H2O
Na+-ионы
1) восстанавливаются
2) окисляются
3) окисляются и восстанавливаются одновременно
4) не изменяют степени окисления
17. Пероксид водорода H2O2 может проявлять в окислительно-восстановительных реакциях свойства
18. В реакции 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O ионы натрия
1) окисляются и восстанавливаются одновременно
2) окисляются
3) восстанавливаются
4) не изменяют степени окисления
19. В реакции
2KMnO4 + 5Na2SO3 + 3H2SO4 = 2MnSO4 + K2SO4 + 5Na2SO4 + 3H2O
сульфит-ионы
1) не изменяют степени окисления
2) окисляются и восстанавливаются одновременно
3) восстанавливаются
4) окисляются
20. Гидроксид хрома (III), Cr(OH)3, может проявлять в окислительно-восстановительных реакциях свойства
21. В реакции K2Cr2O7 + 3KNO2 + 4H2SO4 = Cr2(SO4)3 + 3KNO3 + 4H2O + K2SO4 окисляется ион
22. Сероводород H2S обычно проявляет в окислительно-восстановительных реакциях свойства
23. Восстановителем в реакции
Fe + HNO3(КОНЦ.)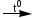 Fe(NO3)3 + NO2 + H2O является
Fe(NO3)3 + NO2 + H2O является
24. В реакции 3HgS + 2HNO3 + 6HCl = 3HgCl2 + 3S + 2NO + 4H2O
окислителем является ион
25. Коэффициент перед окислителем в уравнении реакции
H2S + HNO3(РАЗБ.) S + NO + H2O равен
26. Восстановителем в реакции S + H2SO4(КОНЦ.) SO2 + H2O
является
27. Общая сумма коэффициентов в уравнении реакции
KClO3 KCl + O
2 равна
28. Коэффициент перед восстановителем в уравнении реакции
I2 + Cl2 + H2O HIO3 + HCl равен
29. Восстановителем в реакции H2S + SO2 S + H2O является
30. Общая сумма коэффициентов в левой части уравнения реакции
Cu + H2SO4(КОНЦ.) CuSO4 + SO2 + H2O равна
31.. Гидрид кальция CaH2 может проявлять в окислительно-восстановительных реакциях свойства
а) и окислителя, и восстановителя
б) только окислителя
в) только восстановителя
г) ни окислителя, ни восстановителя
32. Окисление азота происходит в процессе, схема которого
33. Окислительно-восстановительная реакция в стандартных условиях возможна, если
а) стандартный потенциал Е0 окислителя имеет положительное значение
б) электроотрицательность окислителя выше электроотрицательности восстановителя
в) стандартный потенциал Е0 восстановителя имеет отрицательное значение
г) значение разности потенциалов полуреакций окисления и восстановления положительно
34. В реакции
K2Cr2O7 + 6KI + 7H2SO4 = Cr2(SO4)3 + 4K2SO4 + 3I2 + 7H2O
восстанавливается ион
| а) BaCl2 | б) KClO3 | в) NH4Cl | г) C6H5NH3Cl |
44. Размерность концентрации в уравнении pH = -lgC(H+)
| а) моль/л | б) % | в) г/л | г) г/мл |
45. Кислую реакцию среды имеет раствор
| а) NaNO2 | б) CH3COOK | в) K2SO4 | г) BeCl2 |
46. Молекулярному уравнению реакции
FeCl3 + 3NaOH = Fe(OH)3 + 3NaCl соответствует ионное уравнение
| а) Na+ + Cl- = NaCl | в) Fe3+ + 3OH- = Fe(OH)3 |
| б) FeCl3 = Fe3+ + 3Cl- | г) FeCl3 + 3OH- = Fe(OH)3 + 3Cl- |
47. Наибольшее значение рН наблюдается в растворе
| а) HCl | б) KOH | в) H2O | г) NaCl |
48. Если концентрация хлорид-ионов в водном растворе хлорид алюминия (AlCl3) равна 0,6 моль/л, то концентрация соли составляет ___ моль/л.
| а) 0,04 | б) 0,03 | в) 0,06 | г) 0,02 |
49. Концентрация ионов H+ в чистой дистиллированной воде при 200С равна ___ моль/л.
| 1) 10-7 | 2) 14 | 3) 10-14 | 4) 7 |
50. Для водных растворов солей Na2SO4 и Na2SiO3 верно, что
1) в обоих растворах среда щелочная
2) только во втором растворе среда щелочная
3) только во втором растворе среда кислая
4) в обоих растворах среда кислая
6. Окислительно-восстановительные
1. Коэффициент перед молекулой восстановителя в уравнении реакции
КMnO4 + Na2SO3 + H2SO4 → MnSO4 + Na2SO4 + K2SO4 + H2O равен …
| 1) 2 | 2) 1 | 3) 3 | 4) 5 |
2. Общая сумма коэффициентов в уравнении реакции
Mn(NO3)2 + PbO2 + HNO3 → HMnO4 + …
равна
| 1) 18 | 2) 20 | 3) 22 | 4) 16 |
3. Сера проявляет окислительные свойства в реакции …
а) S + Cl2 б) S + Fe в) S + HNO3 г) S + O2
4. Восстановителем в реакции H2S + SO2 S + H2O является …
а) H2O б) H2S в) SO2 г) S
5. Коэффициент перед молекулой окислителя в уравнении реакции
C + H2SO4(КОНЦ) CO2 + SO2 + H2O равен…
а) 3 б) 1 в) 4 г) 2
6. Окислителем в реакции
KMnO4 + KNO2 + H2SO4 K2SO4 + MnSO4 + KNO3 + H2O
является
а) MnSO4 б) KNO2 в) KMnO4 г) H2SO4
7. Восстановительные свойства оксида серы (IV) проявляются в реакции
а) SO2 + H2O б) SO2 + KMnO4 + H2O
в) SO2 + NaOH г) SO2 + H2S
8. Общая сумма коэффициентов в уравнении реакции
Fe + HNO3(КОНЦ) -(t0) Fe(NO3)3 + NO2 + H2O равна
а) 10 б) 14 в) 9 г) 12
9. Восстановителем в реакции H2S + O2 S + H2O является
а) H2O б) H2S в) SO2 г) S
10. Окислительные свойства оксида серы (IV) проявляются в реакции
а) SO2 + KMnO4 + H2SO4 б) SO2 + O2
в) SO2 + H2S г) SO2 + Ca(OH)2
11. Сумма коэффициентов в уравнении реакции
KOH + Cl2 KCl + KClO3 + H2O равна
а) 18 б) 12 в 10 г) 16
12. Коэффициент пред молекулой восстановителя в уравнении реакции
K2Cr2O7 + NaNO2 + H2SO4 Cr2(SO4)3 + NaNO3 + K2SO4 + H2O
а) 1 б) 6 в) 2 г) 3
13. Коэффициент перед формулой восстановителя в уравнении реакции
KNO2 + H2SO4 + KI K2SO4 + NO + I2 + H2O равен …
а) 3 б) 4 в) 1 г) 2
14. Сульфит натрия, Na2SO3, может проявлять в окислительно-восстановительных реакциях свойства
| 1) только окислителя | 3) только восстановителя |
| 2) ни окислителя, ни восстановителя | 4) и окислителя, и восстановителя |
15. В реакции 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O оксид азота (1V)
1) восстанавливается
2) окисляется
3) окисляется и восстанавливается одновременно
4) не изменяет степени окисления
16. В реакции
2KMnO4 + 5Na2SO3 + 3H2SO4 = MnSO4 + K2SO4 + 5Na2SO4 + 3H2O
Na+-ионы
1) восстанавливаются
2) окисляются
3) окисляются и восстанавливаются одновременно
4) не изменяют степени окисления
17. Пероксид водорода H2O2 может проявлять в окислительно-восстановительных реакциях свойства
| 1) только восстановителя | 3) и окислителя, и восстановителя |
| 2) только окислителя | 4) ни окислителя, ни восстановителя |
18. В реакции 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O ионы натрия
1) окисляются и восстанавливаются одновременно
2) окисляются
3) восстанавливаются
4) не изменяют степени окисления
19. В реакции
2KMnO4 + 5Na2SO3 + 3H2SO4 = 2MnSO4 + K2SO4 + 5Na2SO4 + 3H2O
сульфит-ионы
1) не изменяют степени окисления
2) окисляются и восстанавливаются одновременно
3) восстанавливаются
4) окисляются
20. Гидроксид хрома (III), Cr(OH)3, может проявлять в окислительно-восстановительных реакциях свойства
| 1) и окислителя, и восстановителя | 3) только окислителя |
| 2) ни окислителя, ни восстановителя | 4) только восстановителя |
21. В реакции K2Cr2O7 + 3KNO2 + 4H2SO4 = Cr2(SO4)3 + 3KNO3 + 4H2O + K2SO4 окисляется ион
| 1) O2- | 3) NO2- |
| 2) Cr2O72- | 4) K+ |
22. Сероводород H2S обычно проявляет в окислительно-восстановительных реакциях свойства
| а) ни окислителя, ни восстановителя | в) только окислителя |
| б) восстановителя | г) и окислителя, и восстановителя |
23. Восстановителем в реакции
Fe + HNO3(КОНЦ.)
| а) железо | в) вода |
| б) азотная кислота | г) оксид азота (IV) |
24. В реакции 3HgS + 2HNO3 + 6HCl = 3HgCl2 + 3S + 2NO + 4H2O
окислителем является ион
| а) Hg2+ | б) H+ | в) NO-3 | г) S2- |
25. Коэффициент перед окислителем в уравнении реакции
H2S + HNO3(РАЗБ.) S + NO + H2O равен
| а) 1 | б) 2 | в) 4 | г) 3 |
26. Восстановителем в реакции S + H2SO4(КОНЦ.) SO2 + H2O
является
| а) SO2 | в) H2SO4 |
| б) S | г) H2O |
27. Общая сумма коэффициентов в уравнении реакции
KClO3 KCl + O
2 равна
| а) 7 | б) 3 | в) 5 | г) 4 |
28. Коэффициент перед восстановителем в уравнении реакции
I2 + Cl2 + H2O HIO3 + HCl равен
| а) 10 | б) 6 | в) 5 | г) 1 |
29. Восстановителем в реакции H2S + SO2 S + H2O является
| а) SO2 | б) H2O | в) S | г) H2S |
30. Общая сумма коэффициентов в левой части уравнения реакции
Cu + H2SO4(КОНЦ.) CuSO4 + SO2 + H2O равна
| а) 7 | б) 4 | в) 3 | г) 6 |
31.. Гидрид кальция CaH2 может проявлять в окислительно-восстановительных реакциях свойства
а) и окислителя, и восстановителя
б) только окислителя
в) только восстановителя
г) ни окислителя, ни восстановителя
32. Окисление азота происходит в процессе, схема которого
| а) NO-2 NO | в) NO-3 NO |
| б) NH+4 N2 | г) Li3N NH3 |
33. Окислительно-восстановительная реакция в стандартных условиях возможна, если
а) стандартный потенциал Е0 окислителя имеет положительное значение
б) электроотрицательность окислителя выше электроотрицательности восстановителя
в) стандартный потенциал Е0 восстановителя имеет отрицательное значение
г) значение разности потенциалов полуреакций окисления и восстановления положительно
34. В реакции
K2Cr2O7 + 6KI + 7H2SO4 = Cr2(SO4)3 + 4K2SO4 + 3I2 + 7H2O
восстанавливается ион
| а) H+ | б) SO2-4 | в) Cr2O2-7 | г) I- |


