Добавлен: 02.05.2024
Просмотров: 46
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
По размеру (величине молекулы):
- Олигомеры (4000 - 10000);
- Низкомолекулярные вещества (10000 – 45000);
- Среднемолекулярные (45000 – 150000);
- Высокомолекулярные вещества – полимеры (150000 – 500000).
-
Влияния вспомогательных веществ на скорость растворения фармацевтических субстанций
Фармацевтическая разработка лекарственных препаратов – это неотъемлемая часть их жизненного цикла. Основная задача фармацевтической разработки заключается в создании качественного лекарственного препарата и производственного процесса, и одним из критериев качества является подбор и обоснование выбора вспомогательных веществ.
При осуществлении фармацевтической разработки с целью получения информации о высвобождении фармацевтической субстанции из твердой лекарственной формы необходимо знать скорость растворения, то есть количество фармацевтической субстанции, высвободившейся за определенный промежуток времени в жидкую среду растворения в стандартных условиях [1,8].
Наибольшее влияние на скорость растворения оказывают вспомогательные вещества в составе твердых дисперсий. Так, например, наблюдается увеличение растворимости метилурацила, нифедипина индометацина при включении их в твердую дисперсию с полиэтиленгликолем и различной молекулярной массы [6,7,11,12,13]. Возрастает как растворимость, так и скорость растворения диклофенака в воде из твердой дисперсии с полиэтиленгликолем-1500 и поливинилпирролидоном 10000.
Твердые лекарственные формы, как например, таблетки целекоксиба, содержащие в качестве антифрикционного вещества тальк (способный образовывать гидрофильный слой) имеют лучший профиль растворения по сравнению с таблетками, у которых используется магния стеарат или коллоидный диоксид кремния. Установлено также, что присутствие этих гидрофобных веществ замедляет процесс абсорбции [22].
Высокой степенью растворения и биодоступности в сочетании с и поливинилпирролидоном характеризуются следующие соединения: преднизолон, гризеофульвин, салициламид, хлорамфеникол [19].
-
Влияния вспомогательных веществ на скорость высвобождения фармацевтических субстанций
Прежде чем фармацевтическая субстанция попадет в кровь, должно произойти ее высвобождение из лекарственной формы. В процессе фармацевтической разработки в зависимости от поставленных задач лекарственная форма должна способствовать либо быстрому и полному высвобождению лекарственного препарата, либо обеспечивать пролонгацию его действия. Ряд исследований показали влияние вспомогательных веществ на изменение скорости высвобождения фармацевтической субстанции из твердых лекарственных форм.
Так, например, циклодекстрины часто применяются для увеличения биодоступности плохо растворимых в воде фармацевтических субстанций, повышают их скорость и полноту высвобождения, в том числе путем введения фармацевтической субстанции в комплексы включения [20].
Использование спиртового раствора связующего вещества в технологии получения таблеток методом влажного гранулирования увеличивает полноту и скорость высвобождения фармацевтической субстанции с неудовлетворительной растворимостью [21].
Поливинилпирролидон применяется для повышения биодоступности и ускорения процесса высвобождения фармацевтической субстанции.
Стоит отметить, что в настоящее время активно развивается такое направление получения лекарственной формы, как 2D-технология, принцип которого заключается в нанесении чернил, содержащих на специальную подложку (субстрат). Подбор субстрата совместно с составом чернил также оказывает влияние на морфологические свойства и растворимость печатаемых лекарственных форм [23]. На примере индометацина и итраконазола было показано, что скорость высвобождения фармацевтических субстанций со съедобных субстратов (различных типов рисовой бумаги) была ниже в сравнении с образцами, напечатанными на диапозитивной пленке, что наиболее заметно в случае с индометацином. Увеличенное время высвобождения со съедобных субстратов объяснялось более пористой структурой субстратов, в результате чего частицы ФС включались в матрицу субстрата.
-
Влияния вспомогательных веществ на скорость всасывания фармацевтических субстанций
Всасывание – процесс, в результате которого фармацевтическая субстанция поступает из места введения в кровеносное русло. Всасывание фармацевтической субстанции начинается сразу после его введения. В результате фармацевтической разработки вспомогательных веществ, в зависимости от своей природы и характера взаимодействия с фармацевтической субстанцией, могут оказывать различное влияние на данный параметр.
Применением поливинилпирролидона в лекарственной форме удается увеличить относительную биодоступность полимерных частиц тамоксифена после перорального применения более чем в 2 раза [2].
Установлено снижение абсорбции циметидина в присутствии гидроксипропилметилцеллюлозы и талька в составе капсул.
-
Влияния вспомогательных веществ на другие фармацевтические характеристики фармацевтических субстанций.
В результате осуществления фармацевтической разработки, помимо изменения скорости растворения, высвобождения и всасывания фармацевтических субстанций, вспомогательные вещества также могут оказывать существенное влияние на их фармацевтические показатели.
Пероксидные примеси в повидоне, выступающем в роли связующего, и кросповидоне в роли дезинтегранта, приводили к деградации структуры ралоксифена гидрохлорида (модулятор эстрогеновых рецепторов).
Пропиленгликоль ингибирует микросомальный цитохром Р450, который принимает участие в инактивации ядовитых веществ, распаде и образовании гормонов надпочечников; в обмене белков и сохранении генетической информации.
Взаимодействие лактозы, выступающей в качестве наполнителя при измельчении совместно с 4-метилфениламиноацетатом гидрохлоридом ускоряет разрушение структуры последнего [8].
Глава 2. Статистическая обработка применения вспомогательных веществ в пероральных суспензиях
2.1. Модификаторы вязкости, используемые в составах суспензий для приема внутрь
Эволюцию подходов к конструированию пероральных суспензий можно проследить по изменениям классификации вспомогательных веществ, используемых в их составе. Наиболее полно этот вопрос раскрывается в основополагающих учебных и научных изданиях, посвящённых технологии лекарственных форм. В состав суспензий, помимо действующего вещества и дисперсионной среды, в ряде случаев необходимо включать стабилизаторы агрегативной и седиментационной устойчивости, в качестве которых рекомендуется использовать электролиты и высокомолекулярные соединения, обладающие поверхностноактивными свойствами [3].
В качестве источника сведений о вспомогательных веществах, используемых в составах пероральных суспензий, представленных на фармацевтическом рынке России, использовались инструкции к лекарственным препаратам, внесённым в электронную версию Государственного реестра лекарственных средств [4], содержащие в ряде случаев также указания на количественные соотношения компонентов. Опираясь на данные сведения, были проанализированы составы 51 суспензии для приема внутрь, позволившие классифицировать и описать следующие группы вспомогательных веществ.
Модификаторы вязкости (загустители) используются для повышения стабильности дисперсной системы путем повышения вязкости дисперсионной среды в соответствии с законом Стокса [16]. В составе этой группы можно выделить вещества синтетического, полусинтетического и природного происхождения, являющиеся растительными полисахаридами. В качестве модификаторов вязкости в пероральных суспензиях в настоящее время используются глинистые минералы, камеди, производные целлюлозы, а также карбополы, высокомолекулярный макрогол и повидон (Рисунок 1).
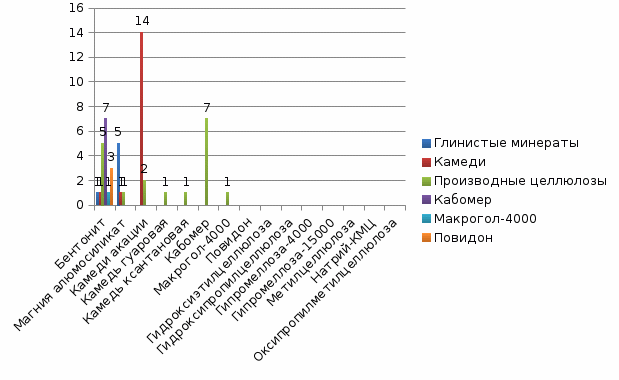
Рисунок 1. Модификаторы вязкости, используемые в составах суспензий для приёма внутрь (ГРЛС)
В 35% составов пероральных суспензий для повышения вязкости вводят производные целлюлозы, причем наиболее популярным среди них является традиционное и хорошо известное в отечественной фармацевтической практике вещество – натриевая соль карбоксиметилцеллюлозы, упоминаемая в составах под названием «кармеллоза натрия» и используемая в 13,7% изученных составов. Следующим по востребованности производным целлюлозы является гидроксиэтилцеллюлоза (гиэтеллоза, ГЭЦ), упоминаемая в 9,8% составов, гидроксипропилметилцеллюлоза (ГПМЦ) используется в 7,8% изученных суспензий, а такие производные, как метилцеллюлоза и оксипропилметилцеллюлоза востребованы как загустители пероральных суспензий в значительно меньшей степени (упоминаются примерно в 2% суспензий). Что касается используемых концентраций, то согласно представленным в инструкциях к лекарственным препаратам сведениям ГЭЦ вводится в составы суспензий для внутреннего применения в количестве 0,1–0,3%, ГПМЦ – 0,3–1,0%, а натрий-КМЦ – около 1%.
Самым популярным модификатором вязкости в суспензиях для внутреннего применения является камедь ксантановая (27,5% изученных составов), однако другие модификаторы вязкости группы камедей – гуаровая камедь и камедь акации – используются очень редко, всего в 2% составов. При этом ксантановая камедь использовалась в концентрации 0,3–0,6%, камедь акации упоминалась в составах в концентрации 1,5–6%.
Для повышения вязкости дисперсионной среды суспензий для внутреннего применения также используют глинистые минералы – магния алюмосиликат (вээгум) в концентрации 0,25–0,57% и значительно реже бентонит.
Также в составе пероральных суспензий достаточно широко применяются полимеры группы карбополов (карбомеров), например, карбомер 947P, однако их использование требует дополнительного введения в состав суспензии щелочных компонентов, чаще всего натрия гидроксида. Концентрация карбопола в рассмотренных составах суспензий находилась в диапазоне от 0,035% до 0,4%.
Повидон, представляющий собой линейный полимер 1-винил-2-пирролидона, упоминался в составах около 6% рассмотренных пероральных суспензий. Удалось обнаружить только единичное упоминание вводимого количества повидона – около 0,06%. Столь невысокая концентрация может объясняться тем, что повидон в малых концентрациях используется не столько для повышения вязкости, сколько в качестве так называемого полимерного адсорбционного стабилизатора. При этом молекулы повидона сорбируются на поверхности частиц суспендированного вещества и осуществляют стерическую стабилизацию суспензии, препятствуя слипанию частиц. Кроме того, в ряде случаев повидон может использоваться и для понижения вязкости, точнее, для улучшения текучести суспензий с большим количеством дисперсной фазы [24].
Высокомолекулярный полиэтиленоксид (макрогол 4000) используется для модификации вязкости в крайне небольшом числе (около 2%) рассмотренных составов суспензий для внутреннего применения.
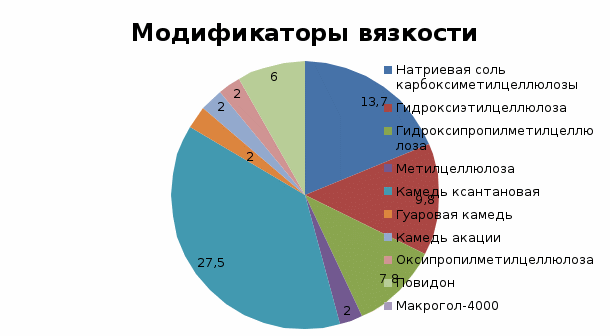
Таким образом, по частоте использования в составах пероральных суспензий можно выстроить следующий ряд модификаторов вязкости: камедь ксантановая > карбомер = натрий-КМЦ > магния алюмосиликат = ГЭЦ > повидон > ГПМЦ > прочие.
2.2. Поверхностно-активные вещества, используемые в составах суспензий для приёма внутрь
Поверхностно-активные вещества, используемые в составах суспензий, в различных источниках могут носить названия смачивающих агентов или сурфактантов [24]. В этой роли могут выступать как индивидуальные соединения, так и, реже, смеси сходных по химической природе веществ синтетического (полисорбаты, стеараты) или природного (аммония глицирризинат, лецитин) происхождения.
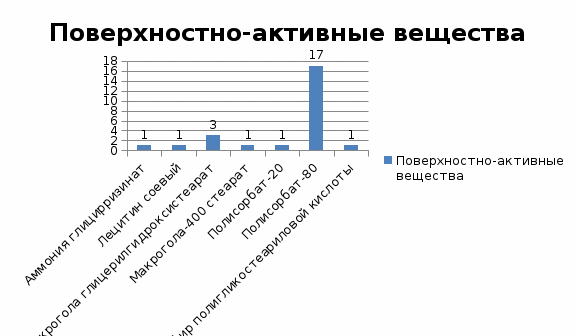
Рисунок 2. Поверхностно-активные вещества, используемые в составах суспензий для приёма внутрь (ГРЛС)
Безусловным лидером среди ПАВ, вводимых в составы суспензий для внутреннего применения, является полисорбат-80 (твин-80). Согласно проведённым исследованиям полисорбат-80 упоминался в более чем 30% рассмотренных составов. Указанные в доступных источниках используемые концентрации при этом укладывались в диапазон от 0,05% до 1%.
На втором месте по частоте использования (около 6% изученных составов) стоит производное макрогола – макрогола глицерилгидроксистеарат, также встречающийся под названием Кремофор RH40. Для стабилизации суспензии его вводили в концентрациях 0,2–1,14%.
