Файл: Решение Закон гласит количества эквивалентов вступающих в реакцию веществ равны.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.05.2024
Просмотров: 10
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
1. При восстановлении 1,17 г оксида олова водородом образовалось 0,16 г воды. Вычислите эквивалентную массу олова.
Дано: 1,17 г оксида олова, 0,16 г воды
Решение:
Закон гласит: количества эквивалентов вступающих в реакцию веществ равны.
0.16г воды — это 0.16*16/18 = 0.1422 г кислорода
Исходный оксид олова содержал 1.0278г олова и 0.1422г кислорода.
Если атомная масса 118 г/моль, то фактор экв. равен 2, и формула оксида SnO.
экв. масса кислорода = 8 г/(моль*экв)
кол-во экв. кислорода 0.1422/8 = 0.017775 моль*экв.
олова столько же, значит его экв. масса:
1.0278 / 0.017775 = 57.9 г / (моль*экв)
Ответ: 57,9 г.
2. Объясните физический смысл орбитального квантового числа. Укажите значения, которые оно может принимать и формы орбиталей, которые им соответствуют.
В квантовых состояниях с заданным значением главного квантового числа
Из выводов предыдущего параграфа следует, что стационарные волновые функции
Следовательно, в любом квантовом состоянии атом обладает определенным значением квадрата момента импульса, причем модуль орбитального момента импульса движущегося в атоме электрона однозначно определяется орбитальным квантовым числом:
| |
Проанализируем эту формулу квантования момента импульса. Сравнивая ее с условием квантования момента импульса движущегося электрона в теории Бора, можно заметить, что эти условия не совпадают. И дело не только в отличии числовых значений, рассчитанных по этим формулам. Принципиальное отличие этих соотношений состоит в том, что в квантовой механике возможны состояния атома с нулевым моментом импульса. Во всех
При классическом описании движения электрона в атоме по определенной траектории (орбите) в любом состоянии атом должен обладать ненулевым моментом импульса.
Опыт подтверждает существование квантовых состояний атома с нулевыми орбитальными моментами. Следовательно, опыт подтверждает, что только отказ от классического траекторного способа описания движения электрона в атоме позволяет правильно рассчитать и предсказать свойства атома. Вероятностный способ описания движения частиц в квантовой механике является единственно правильным способом описания свойств атомных систем - таков вывод современной физики.
Так как движущийся вокруг ядра электрон является заряженной частицей, то такое движение обуславливает протекание некоторого замкнутого тока в атоме, который можно охарактеризовать орбитальным магнитным моментом
В теории Бора, когда с позиции классической теории рассматривается круговое движение электрона по орбите радиуса
который можно охарактеризовать величиной магнитного момента
.
Связь механического и магнитного моментов при этом определяется гиромагнитным отношением
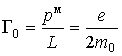 . . |
Так как заряд электрона отрицателен, то для орбитального движения направление вектора магнитного момента
Для расчета орбитального магнитного момента в квантовой теории следует определить пространственную плотность электрического тока
 |
| |
Итак, в любом квантовом состоянии атом водорода обладает не только механическим моментом
| | |
Здесь универсальная постоянная
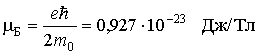
служит единицей измерения магнитных моментов атомов и называется магнетоном Бора.
Если атом переходит из одного квантового состояния в другое с испусканием (поглощением) фотона излучения, то возможны лишь такие переходы, для которых орбитальное квантовое число
Физический смысл орбитального квантового числа l заключается в том, что оно определяет значение углового момента. Дискретность l определяет дискретные значения L, т.е. величина углового момента квантуется. Для состояния с l = 0 угловой момент равен нулю.
3. Укажите тип кристаллической решетки и характер связи в кристаллах NaCl и Na. Чему равно координационное число натрия в этих решетках?
Натрий - элемент IA группы ПСХЭ Д.И. Менделеева, порядковый номер 11, имеет на внешнем энергетическом уровне 1 электрон, следовательно - типичный металл. Металлы могут образовывать всего 2 вида химической связи:
а) Металлическая связь (для металлического натрия - простого вещества);
б) Ионная химическая связь (в соединения с атомам элементов-неметаллов).
Строение кристаллических решеток обусловлено видом химической связи.
Для веществ с металлической связью образуется металлическая кристаллическая решетка (в узлах КР находятся атом-ионы натрия, а между ними располагаются делокализованные общие электроны, принадлежащие сразу всем атом-ионам - электронный газ). В случае металлического натрия кристаллическая решетка кубическая гранецентрированная.
Вещества с ионной химической связью обладают ионной кристаллической решеткой (в узлах находятся ионы Na+ и Cl-, при этом они чередуются между собой через один). Тип кристаллической решетки в этом случае кубическая.
Таким образом один атом натрия в обоих случаях координирует 8 соседних частиц. Значит, координационное число натрия равно 8.
4. Определить, на сколько градусов необходимо повысить температуру, чтобы скорость реакции увеличилась в 27 раз (температурный коэффициент (γ) равен 3).
Дано: скорость реакции увеличилась в 27 раз
(γ) = 3
Решение: По правилу Вант-Гоффа имеем
V2/V1 = гамма^ (t2-t1)/10
V2/V1 - отношение скоростей реакций при температурах t2 и t1 (по условию 27) А гамма - температурный коэффициент(по условию 3)
27= 3^(t2-t1)/10
(t2-t1)/10 = 3
t2-t1 = 30
Ответ: на 30 градусов
5. Вычислите энергию Гиббса тепловой денатурации трипсина при 50о С, если при 25оС ∆Н0реакции= 283 кДж/моль, а ∆S0 реакции =288 Дж/(моль·К). Считать, что изменение энтальпии и энтропии не зависит от температуры в данном диапазоне.
Дано: ∆Н0реакции= 283 кДж/моль
∆S0 реакции =288 Дж/(моль·К)
Решение:
Обратите внимание, что T · ΔS° = 323 ∙ 288 ∙ 10–3 = 93,024 кДж/моль, то есть ΔН° > T · ΔS°
Ответ: > 0, реакция эндэргоническая за счет энтальпийного фактора. Реакция не может самопроизвольно протекать при данной температуре.
6. Рассчитайте объем раствора с массовой долей карбоната натрия 15% (g=1,16 г/см3), необходимый для приготовления 120 мл 0,45 М раствора Na2СО3.
Дано: Доля карбоната натрия 15% (g=1,16 г/см3)
120 мл 0,45 М раствора Na2СО3.
1. Вычислим количество вещества Na2CO3 в 0,45М растворе объемом 120 мл:
n(Na2CO3)= C(Na2CO3) ⋅ V(р-ра) = 0,45⋅ 0,12= 0,054 моль
2. Масса вещества составит: m(Na2CO3)= n(Na2CO3) M(Na2CO3)= 0,054 ·106 = 5,72 г
3. Вычислим массу раствора с массовой долей Na2CO3 0,15
mр—ра (Na2CO3)= m(Na2CO3)\ω(Na2CO3)=5,72\0,15 = 38,13 г
4. Vр—ра(Na2CO3)= mр—ра (Na2CO3)\ρр—ра(Na2CO3) = 38,13\1,16 = 32,8 мл
Ответ: 32,8 мл
7. В желудке содержится соляная кислота, которая практически полностью диссоциирует в водных растворах. Рассчитайте рН желудочного сока, если массовая доля HCl в нем составляет в норме 0,05%. Плотность желудочного сока принять равной 1 г/см3.
Дано: 0,05 % HCl в 100 г жел. сока.
Решение: n(HCl)=m/M=0,5/36,5=0,014 моль при плотности жел. сока=1, мол. концентрация С (HCl)=n/V=0,014/0,1=0,14 моль/л HCl=H+ + Cl+ [H+]=C=0,14 моль/л pH=-lg[H+]=0,86
Ответ: 0,86
8. Запишите уравнение Гендерсона-Хасельбаха для расчета рН фосфатной и гидрокарбонатной буферной системы.


