Файл: Задание Химическое строение, классификация и номенклатура органических веществ.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.02.2024
Просмотров: 9
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
-
Типы химических связей и механизмы их образования: все химические связи в молекуле (С–Н, С–О) – локализованные ковалентные σ-связи, образованы по обменному механизму, связь С=С–С – локализованная ковалентная -связь, образована по обменному механизму.
-связь, образована по обменному механизму. -
Количественные параметры связей:
| Параметр | С=С–С | С–О | С–Н |
| Длина связи, нм | 0,139 | 0,143 | 0,111 |
| Энергия связи, кДж/моль | 620 | 360 | 414 |
| Полярность связи | ΔЭО = 0 Ковалентная неполярная | ΔЭО = 3,5-2,5=1 Ковалентная полярная | ΔЭО = 2,5-2,1= 0,4 Ковалентная малополярная |
-
Сопряжение: присутствует. -
Ароматичность: присутствует.
Электронные эффекты в молекуле: в молекуле возникает отрицательный индуктивный эффект (-I), связанный с электроноакцепторными свойствами группы –О–СН3 и положительный мезомерный эффект (+М) группы –О–СН3. +M-эффект в этих группах сильнее, чем -I-эффект. Электронная плотность в бензольном кольце повышается.
-
Распределение электронной плотности в молекуле:
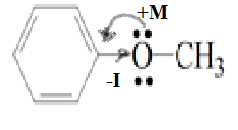
+M > -I
d)
Октетная формула Льюиса:
Н Н Н
. . . . . .
Н : С : : С : С : С : Н
. . . .
. . Н
Н : C
. .
Н
Типы гибридизации атомов в молекуле:
| sp2 sp2 sp3 sp3 | 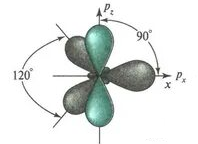 | 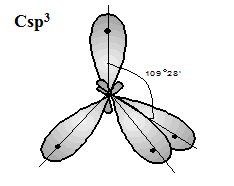 |
Электронное строение молекулы при помощи модели электронных облаков:
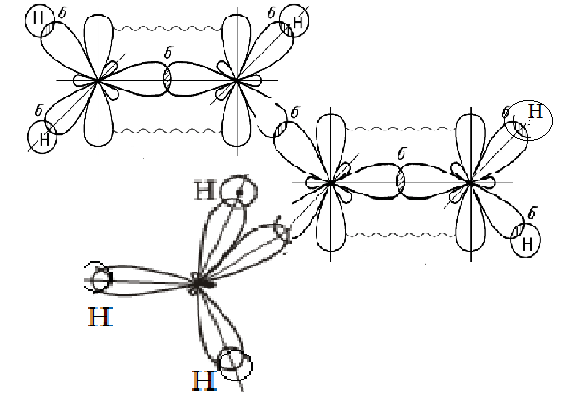
-
Типы химических связей и механизмы их образования: все химические связи в молекуле (С–Н, С–С) – локализованные ковалентные σ-связи, образованы по обменному механизму, связь С=С – локализованная ковалентная -связь, образована по обменному механизму.
-связь, образована по обменному механизму. -
Количественные параметры связей:
| Параметр | С=С | С–С | С–Н |
| Длина связи, нм | 0,134 | 0,154 | 0,111 |
| Энергия связи, кДж/моль | 620 | 348 | 414 |
| Полярность связи | ΔЭО = 0 Ковалентная неполярная | ΔЭО = 0 Ковалентная неполярная | ΔЭО = 2,5-2,1= 0,4 Ковалентная малополярная |
-
Сопряжение: присутствует. -
Ароматичность: отсутствует. -
Электронные эффекты в молекуле: в молекуле возникает положительный индуктивный эффект (+I), связанный с электронодонорными свойствами группы СН3-. -
Распределение электронной плотности в молекуле:
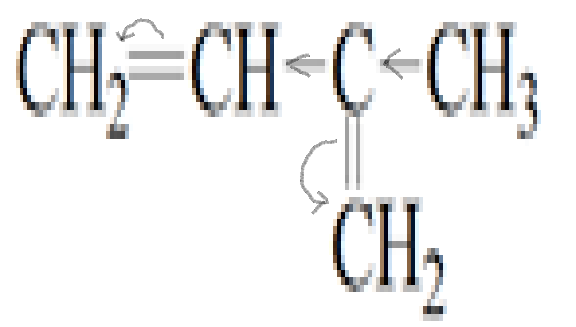
Задание 3.
Пространственное строение органических веществ
Для соединений, названия которых представлены:
-
определите число асимметрических атомов углерода в молекуле, -
определите общее число конфигурационных изомеров, их формулы; -
дайте название стериоизомерам по D,L- номенклатуре и R, S-номенклатуре; -
изобразите диастериомеры, трео-, эритро- и мезо-формы, если таковые имеются. -
для одного из конфигурационных изомеров изобразите с помощью проекции Ньюмена заслоненный и заторможенный конформационный изомер, произвольно выбрав С-С связь; -
для одного из конфигурационных изомеров с двойной связью напишите цис- и транс – изомер, лайте ему название.
Варианты заданий
| Вариант | Названия органических соединений |
| 9. | 2-бром-3-метилбутан; 2-бром-2-метилбутан; 1-бромбутен-2, 3-хлорбутанон-2 |
2-бром-3-метилбутан
Число асимметрических атомов углерода в молекуле:
1 2 3 4
*
СН3 – СН – СН – СН3 nC* = 1
| |
Br СН3
Общее число конфигурационных изомеров: 21 = 2.
Формулы Фишера возможных стериоизомеров:
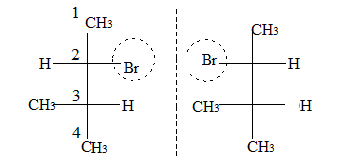
D(R)-2-бром- L(S)-2-бром-
3-метилбутан 3-метилбутан
Название стериоизомеров: у 2-бром-3-метилбутана имеется только одна пара энантиомеров (D и L).
Для того, чтобы определить какова конфигурация, например D-2-бром-3-метилбутана по R,S-номенклатуре, необходимо произвести следующие действия:
1. Определяют старшинство заместителей у С2: Br CH(CH3)2 CH3;
2. Сделать перестановки и определить направление изменения старшинство заместителя.
Полное название D-2-бром-3-метилбутана по R,S-номенклатуре: 2(R)- бром-3-метилбутан.
Конформационные изомеры (для D-2-бром-3-метилбутана по связи С2-С3): заторможенная и заслоненная конфигурации
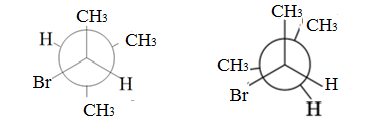
Цис- и транс- изомеры: отсутствуют, так как нет двойных связей С=С.
2-бром-2-метилбутан
Число асимметрических атомов углерода в молекуле:
1 2 3 4
СН3
|
СН3 – С – СН2 – СН3 nC* = 0
|
Br
Общее число конфигурационных изомеров: конфигурационных изомеров нет
Конформационные изомеры (для 2-бром-2-метилбутана по связи С2-С3): заторможенная и заслоненная конфигурации
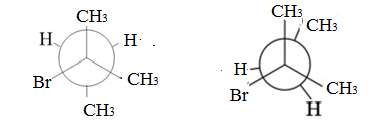
Цис- и транс- изомеры: отсутствуют, так как нет двойных связей С=С.
1-бромбутен-2
Число асимметрических атомов углерода в молекуле:
1 2 3 4
СН2 – СН = СН – СН3 nC* = 0
|
Br
Общее число конфигурационных изомеров: конфигурационных изомеров нет
Конформационные изомеры (для 1-бромбутена-2 по связи С2-С3): нет
Цис- и транс- изомеры: есть, так как есть двойная связь С=С.
BrН2С СН3 BrН2С Н
\ / \ /
С = С С = С
/ \ / \
Н Н Н СН3
Цис-изомер Транс- изомер
3-хлорбутанон-2
Число асимметрических атомов углерода в молекуле:
1 2 3 4
*
СН3 – С – СН – СН3 nC*
= 1
|| |
О Сl
Общее число конфигурационных изомеров: 21 = 2.
Формулы Фишера возможных стериоизомеров:
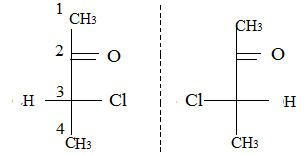
D(R)-3-хлор- L(S)-3-хлор-
бутанон-2 бутанон-2
Название стериоизомеров: у 3-хлорбутанона-2 имеется только одна пара энантиомеров (D и L).
Для того, чтобы определить какова конфигурация, например D-3-хлорбутанона-2 по R,S-номенклатуре, необходимо произвести следующие действия:
1. Определяют старшинство заместителей у С3: OH CООH CH(ОН)СООH ;
2. Сделать две перестановки и определить направление изменения старшинство заместителя.
Полное название D-3-хлор-бутанона-2 по R,S-номенклатуре: 3(R)-хлор-бутанон-2.
Конформационные изомеры (для D-3-хлор-бутанона-2 по связи С3-С4): заторможенная и заслоненная конфигурации
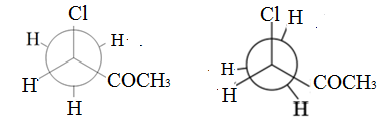
Цис- и транс- изомеры: отсутствуют, так как нет двойных связей С=С.


