ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.02.2024
Просмотров: 64
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
, нанесенный на активированный уголь или другой носитель с развитой поверхностью. Также в качестве катализатора можно применять смесь ацетата цинка и кадмия или просто ацетат кадмия. В качестве развитой поверхности вместо активированного угля применяют оксид алюминия, пемзу или силикагель. Оптимальной температурой является 170-220оС в газовой фазе в трубчатом реакторе со стационарным слоем катализатора при избытке ацетилена.
При парофазном синтезе винилацетата наблюдается получение до 60% побочных продуктов: этилидендиацетат (образующийся из винилацетата и ацетилена), ацетальдегид (из частичного гидролиза ацетилена следами воды) и ацетон. А также наблюдается небольшое количество непредельных соединений, которые образуют смолистый продукт.[6]
По количеству среди примесей самым значимым является ацетальдегид (0,5%-1,8%). Он может получаться при гидратации ацетилена, разложении и гидролизе винилацетата:
CHCH + H2O → CH3CHO 2CHCH + H2O → CH3CH=СНСOН
CH2=CH–OCOCH3 → CH3CHO + CH2=C=O
СH2=CH–OCOCH3 + H2O → CH3CHO + CH3COOH
Воду для данной реакции получают в результате разложения уксусной кислоты:
2CH3COOH → CH3COCH3 + CO2 + H2O
Чтобы увеличить выход целевого продукта, реакцию необходимо проводить с избытком ацетилена относительно уксусной кислоты. В промышленности соотношение ацетилена к кислоте составляет 3,5:1 и до 5:1. Также конверсию уксусной кислоты ограничивают в пределах 60%-70%. Таким образом можно добиться выхода винилацетата вплоть до 99%
Жидкофазный метод получения впервые появился в 1920г. в Канаде, а затем, данный метод начал распространяться по Европе: в Италии, Бельгии, во Франции и других странах.
Данный синтез протекает в присутствии катализатора: азотнокислой закиси ртути или фосфорнокислой ртути. Промотирующими добавками являются трифторид бора, кремнийвольфрамовые кислоты, ртутная соль фторводородной и мышьяковистой кислоты.
В качестве побочного продукта получается этилидендиацетат, образующийся в присутствии бензосульфоната или оксида алюминия и разлагается на уксусную кислоту и винилацетат.
CH3–CH(OCOCH3)2 → CH2=CH–OCOCH3 + CH3COOH
На данный момент жидкофазный синтез не используется в промышленных масштабах. [9]
Уравнение реакции получения винилацетата из уксусной кислоты и этилена:
CH2=CH2 + 0,5О2 + CH3COOH → CH2=CH–OCOCH3 + Н2О
Реакция ацетоксилирования этилена в присутствии восстановленного катализатора (соли палладия:хлорид, бромид, ацетат; и металлический палладий). Происходит замещение водорода в этилене группой CH3COO- в присутствии кислорода.
Синтез также может проводиться двумя способами: жидкофазным и парофазным.
Основы жидкофазного метода были разработаны советскими учеными М.Н. Варгафтиком и И. И. Моисеевым. В роли катализатора участвовали соли палладия карбоновых кислот, соли меди и кислород. Промышленное
производство винилацетата на основе этилена жидкофазным
методом впервые было осуществлено в 1966 году английской фирмой «АйСиАй». [7]
Процесс осуществляют в интервале температур 353-403 К и давлении 1,0-7,0 МПа. Реакция получения винилацетата из этилена жидкофазным методом описывается следующим уравнением: [7]
CH2=CH2 + CH3COOH + PdCl2 → CH2=CH―OCOCH3 + 2HCl + Pd
В результате каталитического цикла, высвобождающийся металлический палладий вновь переводится в степень окисления +2 путем взаимодействия с редокс-системой, в качестве которой используют соли любого поливалентного металла, имеющего большой потенциал окисления, предпочтительно соли меди. Для поддержания меди со степенью окисления +2 в реактор периодически или непрерывно добавляют соляную кислоту в результате реакций:
Pd + 2CuCl2 → PdCl2 + 2CuCl
2CuCl + 2HCl + 0,5O2 → 2CuCl2 + H2O
Также к катализаторному раствору добавляют карбоксилаты щелочных и щелочноземельных металлов, например ацетаты лития, калия, натрия. Побочными продуктами реакции синтеза является ацетальдегид, CO2, H2O, и в малых количествах этилидендиацетат, моно- и диацетаты гликоля, щавелевая кислота, β-хлорацетат и ряд других соединений. Самым значительным из них является ацетальдегид (примерно 20%-25% по содерж.). Одним из самых вредоносных продуктов является щавелевая кислота, образующая нерастворимые окасалаты с ионами меди и палладия в катализаторном растворе.
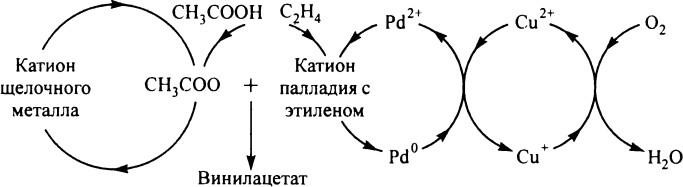
Рисунок 4 Схема получения винилацетата жидкофазным методом
Для полной компенсации уксусной кислоты, используемой в синтезе винилацетата, требуется определенное количество ацетальдегида. Для этого необходимо поддерживать постоянное мольное соотношение винилацетата и ацетальдегида, равное 1,14. Тогда для получения винилацетата можно использовать необезвоженную свежую уксусную кислоты и не проводить
обезвоживания возвратной уксусной кислоты, что значительно снижает затраты на разделение реакционной смеси.
Ацетат натрия, необходимый для протекания этой реакции, в случае хлорида палладия является источником ионов ацетата, участвующих во внутрисферной нуклеофильной, а также в процессе изомеризации комплекса в металлоорганическое соединение. Активность катализатора из палладия при синтезе винилацетата повышается практически в 10 раз при добавлении 2%- 10% ацетатов щелочных металлов. Гидролизу винилацетата с образованием ацетальдегида способствуют повышение содержания воды, температуры, длительности пребывания винилацетата в реакционной зоне, содержания палладия в растворе катализатора. [9]
При диапазоне температур 100оС-130оС активно работает катализатор. Температура определяет скорость процесса, при увеличении температуры на 10оС скорость увеличивается в 1,3 раза. При увеличении температуры усиливается гидролиз винилацетата и повышается выход ацетальдегида
, но влияние концентрации воды на выход ацетальдегида сказывается сильнее, чем температура.
При повышении парциальных давлений этилена и кислорода снижается выход этилидендиацетата, за счет увеличения растворимости и скорости основной реакции. Увеличение давления этилена приблизительно пропорцианально увеличивает объемную производительность реактора.
Оптимальные условия:
Температура: 100оС -130оС Давление: 3МПа-4Мпа
Содержание ионов Pd: 30мг/л-50мг/л Содержание ионов Cu: 3г/л-5г/л
Для отгонки полученных ацетальдегида и винилацетата используется большой избыток этилена; потери хлорид-ионов компенсируются подачей НСl. В этих условиях конверсия уксусной кислоты достигает от 20 до 30 %, а этилена только от 2 до 3% за один проход.
Побочные продукты реакции: бутены, хлорорганические соединения, щавелевая и муравьиная кислоты, сложные эфиры, углекислый газ и др.
При парофазном синтезе винилацетата наблюдается получение до 60% побочных продуктов: этилидендиацетат (образующийся из винилацетата и ацетилена), ацетальдегид (из частичного гидролиза ацетилена следами воды) и ацетон. А также наблюдается небольшое количество непредельных соединений, которые образуют смолистый продукт.[6]
По количеству среди примесей самым значимым является ацетальдегид (0,5%-1,8%). Он может получаться при гидратации ацетилена, разложении и гидролизе винилацетата:
CHCH + H2O → CH3CHO 2CHCH + H2O → CH3CH=СНСOН
CH2=CH–OCOCH3 → CH3CHO + CH2=C=O
СH2=CH–OCOCH3 + H2O → CH3CHO + CH3COOH
Воду для данной реакции получают в результате разложения уксусной кислоты:
2CH3COOH → CH3COCH3 + CO2 + H2O
Чтобы увеличить выход целевого продукта, реакцию необходимо проводить с избытком ацетилена относительно уксусной кислоты. В промышленности соотношение ацетилена к кислоте составляет 3,5:1 и до 5:1. Также конверсию уксусной кислоты ограничивают в пределах 60%-70%. Таким образом можно добиться выхода винилацетата вплоть до 99%
3.1.2 Жидкофазный метод
Жидкофазный метод получения впервые появился в 1920г. в Канаде, а затем, данный метод начал распространяться по Европе: в Италии, Бельгии, во Франции и других странах.
Данный синтез протекает в присутствии катализатора: азотнокислой закиси ртути или фосфорнокислой ртути. Промотирующими добавками являются трифторид бора, кремнийвольфрамовые кислоты, ртутная соль фторводородной и мышьяковистой кислоты.
В качестве побочного продукта получается этилидендиацетат, образующийся в присутствии бензосульфоната или оксида алюминия и разлагается на уксусную кислоту и винилацетат.
CH3–CH(OCOCH3)2 → CH2=CH–OCOCH3 + CH3COOH
На данный момент жидкофазный синтез не используется в промышленных масштабах. [9]
-
Получение винилацетата из этилена и уксусной кислоты
Уравнение реакции получения винилацетата из уксусной кислоты и этилена:
CH2=CH2 + 0,5О2 + CH3COOH → CH2=CH–OCOCH3 + Н2О
Реакция ацетоксилирования этилена в присутствии восстановленного катализатора (соли палладия:хлорид, бромид, ацетат; и металлический палладий). Происходит замещение водорода в этилене группой CH3COO- в присутствии кислорода.
Синтез также может проводиться двумя способами: жидкофазным и парофазным.
-
Жидкофазный метод
Основы жидкофазного метода были разработаны советскими учеными М.Н. Варгафтиком и И. И. Моисеевым. В роли катализатора участвовали соли палладия карбоновых кислот, соли меди и кислород. Промышленное
производство винилацетата на основе этилена жидкофазным
методом впервые было осуществлено в 1966 году английской фирмой «АйСиАй». [7]
Процесс осуществляют в интервале температур 353-403 К и давлении 1,0-7,0 МПа. Реакция получения винилацетата из этилена жидкофазным методом описывается следующим уравнением: [7]
CH2=CH2 + CH3COOH + PdCl2 → CH2=CH―OCOCH3 + 2HCl + Pd
В результате каталитического цикла, высвобождающийся металлический палладий вновь переводится в степень окисления +2 путем взаимодействия с редокс-системой, в качестве которой используют соли любого поливалентного металла, имеющего большой потенциал окисления, предпочтительно соли меди. Для поддержания меди со степенью окисления +2 в реактор периодически или непрерывно добавляют соляную кислоту в результате реакций:
Pd + 2CuCl2 → PdCl2 + 2CuCl
2CuCl + 2HCl + 0,5O2 → 2CuCl2 + H2O
Также к катализаторному раствору добавляют карбоксилаты щелочных и щелочноземельных металлов, например ацетаты лития, калия, натрия. Побочными продуктами реакции синтеза является ацетальдегид, CO2, H2O, и в малых количествах этилидендиацетат, моно- и диацетаты гликоля, щавелевая кислота, β-хлорацетат и ряд других соединений. Самым значительным из них является ацетальдегид (примерно 20%-25% по содерж.). Одним из самых вредоносных продуктов является щавелевая кислота, образующая нерастворимые окасалаты с ионами меди и палладия в катализаторном растворе.

Рисунок 4 Схема получения винилацетата жидкофазным методом
Для полной компенсации уксусной кислоты, используемой в синтезе винилацетата, требуется определенное количество ацетальдегида. Для этого необходимо поддерживать постоянное мольное соотношение винилацетата и ацетальдегида, равное 1,14. Тогда для получения винилацетата можно использовать необезвоженную свежую уксусную кислоты и не проводить
обезвоживания возвратной уксусной кислоты, что значительно снижает затраты на разделение реакционной смеси.
Ацетат натрия, необходимый для протекания этой реакции, в случае хлорида палладия является источником ионов ацетата, участвующих во внутрисферной нуклеофильной, а также в процессе изомеризации комплекса в металлоорганическое соединение. Активность катализатора из палладия при синтезе винилацетата повышается практически в 10 раз при добавлении 2%- 10% ацетатов щелочных металлов. Гидролизу винилацетата с образованием ацетальдегида способствуют повышение содержания воды, температуры, длительности пребывания винилацетата в реакционной зоне, содержания палладия в растворе катализатора. [9]
При диапазоне температур 100оС-130оС активно работает катализатор. Температура определяет скорость процесса, при увеличении температуры на 10оС скорость увеличивается в 1,3 раза. При увеличении температуры усиливается гидролиз винилацетата и повышается выход ацетальдегида
, но влияние концентрации воды на выход ацетальдегида сказывается сильнее, чем температура.
При повышении парциальных давлений этилена и кислорода снижается выход этилидендиацетата, за счет увеличения растворимости и скорости основной реакции. Увеличение давления этилена приблизительно пропорцианально увеличивает объемную производительность реактора.
Оптимальные условия:
Температура: 100оС -130оС Давление: 3МПа-4Мпа
Содержание ионов Pd: 30мг/л-50мг/л Содержание ионов Cu: 3г/л-5г/л
Для отгонки полученных ацетальдегида и винилацетата используется большой избыток этилена; потери хлорид-ионов компенсируются подачей НСl. В этих условиях конверсия уксусной кислоты достигает от 20 до 30 %, а этилена только от 2 до 3% за один проход.
Побочные продукты реакции: бутены, хлорорганические соединения, щавелевая и муравьиная кислоты, сложные эфиры, углекислый газ и др.
- 1 2 3 4 5 6 7 8 9 10

