ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 29.04.2024
Просмотров: 106
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
27. Если температурный коэффициент реакции = 2, то при повышении температуры на 20˚С скорость реакции возрастает в ___ раз(а).
| а) 2 | б) 20 | в) 8 | г) 4 |
28. Если температурный коэффициент реакции = 2, то чтобы уменьшить скорость реакции в 8 раз, необходимо понизить температуру на ___ ˚С.
| а) 30 | б) 20 | в) 10 | г) 40 |
29. Если температурный коэффициент химической реакции равен 3, то чтобы уменьшить скорость реакции в 27 раз, необходимо температуру понизить на ___˚С
| а) 30 | б) 20 | в) 10 | г) 40 |
30. Неверно, что при добавлении катализатора
1) изменяется механизм реакции
2) понижается энергия активации
3) увеличивается скорость реакции
4) происходит смещение положения химического равновесия
17. Равновесие
1. Для смещения равновесия в системе SO2() + Cl2() SO2Cl2(), H<0 в сторону продуктов реакции необходимо
| 1) понизить концентрацию SO2 | 3) понизить давление |
| 2) понизить температуру | 4) ввести катализатор |
2. Для смещения равновесия в системе
H2(Г) + S(Т) H2S(Г), H = -21 кДж
в сторону образования сероводорода
а) повысить давление б) понизить давление
в) понизить температуру г) повысить температуру
3. Для увеличения выхода продуктов реакции
2Pb(NO3)2(Т) 2PbO(Т) + 4NO2(Г) + O2(Г) , H0 > 0 необходимо
а) увеличить температуру б) ввести катализатор
в) увеличить давление г) уменьшить температуру
4. Для смещения равновесия в системе
CaCO3(Т) CaO(Т) + CO2(Г); H > 0 в сторону продуктов реакции необходимо
а) увеличить давление б) ввести катализатор
в) увеличить температуру г) уменьшить температуру
5. Для смещения равновесия в системе
MgO(Т) + CO2(Г) MgCO3(Т), H<0
в сторону продуктов реакции необходимо
а) понизить давление б) понизить температуру
в) повысить температуру г) ввести катализатор
6. Для смещения равновесия в системе
SO2(Г) + Cl2(Г) SO2Cl2(Г), H<0
в сторону продуктов реакции необходимо …
а) ввести катализатор б) понизить температуру
в) понизить давление г )понизить концентрацию SO2
7. Для увеличения выхода аммиака по уравнению реакции
N2(Г) + 3H2(Г) 2NH3(Г), H < 0 необходимо ...
а) повысить концентрацию NH3 б) понизить концентрацию азота
в) понизить давление г) понизить температуру0>0>
8. При увеличении давления в системе H2(Г) + I2(Г) 2HI(Г), HO < 0,
1) увеличивается содержание продуктов
2) увеличивается содержание продуктов и исходных веществ
3) состояние равновесия не изменяется
4) увеличивается содержание исходных веществ
9. При увеличении давления в системе CO() + 2H2() CH3OH(), H < 0,
1) увеличивается выход продуктов
2) уменьшается выход продуктов
3) состояние равновесия меняется неоднозначно
4) состояние равновесия не изменяется
10. Для смещения равновесия в системе
CO(Г) + 2H2(Г) CH3OH(Г), H < 0
в сторону продуктов реакции необходимо
| 1) понизить давление | 3) понизить концентрацию водорода |
| 2) повысить давление | 4) повысить температуру |
11. При увеличении температуры в системе
C2H2(Г) + H2О(Г) C2H5OH(Г), H0 < 0
равновесие
| 1) не изменится | 3) сместится в сторону продуктов реакции |
| 2) изменится неоднозначно | 4) сместится в сторону исходных веществ |
12. Увеличение температуры вызывает смещение равновесия в сторону ___ процесса.
| 1) адиабатического | 3) изотермического |
| 2) экзотермического | 4) эндотермического |
13. Состояние равновесия характеризуется равенством
а) температуры продуктов и исходных веществ
б) количества вещества в системе
в) концентраций продуктов и исходных веществ
г) скоростей прямого и обратного процессов
14. Для смещения равновесия в системе H2(Г) + I2(Г) 2HI(Г), H < 0 в сторону исходных веществ необходимо
а) уменьшить температуру
б) увеличить концентрацию йода
в) увеличить давление
г) уменьшить концентрацию йода
15. Понижение температуры вызывает смещение положения равновесия в сторону ____ реакции
| а) адиабатической | в) экзотермической |
| б) изотермической | г) эндотермической |
16. Уравнение константы равновесия гетерогенной химической реакции SiO2(к.) + H2(г.) Si(к.) + 2H2O(г.) имеет вид
| а) | в) 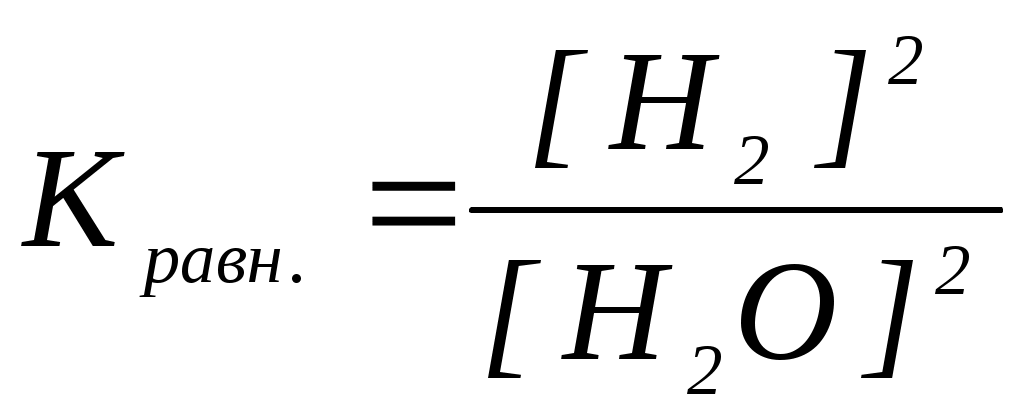 |
| б) | г) 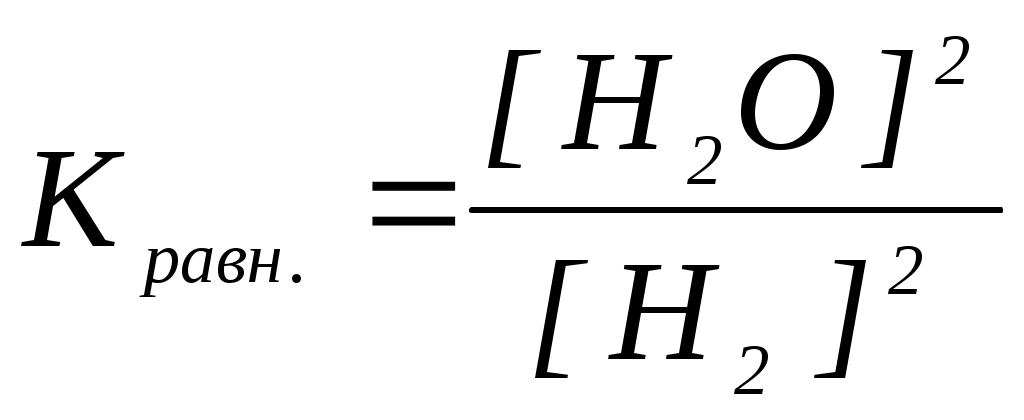 |
17. Уравнение константы равновесия гетерогенной химической реакции 2NaHCO3(К.) Na2CO3(К.) + H2O(Г.) + CO2(Г.) имеет вид
| а) | в) |
| б) | г) |
18. Уравнение константы равновесия гетерогенной химической реакции 3S(к.) + 2H2O(г.) 2H2S(г.) + SO2(г.) имеет вид
| а) 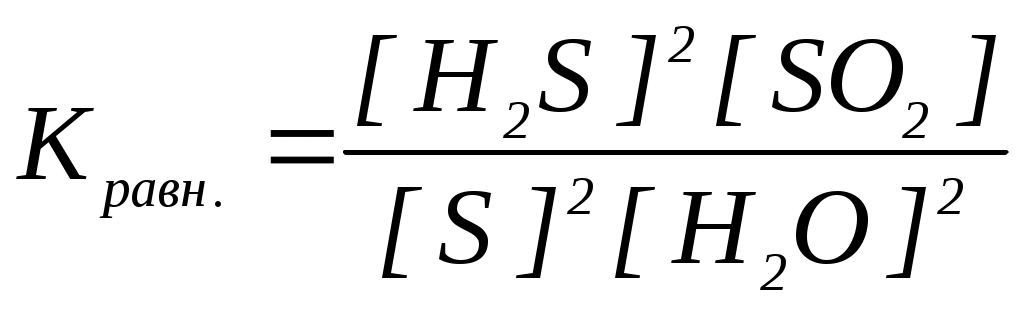 | в) 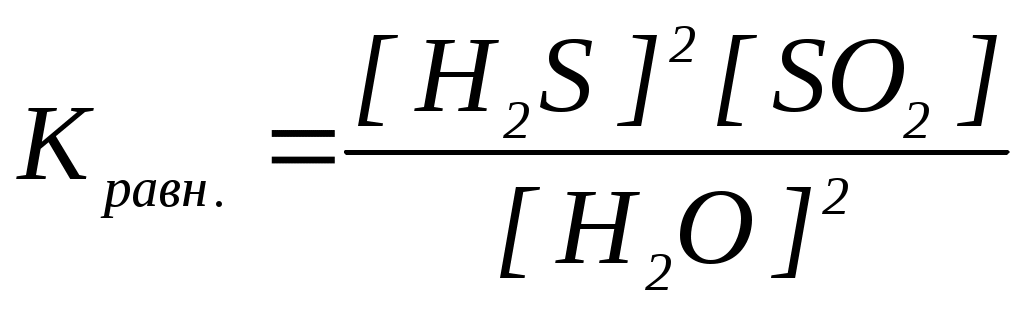 |
| б) 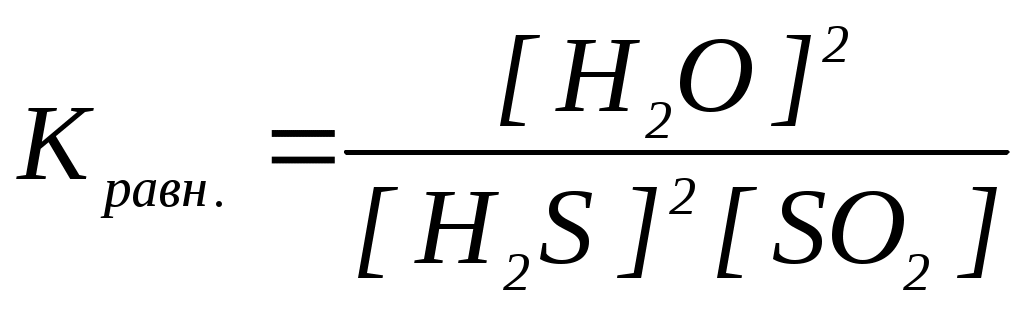 | г) 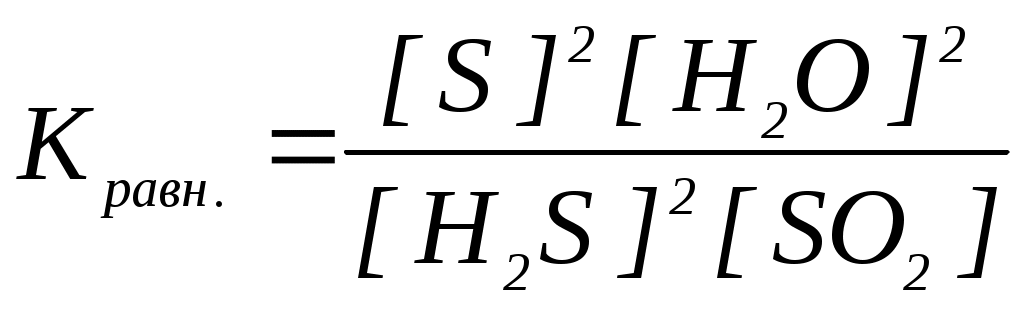 |
19. Уравнение константы равновесия гетерогенной химической реакции 2CO(г.) С(графит) + CO2(г.) имеет вид
| а) | в) |
| б) | г) |
20. Если прямая реакция равновесной конденсированной системы протекает с выделением теплоты, то для смещения положения равновесия в сторону продуктов, следует
| 1) понизить температуру | 3) повысить температуру |
| 2) повысить давление | 4) понизить давление |
21. Константа скорости химической реакции не зависит от
| 1) природы реагирующих веществ | 3) температуры |
| 2) концентраций реагирующих веществ | 4) наличия катализатора |
18. Общие свойства раствором
1. Раствор, содержащий 11,6 г вещества в 400 г воды, замерзает при температуре
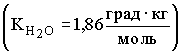 . Тогда молярная масса растворенного вещества равна
. Тогда молярная масса растворенного вещества равна | 1) 29 г/моль | 2) 58 г/моль | 3) 87 г/моль | 4) 116 г/моль |
2. Давление паров воды при 25С составляет 3,167 кПа. Давление пара (кПа) над раствором, в 450 г которого содержится 180 г глюкозы, равно
| 1) 1,267 | 2) 2,969 | 3) 1,900 | 4) 1,198 |
3. Концентрация раствора глюкозы, кипящего при 100,780С (ЕH2O = 0,52 град*кг/моль) равна ….
а) 0,3 моль/кг б) 1 моль/кг в) 0,5 моль/кг г) 1,5 моль/кг
4. Осмотическое давление 0,1М раствора глицерина при 25С равно


