Файл: Курсовая работа по дисциплине Общая химическая технология Тема Синтез аммиака в производстве аммиака.docx
Добавлен: 03.05.2024
Просмотров: 409
Скачиваний: 6
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
Можно подвести итог, что для начального содержания исходных веществ повышение температуры будет влиять положительно на скорость реакции, а при дальнейшем увеличении содержания аммиака в смеси, температуру необходимо уменьшать, чтобы скорость реакции не уменьшалась. По уравнению Тёмкина-Пыжова (1) можно сделать вывод: На скорость протекания синтеза аммиака повышение температуры будет влиять положительно, так как k1иk2 будут увеличиваться, и Kр тоже будет расти, а понижение температуры – отрицательно, так как Kр будет уменьшатьсяи скорость соответственно тоже.
Разложим уравнение Тёмкина-Пыжева (1) на две части, для прямой и обратной реакции соответственно:
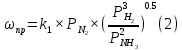
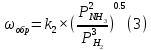
Мы видим, что для прямой реакции с ростом давления исходных реагентов (PH2, PN2) скорость будет увеличиваться, с уменьшением давления наоборот – снижаться. Для обратной реакции с увеличением давления исходных веществ (PH2), скорость будет уменьшаться, а с увеличением давления продукта (PNH3), скорость будет увеличиваться.
Поэтому обратимся к закону Дальтона, чтобы сделать вывод о влиянии общего давления на систему:
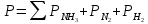
Повышение парциального давления исходных реагентов увеличивает общее давление, что благоприятно сказывается наскорости реакции синтеза аммиака, а понижение давления реагентов будет уменьшать общее давление, что отрицательно отразится на скорости реакции.
Преобразуем уравнения скорости (2) и (3):
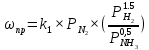
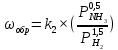
Скорость реакции зависит от концентрации исходных веществ и по мере протекания процесса исходные вещества расходуются, и их концентрация уменьшается, поэтому скорость прямой реакции тоже уменьшается. С дальнейшим протеканием процесса будет увеличивается скорость обратной реакции, потому что будет происходить увеличение концентрация конечных веществ. Поэтому при увеличении концентрации N2, скорость процесса будет увеличиваться, потому что PN2 тоже будет увеличиваться. Если мы будем увеличивать H2, то
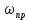 будет увеличиваться, что видно по уравнению, а
будет увеличиваться, что видно по уравнению, а 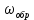 будет уменьшаться, значит общая скорость процесса будет увеличиваться. При увеличении содержания NH3скорость прямой реакции будет уменьшаться, а обратной реакции – увеличиваться.
будет уменьшаться, значит общая скорость процесса будет увеличиваться. При увеличении содержания NH3скорость прямой реакции будет уменьшаться, а обратной реакции – увеличиваться.Тогда для увеличения скорости можно увеличить содержание исходных продуктов, либо уменьшить начальное содержание аммиака и инертных веществ.
Рассмотрим, как катализаторы будут влиять на кинетику реакции. Катализаторы используются для ускорения процесса при низких температурах, поэтому, чем катализатор будет активнее, тем температура, при которой с оптимальной скоростью можно проводить реакцию будет ниже. В процессе синтеза аммиака применяются железные катализаторы с добавлением промоторов, для повышения его активности, потому что чистое железо быстро теряет свою активность. Промоторы в промышленном использовании бывают двух видов:
1. Структурообразующие (Al2O3, MgO, SiO2 и др.)
2. Модифицирующие (K2O, CaO и др.)
Каталитическими действиями они не обладают, но улучшают активность и селективность катализаторов. Катализатор, применяемый для синтеза аммиака, содержит 90-93% Fe3O4 и 7-10% промоторов. Один из которых K2O, он, повышая удельную каталитическую активность поверхности, снижает термостойкость и устойчивость к кислотосодержащим ядам. Содержание Al2O3 увеличивает активную поверхность, термоустойчивость и стойкость к кислородосодержащим ядам, которые снижают активность катализатора. Селективность характеризуется избирательностью катализатора, то есть если мы имеем основную реакцию и побочные, то катализатор не должен влиять на побочные. Для синтеза аммиака побочных реакций не имеется, значит, селективность катализатора не будет играть важную роль. В случае синтеза аммиака ядами являются инертные вещества, такие как аргон, гелий, они снижают общее давление и уменьшают реакцию протекания процесса. Если применять гранулированный катализатор будет обеспечиваться более равномерная структура слоя и равномерное распределение газового потока, а мелкозернистый катализатор в свою очередь уменьшает диффузионное торможение
, увеличивая выход аммиака. Для синтеза аммиака выпускают два вида катализатора CA-1(окисленный) по ОСТ 113-03-71-78 и СА-2(восстановленный) по ТУ-6-03-394-79в гранулированном и дробленом виде [3]:
Таблица 3.2 – Характеристики катализаторов
| Марка | Форма зерен | Размер зерен, мм | Относительная активность |
| CA-1 и CA-2 | Дробленый | 10-15 | 1,0 |
| 5-7 | 1,15 | ||
| 1-3 | 1,25 | ||
| CA-2 | Гранулированный | 10-15 | - |
| 5-7 | 1,50 | ||
| 1-3 | 4,0 |
В промышленных каталитических реакторах процесс синтеза аммиака
протекаетприменяющихсяподлинезоныкатализаторатемпературе,
объемнойскорости,составегазаит.д.,чтоприводиткизменению
химического состава и строения поверхности катализатора и вследствие этого
– активности катализатора.
В окисленном состоянии катализатор содержит 90-93G% магнетита Fe
3
O
4
c некоторымизбыткомFeOпосравнениюсостехиометрическим,7-10G%
промотирующих(Al
2
O
3
,К
2
О,СаО)ипримесных(SiO
2
идр.)соединений.
Качество катализатора гарантируется единым отраслевым стандартом.
Катализатор синтеза аммиака выпускают двух марок СА-1 (окисленный)
и СА-1В (восстановленный), в гранулированном и дробленном виде.
Основныефизическиесвойствакатализаторов:содержание
нерасколотыхгранул,коэффициентокруглости,насыпнаяплотность,
прочность гранул, удельная поверхность, общая пористость, Gпорозность слоя
Призагрузкекатализаторахвколоннунеобходимоучитывать
конструктивныеособенностиколонны,допустимоегидравлическое
сопротивлениесистемы,формучастицкатализатора.Приприменении
гранулированного катализатора обеспечивается более равномерная структура
слояиболееравномерноераспределениегазовогопотока.Использование
мелкозернистогокатализаторапозволяетуменьшитьдиффузионное
торможениеиувеличитьвыходаммиака,однакоприэтомувеличивается
гидравлическое сопротивление слоя.
Восстановлениекатализатораипускколонныприеезагрузкетолько
окисленным катализатором продолжается 7-10 суток.
Восстановленныйкатализаторобладаетпирофорнымисвойствами
(самовозгорается на воздухе). Чтобы предотвратить самовозгорание проводят
пассивацию (окисление поверхности катализатора) кислородом воздуха,
дозируемого впотоказота,которыйпропускаютчерезкатализатор с
объемнойскоростьюдо1000час
-1
притемпературевзонепассивациине
выше 150
о
С
В промышленных каталитических реакторах процесс синтеза аммиака
протекаетприменяющихсяподлинезоныкатализаторатемпературе,
объемнойскорости,составегазаит.д.,чтоприводиткизменению
химического состава и строения поверхности катализатора и вследствие этого
– активности катализатора.
В окисленном состоянии катализатор содержит 90-93G% магнетита Fe
3
O
4
c некоторымизбыткомFeOпосравнениюсостехиометрическим,7-10G%
промотирующих(Al
2
O
3
,К
2
О,СаО)ипримесных(SiO
2
идр.)соединений.
Качество катализатора гарантируется единым отраслевым стандартом.
Катализатор синтеза аммиака выпускают двух марок СА-1 (окисленный)
и СА-1В (восстановленный), в гранулированном и дробленном виде.
Основныефизическиесвойствакатализаторов:содержание
нерасколотыхгранул,коэффициентокруглости,насыпнаяплотность,
прочность гранул, удельная поверхность, общая пористость, Gпорозность слоя
Призагрузкекатализаторахвколоннунеобходимоучитывать
конструктивныеособенностиколонны,допустимоегидравлическое
сопротивлениесистемы,формучастицкатализатора.Приприменении
гранулированного катализатора обеспечивается более равномерная структура
слояиболееравномерноераспределениегазовогопотока.Использование
мелкозернистогокатализаторапозволяетуменьшитьдиффузионное
торможениеиувеличитьвыходаммиака,однакоприэтомувеличивается
гидравлическое сопротивление слоя.
Восстановлениекатализатораипускколонныприеезагрузкетолько
окисленным катализатором продолжается 7-10 суток.
Восстановленныйкатализаторобладаетпирофорнымисвойствами
(самовозгорается на воздухе). Чтобы предотвратить самовозгорание проводят
пассивацию (окисление поверхности катализатора) кислородом воздуха,
дозируемого впотоказота,которыйпропускаютчерезкатализатор с
объемнойскоростьюдо1000час
-1
притемпературевзонепассивациине
выше 150
о
С
При разработке катализатора, используемого в промышленности следует
учитыватьдлительностьслужбыкатализатора(нескольколет)вусловиях
некоторой нестационарности технологического процесса.
В промышленных каталитических реакторах процесс синтеза аммиака
протекаетприменяющихсяподлинезоныкатализаторатемпературе,
объемнойскорости,составегазаит.д.,чтоприводиткизменению
химического состава и строения поверхности катализатора и вследствие этого
– активности катализатора.
В окисленном состоянии катализатор содержит 90-93G% магнетита Fe
3
O
4
c некоторымизбыткомFeOпосравнениюсостехиометрическим,7-10G%
промотирующих(Al
2
O
3
,К
2
О,СаО)ипримесных(SiO
2
идр.)соединений.
Качество катализатора гарантируется единым отраслевым стандартом.
Катализатор синтеза аммиака выпускают двух марок СА-1 (окисленный)
и СА-1В (восстановленный), в гранулированном и дробленном виде.
Основныефизическиесвойствакатализаторов:содержание
нерасколотыхгранул,коэффициентокруглости,насыпнаяплотность,
прочность гранул, удельная поверхность, общая пористость, Gпорозность слоя
Призагрузкекатализаторахвколоннунеобходимоучитывать
конструктивныеособенностиколонны,допустимоегидравлическое
сопротивлениесистемы,формучастицкатализатора.Приприменении
гранулированного катализатора обеспечивается более равномерная структура
слояиболееравномерноераспределениегазовогопотока.Использование
мелкозернистогокатализаторапозволяетуменьшитьдиффузионное
торможениеиувеличитьвыходаммиака,однакоприэтомувеличивается
гидравлическое сопротивление слоя.
Восстановлениекатализатораипускколонныприеезагрузкетолько
окисленным катализатором продолжается 7-10 суток.
Восстановленныйкатализаторобладаетпирофорнымисвойствами
(самовозгорается на воздухе). Чтобы предотвратить самовозгорание проводят
пассивацию (окисление поверхности катализатора) кислородом воздуха,
дозируемого впотоказота,которыйпропускаютчерезкатализатор с
