ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.05.2024
Просмотров: 7
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
= O2 + 4H+.
Далее составляем схему электролиза с растворимым анодом. Электрохимическая система:
(-) Fe | SbF3, H2O | Sb (+).
Реакции на электродах:
А: Sb0 = Sb3+ + 3е.
К: Mn3+ + 3е = Mn0,
2Н+ + 2е = Н2.
Схема электролиза водного раствора SbF3 c растворимым анодом:
(–) Катод (+) Анод
← Sb3+ → H2O
← H+ → F
→ Fe0
Sb3+ + 3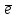 = Sb0 2F- - -2e=F2
= Sb0 2F- - -2e=F2
2H+ + 2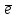 = H2 2Fe0 - 4
= H2 2Fe0 - 4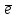 = 2Fe2+.
= 2Fe2+.
Количество электричества по закону Фарадея составит
Q=It=mzF/ABi=0,77·3·96500/122·0,71=2573,48 Кл
Оно пропущено в течении времени
t=Q/I=2573,48 /0,99·3600=0,72 ч
Далее составляем схему электролиза с растворимым анодом. Электрохимическая система:
(-) Fe | SbF3, H2O | Sb (+).
Реакции на электродах:
А: Sb0 = Sb3+ + 3е.
К: Mn3+ + 3е = Mn0,
2Н+ + 2е = Н2.
Схема электролиза водного раствора SbF3 c растворимым анодом:
(–) Катод (+) Анод
← Sb3+ → H2O
← H+ → F

→ Fe0
Sb3+ + 3
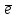 = Sb0 2F- - -2e=F2
= Sb0 2F- - -2e=F22H+ + 2
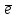 = H2 2Fe0 - 4
= H2 2Fe0 - 4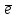 = 2Fe2+.
= 2Fe2+. Количество электричества по закону Фарадея составит
Q=It=mzF/ABi=0,77·3·96500/122·0,71=2573,48 Кл
Оно пропущено в течении времени
t=Q/I=2573,48 /0,99·3600=0,72 ч


