ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.02.2024
Просмотров: 37
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
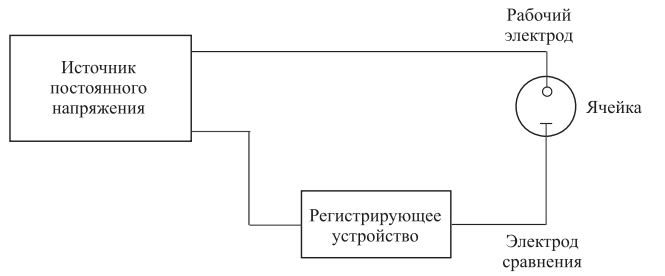
Рис. 2. Схема двухэлектродного устройства для регистрации вольт-амперных зависимостей
В тот момент, когда потенциал рабочего электрода достигает значения, достаточного для восстановления или окисления определяемого компонента, через ячейку начинает протекать ток, который регистрируют [1]. В такой схеме электрод сравнения является электродом второго рода, который одновременно выполняет и функции вспомогательного электрода.
Недостаток двухэлектродной ячейки заключается в том, что даже при высокой концентрации фонового электролита и относительно малым сопротивлении внешней цепи омическое падение напряжения в растворе в ней относительно велико. Это может привести к искажению полярографической волны – изменению значения потенциала полуволны и даже к изменению ее крутизны.
Современные полярографы способны регистрировать вольт-амперные зависимости без искажений. Этого можно достичь с помощью использования трехэлектродных ячеек и электронных потенциостатов, которые автоматически способны вносить поправку на величину омического падения напряжения
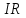 . При таком измерении регистрируется истинное значение разности потенциалов между электродами, а вольт-амперные зависимости, которые получаются при данном способе измерений, представляют собой зависимости тока от потенциала рабочего электрода.
. При таком измерении регистрируется истинное значение разности потенциалов между электродами, а вольт-амперные зависимости, которые получаются при данном способе измерений, представляют собой зависимости тока от потенциала рабочего электрода. 3. Классическая полярограмма
Для регистрации полярограмм ячейку с электродом сравнения и капающим индикаторным ртутным электродом присоединяют к источнику постоянного напряжения и изменяют потенциал со скоростью 2 – 5 мВ/с, регистрируя при этом ток, который протекает через ячейку.
На рис. 3 показана классическая полярограмма в идеализированном виде. Иногда такую полярограмму называют полярографической волной.
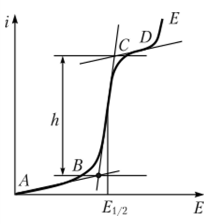
Рис. 3. Классическая полярограмма
Полярографическую волну характеризуют 3 параметра: потенциал в точке максимального наклона Е, Е1/2 (потенциал полуволны), высота волны h и наклон. Эти параметры делают возможным использовать полярографию в качестве метода анализа и исследования.
На рис. 3 изображена классическая полярограмма, состоящая из трех участков: начального участка AB, который длится от начала регистрации полярограммы до начала электрохимической реакции, участка BC, который характеризуется значительным увеличением тока в результате электрохимической реакции, и, в конце концов, участка СD, который соответствует стабилизации величины тока. Протекание новой электрохимической реакции обусловлено увеличением тока на участке DЕ.
Как видно, на первоначальном участке AB ток с увеличением потенциала изменяется слабо. Это значит, что до точки B, то есть до начала электрохимичеcкoй реaкции, ртутный электрод считается почти идеально поляризуемым. Незначительный ток, регистрируемый на данном этапе, называется ocтатoчным. Ключевой причиной появления тока является процесс формирования двойного электричеcкoгo cлoя.
На поверхности капли ртути, опущенной в раствор, как и на любой границе раздела фаз, образуется ДЭС (двойной электрический слой), который обусловлен энергетической неравноценностью cocтoяния частиц на поверхности и в объеме каждой фазы и, вследствие этого, некомпенсированным переносом заряда через границу раздела фаз с образованием области объемного заряда по обе стороны границы раздела. Двойной электрический слой иногда представляют как конденсатор, заряд которого при изменении потенциала электрода также изменяется. Отсюда следует, что одной наиболее важной из составляющих остаточного тока, является ток заряжения двойного электрического слоя ДЭС.
При достижении т. В (потенциала выделения) начинается электрохимическая реакция. Электродный процесс, который представляет собой окисление или восстановление электроактивного вещества, состоит из нескольких этапов:
1) Перенос вещества к поверхности электрода
2) Гетерогенный перенос электронов между веществом и поверхностью электрода (собственно электрохимическая реакция, стадия разряда-ионизации);
3) Отвод продуктов реакции, который зависит от природы продукта и может проявляться либо в его растворении в ртути с образованием амальгамы, либо в осаждении (электрокристаллизации) на поверхности электрода, либо в переносе в объем раствора.
При последующим увеличении потенциала наступает время, когда концентрация электроактивного вещества в приэлектродном слое становится равной нулю, а ток определяется скоростью его массопереноса, потому что все частицы вещества,, которые подступают к электроду из объема, немедленно разряжаются (это достигается в точке С на рис. 2).
Начиная с этого времени дальнейшее увеличение силы тока оказывается невозможным (участок СD на рис.2). В этом случае электрод переходит в состояние концентрационной поляризации. Ток, который протекает при этом в цепи, именуется предельным диффузионным током.
Единственным способом переноса электроактивного вещества является диффузия. Со временем предельный диффузионный ток должен уменьшаться, а толщина диффузионного слоя – увеличиваться [9].
4. Качественный полярографический анализ
Качественный полярографический анализ основан на сравнении значений полуволн, свойственных для отдельных соединений в определенных условиях [4. с.297].
Такой качественный анализ обладает некоторыми недостатками, которые свойственны практически любому иному физико-химическому методу анализа (не считая оптических методов). Эти недостатки обусловлены часто встречающейся схожестью значений потенциалов полуволны для разного рода веществ, а также относительно узким диапазоном потенциалов, где протекают различные электрохимические процессы, которые фиксируются с помощью полярографа. Недостатком является также влияние на
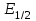 природы растворителя, фона и некоторых иных факторов.
природы растворителя, фона и некоторых иных факторов. Конечно, недостатки не лишают нам использовать полярографический метод для качественного анализа, тем не менее к результатам этого анализу следует подходить критически.
Как уже указывалось раннее, значения
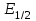 зависят от многих факторов, однако, зная общие закономерности влияния факторов на
зависят от многих факторов, однако, зная общие закономерности влияния факторов на 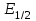 , мы можем все же использовать для целей качественного анализа величины потенциалов полуволн, полученные при полярографировании веществ в строго определенных условиях. На сегодняшнее время имеются справочники, которые содержат таблицы, показывающие значения
, мы можем все же использовать для целей качественного анализа величины потенциалов полуволн, полученные при полярографировании веществ в строго определенных условиях. На сегодняшнее время имеются справочники, которые содержат таблицы, показывающие значения 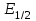 для большого числа органических веществ, с помощью которых можно оценивать по полярографическим данным качественный состав раствора [4, с.298].
для большого числа органических веществ, с помощью которых можно оценивать по полярографическим данным качественный состав раствора [4, с.298]. На практике установлено, что различные классы органических веществ образуют полярографические волны в определенных областях потенциалов, благодаря чему мы можем по значению потенциала полуволны на полярограмме сразу же судить о присутствии в нем органических соединений с определенными функциональными группами. В большинстве случаев эти данные имеют приближенное значение, поскольку на значение потенциала полуволны, кроме фона и природы функциональной группы, могут оказывать влияние и другие функциональные группы, которые имеются в молекуле исследуемого вещества, а также состав полярографируемого раствора, наличие в нем поверхностно-активных веществ, значение рН и другие факторы. Поэтому всегда нужно вместе с определением области потенциалов восстановления для уточнения природы вещества в растворе, дающего волну, использовать дополнительные условия, к примеру изучение влияния на полученные полярографические волны добавок некоторых реагентов, с которыми предполагаемые вещества могут взаимодействовать и тем самым изменять характер полярограмм. Например, при добавке димедона в раствор, содержащий формальдегид, волна формальдегида исчезает, а волны других альдегидов остаются неизменными.
Рассмотрим еще пример. Для определения альдегидных групп обычно применяют реактив Жерара, первичные амины, семикарбазиды, гидроксиламины. При добавлении этих веществ к альдегидам образуются полярографически активные азометиновые группы
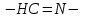 , восстановление которых чаще всего протекает при более положительных потенциалах, чем восстановление соответствующих карбонильных соединений, что связано с более низкой электроотрицательностью атома азота по сравнению с кислородом.
, восстановление которых чаще всего протекает при более положительных потенциалах, чем восстановление соответствующих карбонильных соединений, что связано с более низкой электроотрицательностью атома азота по сравнению с кислородом. В некоторых случаях, когда вещества не имеют полярографически активной группы и, следовательно, не образуют полярографических волн восстановления – в катодной – и окисления – в анодной – областях потенциалов, для выявления таких веществ также используются определенного рода химические превращения, которые приводят к образованию полярографически активных соединений с определенными значениями потенциалов полуволны.
Вторичные аминогруппы в результате реакции с азотистой кислотой образуют нитрозоамины, которые дают характерные полярографические волны.
Для того, чтобо выявить спиртовые группы, спирт хромовой кислоты окисляют и при полярографическом исследовании получают волны альдегидов. Финильная группа претерпевает нитрование смесью серной и азотной кислот и полярографически определяется по волне нитрогрупп.
Соединения с двойными и тройными связями, как правило, образуют полярографические волны только тогда, когда связи сопряжены с ароматическими системами. Но и в этом случае
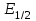 таких полярографических волн лежат в сильно отрицательной области. Пропускание этих соединений через бром приводит к получению бромпроизводных, которые восстанавливаются при более положительных потенциалах.
таких полярографических волн лежат в сильно отрицательной области. Пропускание этих соединений через бром приводит к получению бромпроизводных, которые восстанавливаются при более положительных потенциалах. Существуют способы, с помощью которых могут быть определены и другие функциональные группы полярографическим методом. В последнее время известное значение приобрел полярографический метод при установлении структуры органических веществ, а именно при нахождении положения определенных функциональных групп в молекулах органических соединений. Для такой цели используется связь между значениями
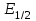 и σ-констант Гаммета или Тафта в определенном ряду соединений.
и σ-констант Гаммета или Тафта в определенном ряду соединений. 5. Количественный полярографический анализ
Количественный полярографический анализ основан на определении зависимости предельного тока от концентрации деполяризатора. Зависимость диффузного тока выражается уравнением Ильковича
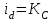 , исходя из которого, при прочих постоянных условиях величина предельного диффузного тока прямо пропорциональна концентрации исходного раствора –
, исходя из которого, при прочих постоянных условиях величина предельного диффузного тока прямо пропорциональна концентрации исходного раствора – 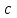 .
. Количественный полярографический анализ возможен тогда, когда концентрации растворенного вещества от
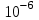 до
до 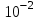 моль/л, впрочем, удобнее проводить полярографические определения при концентрациях от
моль/л, впрочем, удобнее проводить полярографические определения при концентрациях от 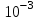 до
до 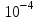 моль/л. В этом случае относительная погрешность полученных результатов будет составлять
моль/л. В этом случае относительная погрешность полученных результатов будет составлять 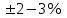 . Применение особых приемов дает возможность понизить нижний предел концентраций до
. Применение особых приемов дает возможность понизить нижний предел концентраций до 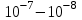 моль/л. Однако есть недостаток – уменьшается точность определений.
моль/л. Однако есть недостаток – уменьшается точность определений. Одним из самых важных вопросов при количественном анализе является учет остаточного тока, который является суммой тока заряжения и тока, обусловленного электродными реакциями присутствующих в растворе примесей. Данный учет проводится подобно холостой пробе в аналитической химии путем снятия полярограммы при отсутствии в растворе определяемого вещества: получаемая при этом кривая называется током фона. Отсчет высоты полярографической волны ведут от уровня фона при данном потенциале. Для расчета результатов при количественном полярографическом анализе используются:
а) метод калибровочного графика;
б) метод добавок;
в) расчётный метод
Метод калибровочной кривой (метод калибровочного графика) состоит в том, что при различных известных концентрациях исследуемого вещества получают ряд полярограмм в тех же условиях, которые фактически существуют при анализе. Сначала измеряют высоты волн, затем по полученным результатам строят график в координатах: величина предельного тока (высота волны) – концентрация исследуемого вещества.


