ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 08.02.2024
Просмотров: 112
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
ЛК50 и порогом однократного воздействия К мин.ост и определяется по формуле:
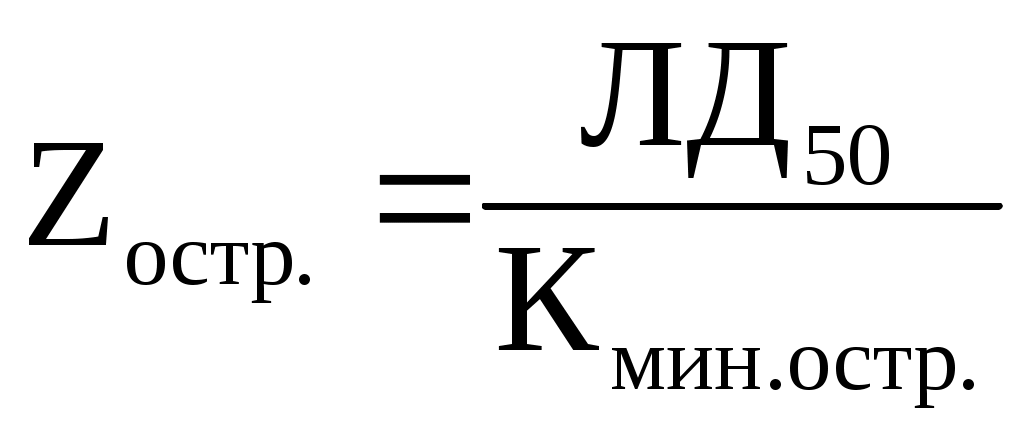 (8.1)
(8.1)
Понятно, что чем ближе друг к другу значения числителя и знаменателя, тем меньше отношение между ними и тем более опасным является данное вещество. Чем уже зона острого токсического действия, тем быстрее легкая интоксикация при увеличении дозы может перейти в отравление с летальным исходом.
Правда, эти значения могут оказаться близкими как для высокотоксичных, так и для малотоксичных веществ, вследствие чего значения Z оцениваются с указанием фактических границ токсичности.
Величина Zхрон. характеризует опасность хронического поступления (интоксикации): чем шире данная зона, тем выше опасность, поскольку при этом возрастает угроза накопления (т.е. кумуляции) вещества в организме. Это величина определяется как отношение
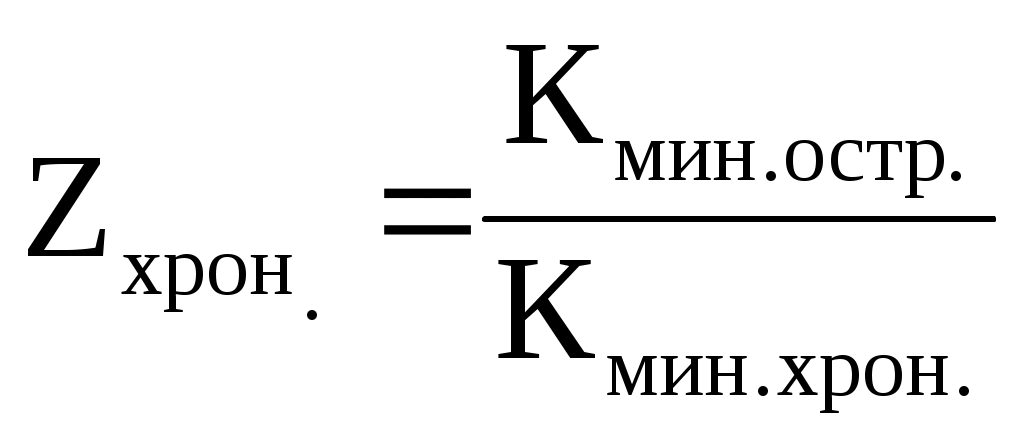 ( 8.2)
( 8.2)
Что касается КВИО, то этот показатель характеризует эффективную токсичность вещества и определяется как отношение его насыщенной концентрации в воздухе при температуре 200С (К20) к среднесмертельной ЛД50 :
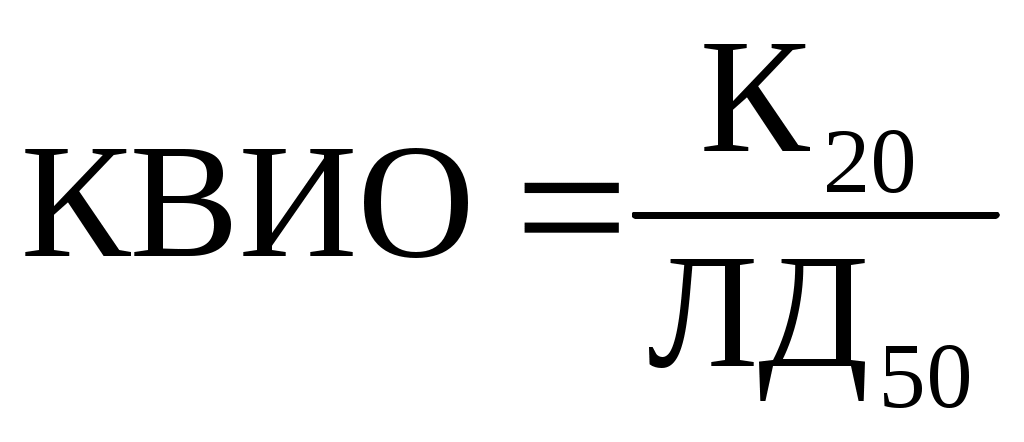 (8.3)
(8.3)
Естественно, что чем выше степень токсичности того или иного вещества, тем более жестокие требования предъявляются при работе с ним или к его присутствию в окружающей среде.
Для описания функциональной связи между эффектом токсичного вещества на организм и его концентрацией (зависимость «доза-эффект») предложены различные уравнения. Наиболее простым является уравнение Хабера:
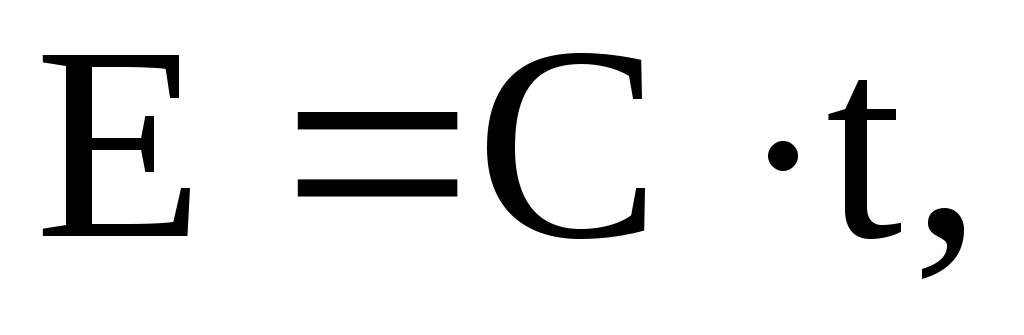 (8.4)
(8.4)
где Е – эффект токсичности, мг мин/м3
С – концентрация вещества, мг/м3,
t – время воздействия вещества, мин.
Уравнение Хабера применимо для ядов с кумулятивным действием. Для ядов, не обладающим кумулятивным эффектом, используется формула Майера:
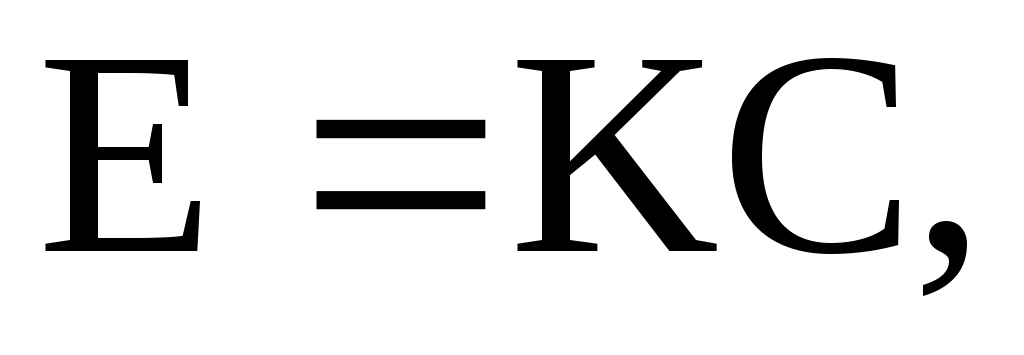 (8.5)
(8.5)
где К – константа, зависящая от свойств яда.
Под временем (экспозицией) понимают период, в течение которого организм находится под воздействием исследуемого фактора, в частности химического вещества. Отличия во времени реагирования на одно и то же вещество у разных тест-организмов будут отражать отличия в их чувствительности.
Таким образом, биологическое действие яда начинает проявляться с некоторой минимальной дозы (минимальной действующей концентрации) – порога, т.е. биологическая активность токсина определяется количеством молекул (ионов) способных вступить во взаимодействие с биоструктурами клетки и вызвать токсический эффект.
Полагают, что нижний предел биологической активности чужеродных соединений в организме (т.е. минимальная концентрация, необходимая для начала химического взаимодействия) составляет 7•1012 молекул на 1г биологической ткани. Для водных организмов это соответствует концентрации токсина в воде 10-8 г-моль/л или 104 атомов токсичных элементов на одну клетку (для канцерогенов этот показатель равен 1013…1017 атомов или молекул на одну клетку).
С превышением этого порога возрастает вероятность взаимодействия токсина с биохимическими структурами, а значит и опасность появления нарушений.
При определении токсической дозы исследуют (экспериментально) зависимость «эффект-доза», которую затем анализируют с помощью статистических методов. Величина токсической дозы зависит от способа введения вещества или пути его поступления в организм, от вида животных, возрастных, половых и индивидуальных различий, а также от конкретных условий воздействия вещества.
При внутривенном, внутримышечном, подкожном и пероральном (через рот) введении, а также при накожной аппликации токсичные дозы имеют размерности: мкг/кг, мг/кг, моль/кг и т.д. Иногда используют также токсичные дозы, отнесенные к единице поверхности тела: мг/м2, г/м2 и т.п. Это связано с тем, что подобные дозы некоторых веществ для разных лабораторных животных и человека различаются в меньшей степени, чем дозы, отнесенные к единице массы. Этим пользуются в ряде случаев для анализа видовой чувствительности и переноса данных с лабораторных животных на человека.
Пересчет доз из размерности мг/м2 в мг/кг проводят с использованием специальных таблиц и номограмм или по формуле, например:
ED50 (мг/м2)=K . ED50 (мг/кг), (8.6)
где К – коэффициент пересчета, который для стандартных лабораторных животных, как правило, определяется их массой – m: K=m
0,309.
Для характеристики токсичности при ингаляции обычно указывают концентрации паров или аэрозолей в воздухе (мг/м3,мг/л и т.п.) и время их воздействия. Иногда применяют соотношения объёмных единиц, имеющих преимущества безразмерных параметров (%, ppm , ррb), хотя они и не соответствуют рекомендациям ВОЗ и Международного Стандарта (ISO).
В американской литературе в качестве объёмных критериев используют величину ррm (parts per million), что соответствует 1 части на миллион, особенно для газов (1ppmоб =1 см3/м3), а иногда и в виде массовых величин для твердых веществ (1ppmмас =1 мг/кг). При очень малых концентрациях в воздухе пользуются данными в ppb, соответствующих 1:109 (1ppbоб =1мм3/м3). В США величина 109 носит наименование биллион, а в Европе – миллиард.
Для идеального газа при 298К (250С) и давлении 101,325 кПа перевод 1 ррm (об) в мг/м3 осуществляется согласно зависимости:
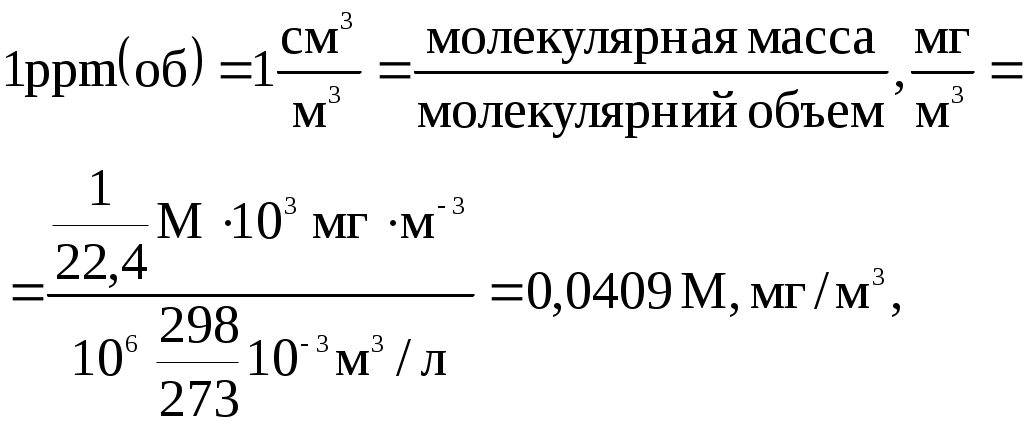
Получаем следующее уравнение для пересчёта:
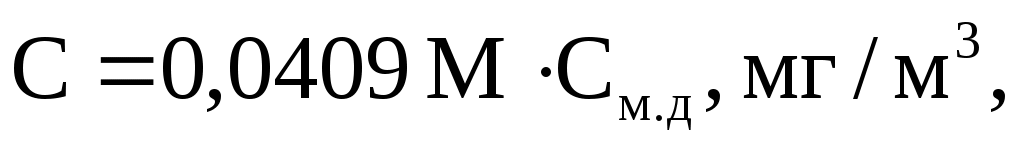 (8.7)
(8.7)
где С – концентрация примеси газа в воздухе, мг/м3;
См.д. – та же концентрация, в единицах ppm (млн-1);
М - молекулярная масса газа.
С учетом температуры и давления уравнение (8.7) приобретает вид:
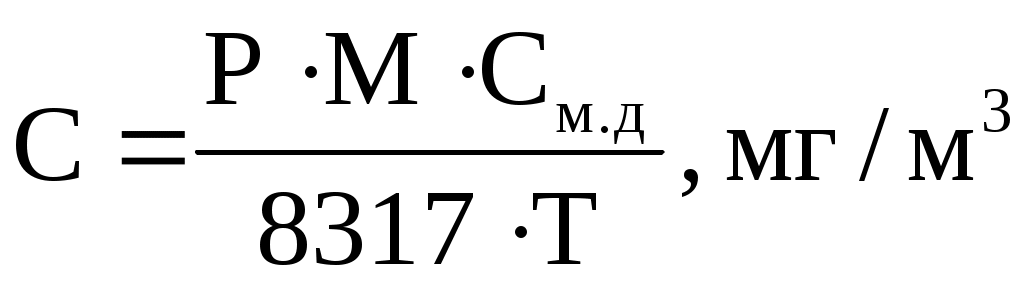
где Р – давление газа, Па; Т – температура, К.
8.1.2. Классификация веществ по токсичности.
Первые попытки создания классификации химических веществ по токсичности базировались на учете скорости развития острого токсического эффекта и степени его выраженности. С развитием широких исследований по разработке ПДК появились классификации химических веществ, основанные на учете величин средне смертельных доз и концентраций.
В настоящее время в промышленной токсикологии наибольшее распространение получила классификация, предусматривающая 4 класса вредных веществ (иногда вместо термина «опасные» используют термин «токсичные») (табл. 8.1).
Эффект токсического действия различных веществ зависит от количества (дозы) вещества, попавшего в организм, его физических свойств, длительности поступления, химизма взаимодействия с биологическими средами и тканями, пола, возраста, индивидуальной чувствительности, путей поступления, распределения и выведения из организма.
Яды, наряду с общей, обладают избирательной токсичностью, т.е. они представляют наибольшую опасность для определенного органа или системы. В токсикологии выделяют следующие группы ядов: сердечные, нервные, печеночные, почечные, кровяные, легочные.
Таблица 8.1–Классификация вредных веществ по степени токсичности
и опасности
Первые три показатели – характеризуют степень токсичности, а три последние – степень опасности вещества.
Классификация химических веществ по степени их токсичности и, особенно, опасности играет важную роль в решении проблем санитарной регламентации при разработке ПДК, если время контакта с токсикантом заранее установлено. Классы токсичности ряда соединений приведены в приложении 1.
Среди многих механизмов реализации токсичности ксенобиотиков в токсикологии выделяют два, как наиболее универсальные:
1. необратимое связывание токсина с биомолекулами различных клеточных и внутри клеточных структур;
2. окислительный стресс, сопровождающийся активизацией не ферментативного свободно - радикального окисления и перекисного окисления лепидов.
Многие ксенобиотики способны «включать» одновременно несколько механизмов токсического действия. И в том и в другом случае происходит, в конечном счете, нарушение обмена веществ, поведенческих реакций организма, его энергетического баланса, гибель клеточных структур и жизнеобеспечивающих органов.
Для проникновения в клетку токсины используют различные «приемы»: «дырявят» мембраны, обманывают клетку, маскируясь под жизненно необходимые для неё соединения и элементы, связывают и выводят из организма жизненно важные микроэлементы и т.д.
Так, никотин воспринимается нервными клетками как ацетилхолин – вещество-медиатор, которое после проведения нервного импульса легко расщепляется ферментом ацетилхолинэстеразой (тем самым снимается длительное раздражение ацетилхолином нервных окончаний). Однако никотин не является медиатором (а это значит, что он не разрушается ацетилхолинэстеразой), поэтому подобная ошибка выводит нервные клетки из строя вследствие длительного непрерывного их раздражения.
Другие ксенобиотики действуют на нервные окончания, используя особенности конфигурации своих молекул. Так, молекула диоксина, имеющая форм прямоугольника размером 3...10 Ǻ, удивительно точно и надолго «вписывается» в рецепторы живых организмов.
Диоксины способны подавлять и искажать жизненные функции организма. При этом в малых количествах они могут «не убивать» человека годами, но, накопившись в организме, они дают о себе знать многими болезнями, в том числе – злокачественными новообразованиями, врожденными аномалиями развития, уродствами и различными мутациями. Кроме того, диоксины проявляют свойства иммуносупрессора, т.е. при интоксикации организма развивается иммунодефицит. Существует мнение, что диоксины являются одной из причин возникновения СПИДа.
Вредное действие ряда ксенобиотиков (некоторые пестициды, четыреххлористый углерод и др.) на организм человека обусловлено высокой токсичностью промежуточных и конечных продуктов их превращений, в первую очередь, активными окислителями – свободными радикалами и перекисными соединениями.
Так, оксиды азота вызывают воспаленные верхних дыхательных путей, фиброзный бронхит, токсикозы, врожденные аномалии, сердечную недостаточность, нервные расстройства, рак. Диоксид серы инициирует бронхиты, пневмонию, дистрофические изменения, в печени, почках и сердце, а в сочетании с бензпиреном – усиливает канцерогенное действие. Присутствие оксида углерода ведет к нарушению жирового, углеводного и витаминного баланса, поражению центральной нервной системы, карбоксигемоглобинемии. Нарушение функции организма наступает при содержании в крови 10…20% карбоксигемоглобина, смерть – при 60%. У жителей крупных промышленных городов уровень карбоксигемоглобина в крови варьирует от 0,8…3,7% (у некурящих) до 1,2…9% (у курящих). Сходное заболевание (метгемоглобинемию) вызывают нитриты и нитраты.
Понятно, что чем ближе друг к другу значения числителя и знаменателя, тем меньше отношение между ними и тем более опасным является данное вещество. Чем уже зона острого токсического действия, тем быстрее легкая интоксикация при увеличении дозы может перейти в отравление с летальным исходом.
Правда, эти значения могут оказаться близкими как для высокотоксичных, так и для малотоксичных веществ, вследствие чего значения Z оцениваются с указанием фактических границ токсичности.
Величина Zхрон. характеризует опасность хронического поступления (интоксикации): чем шире данная зона, тем выше опасность, поскольку при этом возрастает угроза накопления (т.е. кумуляции) вещества в организме. Это величина определяется как отношение
Что касается КВИО, то этот показатель характеризует эффективную токсичность вещества и определяется как отношение его насыщенной концентрации в воздухе при температуре 200С (К20) к среднесмертельной ЛД50 :
Естественно, что чем выше степень токсичности того или иного вещества, тем более жестокие требования предъявляются при работе с ним или к его присутствию в окружающей среде.
Для описания функциональной связи между эффектом токсичного вещества на организм и его концентрацией (зависимость «доза-эффект») предложены различные уравнения. Наиболее простым является уравнение Хабера:
где Е – эффект токсичности, мг мин/м3
С – концентрация вещества, мг/м3,
t – время воздействия вещества, мин.
Уравнение Хабера применимо для ядов с кумулятивным действием. Для ядов, не обладающим кумулятивным эффектом, используется формула Майера:
где К – константа, зависящая от свойств яда.
Под временем (экспозицией) понимают период, в течение которого организм находится под воздействием исследуемого фактора, в частности химического вещества. Отличия во времени реагирования на одно и то же вещество у разных тест-организмов будут отражать отличия в их чувствительности.
Таким образом, биологическое действие яда начинает проявляться с некоторой минимальной дозы (минимальной действующей концентрации) – порога, т.е. биологическая активность токсина определяется количеством молекул (ионов) способных вступить во взаимодействие с биоструктурами клетки и вызвать токсический эффект.
Полагают, что нижний предел биологической активности чужеродных соединений в организме (т.е. минимальная концентрация, необходимая для начала химического взаимодействия) составляет 7•1012 молекул на 1г биологической ткани. Для водных организмов это соответствует концентрации токсина в воде 10-8 г-моль/л или 104 атомов токсичных элементов на одну клетку (для канцерогенов этот показатель равен 1013…1017 атомов или молекул на одну клетку).
С превышением этого порога возрастает вероятность взаимодействия токсина с биохимическими структурами, а значит и опасность появления нарушений.
При определении токсической дозы исследуют (экспериментально) зависимость «эффект-доза», которую затем анализируют с помощью статистических методов. Величина токсической дозы зависит от способа введения вещества или пути его поступления в организм, от вида животных, возрастных, половых и индивидуальных различий, а также от конкретных условий воздействия вещества.
При внутривенном, внутримышечном, подкожном и пероральном (через рот) введении, а также при накожной аппликации токсичные дозы имеют размерности: мкг/кг, мг/кг, моль/кг и т.д. Иногда используют также токсичные дозы, отнесенные к единице поверхности тела: мг/м2, г/м2 и т.п. Это связано с тем, что подобные дозы некоторых веществ для разных лабораторных животных и человека различаются в меньшей степени, чем дозы, отнесенные к единице массы. Этим пользуются в ряде случаев для анализа видовой чувствительности и переноса данных с лабораторных животных на человека.
Пересчет доз из размерности мг/м2 в мг/кг проводят с использованием специальных таблиц и номограмм или по формуле, например:
ED50 (мг/м2)=K . ED50 (мг/кг), (8.6)
где К – коэффициент пересчета, который для стандартных лабораторных животных, как правило, определяется их массой – m: K=m
0,309.
Для характеристики токсичности при ингаляции обычно указывают концентрации паров или аэрозолей в воздухе (мг/м3,мг/л и т.п.) и время их воздействия. Иногда применяют соотношения объёмных единиц, имеющих преимущества безразмерных параметров (%, ppm , ррb), хотя они и не соответствуют рекомендациям ВОЗ и Международного Стандарта (ISO).
В американской литературе в качестве объёмных критериев используют величину ррm (parts per million), что соответствует 1 части на миллион, особенно для газов (1ppmоб =1 см3/м3), а иногда и в виде массовых величин для твердых веществ (1ppmмас =1 мг/кг). При очень малых концентрациях в воздухе пользуются данными в ppb, соответствующих 1:109 (1ppbоб =1мм3/м3). В США величина 109 носит наименование биллион, а в Европе – миллиард.
Для идеального газа при 298К (250С) и давлении 101,325 кПа перевод 1 ррm (об) в мг/м3 осуществляется согласно зависимости:
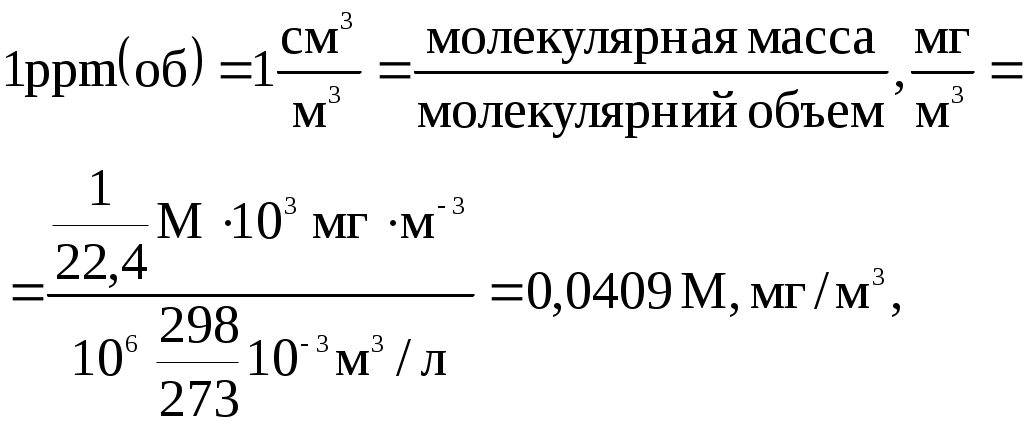
Получаем следующее уравнение для пересчёта:
где С – концентрация примеси газа в воздухе, мг/м3;
См.д. – та же концентрация, в единицах ppm (млн-1);
М - молекулярная масса газа.
С учетом температуры и давления уравнение (8.7) приобретает вид:
где Р – давление газа, Па; Т – температура, К.
8.1.2. Классификация веществ по токсичности.
Первые попытки создания классификации химических веществ по токсичности базировались на учете скорости развития острого токсического эффекта и степени его выраженности. С развитием широких исследований по разработке ПДК появились классификации химических веществ, основанные на учете величин средне смертельных доз и концентраций.
В настоящее время в промышленной токсикологии наибольшее распространение получила классификация, предусматривающая 4 класса вредных веществ (иногда вместо термина «опасные» используют термин «токсичные») (табл. 8.1).
Эффект токсического действия различных веществ зависит от количества (дозы) вещества, попавшего в организм, его физических свойств, длительности поступления, химизма взаимодействия с биологическими средами и тканями, пола, возраста, индивидуальной чувствительности, путей поступления, распределения и выведения из организма.
Яды, наряду с общей, обладают избирательной токсичностью, т.е. они представляют наибольшую опасность для определенного органа или системы. В токсикологии выделяют следующие группы ядов: сердечные, нервные, печеночные, почечные, кровяные, легочные.
Таблица 8.1–Классификация вредных веществ по степени токсичности
и опасности
| Показатели | Классы токсичности (опасности) | |||
| 1 чрезвычайно токсичные | 2 высоко- токсичные | 3 умеренно токсичные | 4 мало- токсичные | |
| ПДКр.з., мг/м3 | <0,1 | 0,1-1 | 1,1-10 | >10 |
| ЛД50 при введении внутрь, мг/м3 | <15 | 15-150 | 151-1500 | >1500 |
| Среднесмертельная кон- центр-ия в воздухе, мг/м3 | <500 | 500-5000 | 5001-50000 | >50000 |
| Zостр. | <6 | 6-18 | 18,1-54 | >54 |
| Zхрон. | >10 | 10-5 | 4,9-2,5 | <2,5 |
| КВИО | >300 | 300-30 | 2,9-3 | <3 |
Первые три показатели – характеризуют степень токсичности, а три последние – степень опасности вещества.
Классификация химических веществ по степени их токсичности и, особенно, опасности играет важную роль в решении проблем санитарной регламентации при разработке ПДК, если время контакта с токсикантом заранее установлено. Классы токсичности ряда соединений приведены в приложении 1.
Среди многих механизмов реализации токсичности ксенобиотиков в токсикологии выделяют два, как наиболее универсальные:
1. необратимое связывание токсина с биомолекулами различных клеточных и внутри клеточных структур;
2. окислительный стресс, сопровождающийся активизацией не ферментативного свободно - радикального окисления и перекисного окисления лепидов.
Многие ксенобиотики способны «включать» одновременно несколько механизмов токсического действия. И в том и в другом случае происходит, в конечном счете, нарушение обмена веществ, поведенческих реакций организма, его энергетического баланса, гибель клеточных структур и жизнеобеспечивающих органов.
Для проникновения в клетку токсины используют различные «приемы»: «дырявят» мембраны, обманывают клетку, маскируясь под жизненно необходимые для неё соединения и элементы, связывают и выводят из организма жизненно важные микроэлементы и т.д.
Так, никотин воспринимается нервными клетками как ацетилхолин – вещество-медиатор, которое после проведения нервного импульса легко расщепляется ферментом ацетилхолинэстеразой (тем самым снимается длительное раздражение ацетилхолином нервных окончаний). Однако никотин не является медиатором (а это значит, что он не разрушается ацетилхолинэстеразой), поэтому подобная ошибка выводит нервные клетки из строя вследствие длительного непрерывного их раздражения.
Другие ксенобиотики действуют на нервные окончания, используя особенности конфигурации своих молекул. Так, молекула диоксина, имеющая форм прямоугольника размером 3...10 Ǻ, удивительно точно и надолго «вписывается» в рецепторы живых организмов.
Диоксины способны подавлять и искажать жизненные функции организма. При этом в малых количествах они могут «не убивать» человека годами, но, накопившись в организме, они дают о себе знать многими болезнями, в том числе – злокачественными новообразованиями, врожденными аномалиями развития, уродствами и различными мутациями. Кроме того, диоксины проявляют свойства иммуносупрессора, т.е. при интоксикации организма развивается иммунодефицит. Существует мнение, что диоксины являются одной из причин возникновения СПИДа.
Вредное действие ряда ксенобиотиков (некоторые пестициды, четыреххлористый углерод и др.) на организм человека обусловлено высокой токсичностью промежуточных и конечных продуктов их превращений, в первую очередь, активными окислителями – свободными радикалами и перекисными соединениями.
Так, оксиды азота вызывают воспаленные верхних дыхательных путей, фиброзный бронхит, токсикозы, врожденные аномалии, сердечную недостаточность, нервные расстройства, рак. Диоксид серы инициирует бронхиты, пневмонию, дистрофические изменения, в печени, почках и сердце, а в сочетании с бензпиреном – усиливает канцерогенное действие. Присутствие оксида углерода ведет к нарушению жирового, углеводного и витаминного баланса, поражению центральной нервной системы, карбоксигемоглобинемии. Нарушение функции организма наступает при содержании в крови 10…20% карбоксигемоглобина, смерть – при 60%. У жителей крупных промышленных городов уровень карбоксигемоглобина в крови варьирует от 0,8…3,7% (у некурящих) до 1,2…9% (у курящих). Сходное заболевание (метгемоглобинемию) вызывают нитриты и нитраты.


