Файл: Химические элементы в природе круговорот и миграция.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.02.2024
Просмотров: 17
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ В ПРИРОДЕ – КРУГОВОРОТ И МИГРАЦИЯ.Между литосферой, гидросферой, атмосферой и живыми организмами Земли постоянно происходит обмен химическими элементами. Этот процесс имеет циклический характер: переместившись из одной сферы в другую, элементы вновь возвращаются в первоначальное состояние. Круговорот элементов имел место в течение всей истории Земли, насчитывающей 4,5 млрд. лет.
Гигантские массы химических веществ переносятся водами Мирового океана. В первую очередь это относится к растворенным газам – диоксиду углерода, кислороду, азоту. Холодная вода высоких широт растворяет газы атмосферы. Поступая с океаническими течениями в тропический пояс, она их выделяет, так как растворимость газов при нагревании уменьшается. Поглощение и выделение газов происходит также при смене теплых и холодных сезонов года.
Огромное влияние на природные циклы некоторых элементов оказало появление жизни на планете. Это, в первую очередь, относится к круговороту главных элементов органического вещества – углерода, водорода и кислорода, а также таких жизненно важных элементов как азот, сера и фосфор. Живые организмы оказывают влияние и на круговорот многих металлических элементов. Несмотря на то, что суммарная масса живых организмов Земли меньше массы земной коры в миллионы раз, растения и животные играют важнейшую роль в перемещении химических элементов.
Деятельность человека также оказывает влияние на круговорот элементов. Особенно заметным оно стало в последнее столетие. При рассмотрении химических аспектов глобальных изменений в круговоротах химических элементов следует учитывать не только изменения в природных круговоротах за счет добавления или удаления присутствующих в них химических веществ в результате обычных циклических и/или вызванных человеком воздействий, но и поступление в окружающую среду химических веществ, ранее не существовавших в природе. Рассмотрим несколько наиболее важных примеров циклического перемещения и миграции химических элементов.
Углерод
– основной элемент жизни – содержится в атмосфере в виде диоксида углерода. В океане и пресных водах Земли углерод находится в двух главных формах: в составе органического вещества и в составе взаимосвязанных неорганических частиц: гидрокарбонат-иона НСО3–, карбонат иона СО32– и растворенного диоксида углерода СО
2. Большое количество углерода сосредоточено в виде органических соединений в животных и растениях. Много «неживого» органического вещества имеется в почве. Углерод литосферы содержится также в карбонатных минералах (известняк, доломит, мел, мрамор). Часть углерода входит в состав нефти, каменного угля и природного газа.
Связующим звеном в природном круговороте углерода является диоксид углерода (рис. 1).
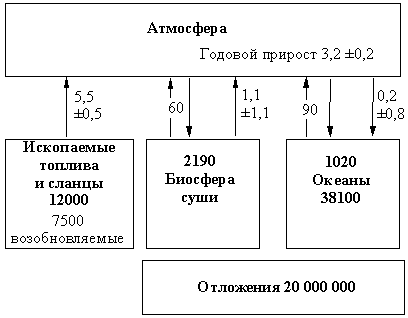
Рис. 1. УПРОЩЕННАЯ СХЕМА глобального цикла углерода. Числа в рамках отражают размеры резервуаров в миллиардах тонн – гигатоннах (Гт). Стрелки показывают потоки, а связанные с ними числа выражены в Гт/год.
Самыми крупными резервуарами углерода являются морские отложения и осадочные породы на суше. Однако бoльшая часть этого вещества не взаимодействует с атмосферой, а подвергается круговороту через твердую часть Земли в геологических временных масштабах. Поэтому эти резервуары играют лишь второстепенную роль в сравнительно быстром цикле углерода, протекающем с участием атмосферы. Следующим по величине резервуаром является морская вода. Но и здесь глубинная часть океанов, где содержится основное количество углерода, не взаимодействует с атмосферой так быстро, как их поверхность. Самыми маленькими резервуарами являются биосфера суши и атмосфера. Именно небольшой размер последнего резервуара делает его чувствительным даже к незначительным изменениям процентного содержания углерода в других (больших) резервуарах, например, при сжигании ископаемых топлив.
Современный глобальный цикл углерода состоит из двух меньших циклов. Первый из них заключается в связывании диоксида углерода в ходе фотосинтеза и новом образовании его в процессе жизнедеятельности растений и животных, а также при разложении органических остатков. Второй цикл обусловлен взаимодействием диоксида углерода атмосферы и природных вод:
СО2 + Н2О
Н2СО3
НСО3–
СО32– + Са2+ = СаСО3Ї
В последнее столетие в углеродный цикл существенные изменения внесла хозяйственная деятельность человека. Сжигание ископаемого топлива – угля, нефти и газа – привело к увеличению поступления диоксида углерода в атмосферу. Это не очень сильно влияет на распределение масс углерода между оболочками Земли, но может иметь серьезные последствия из-за усиления парникового эффекта. См. также УГЛЕРОД.
Кислород
на Земле содержится, в основном, в литосфере в виде диоксида кремния и силикатов. Кроме того, кислород есть в составе воды, образующей гидросферу. В атмосфере кислород находится в молекулярном виде. Он является продуктом процессов жизнедеятельности растений и в то же время одним из основных условий существования жизни на Земле. Образование свободного кислорода связано со световой энергией Солнца. Исходным сырьем для образования кислорода служит вода. Почти весь свободный кислород на Земле – это результат реакции фотосинтеза органического вещества из воды и диоксида углерода. Некоторое количество кислорода образуется при разложении воды в верхних слоях атмосферы. Кислород входит в состав многих органических соединений. Между живыми организмами и атмосферой происходит постоянный обмен кислородом.
Несмотря на выделение кислорода зелеными растениями, его содержание в атмосфере не увеличивается. Одновременно с фотосинтезом происходит разложение органического вещества, при этом поглощается практически весь выделившийся кислород. Часть кислорода расходуется на окисление неорганических веществ. Незначительное количество атмосферного кислорода участвует в цикле образования и разрушения озона. См. такжеКИСЛОРОД.
Водород
на Земле находится, преимущественно, в гидросфере в составе воды. Содержание его в литосфере и атмосфере сравнительно невелико. Он входит также в состав органических веществ. Огромные массы водорода, наряду с кислородом, участвуют в круговороте воды – одном из наиболее мощных циклических процессов на планете.
Особенностью водорода является его способность (наряду с гелием) уходить из поля тяготения Земли благодаря своей малой атомной массе. Эти потери компенсируются выделением водорода из мантии. Молекулярный водород поступает в атмосферу Земли в результате вулканической деятельности, его выделяют также некоторые бактерии. После появления на нашей планете живых организмов водород стал связываться в органическом веществе.
См. также ВОДОРОД.
Азот,
вследствие исключительной прочности молекулы N2, почти полностью сосредоточен в атмосфере. Часть газообразного азота растворена в природных водах, которые содержат и растворенные азотсодержащие органические вещества и неорганические ионы: катион аммония, нитрит-ион и нитрат-ион. Поскольку азот не образует нерастворимых солей, он только в редких случаях накапливается в литосфере. Так, в южноамериканской пустыне Атакама есть скопления нитрата натрия, который, несмотря на высокую растворимость в воде, сохраняется благодаря исключительно сухому климату.
Слово «азот» буквально означает «безжизненный», поскольку он не поддерживает дыхание. Однако этот элемент является обязательной составной частью белков. Поэтому азот в значительном количестве содержится в живых организмах и «мертвом» органическом веществе. Азот непрерывно перемещается между атмосферой, океаном, живыми организмами и почвой.
В атмосфере под действием электрических разрядов азот переходит сначала в монооксид азота, а затем в диоксид азота. Влага воздуха и кислород превращают диоксид азота в азотную кислоту
4NO2 + 2H2O + O2 = 4HNO3
Соединения азота легко растворяются в атмосферных осадках и попадают на поверхность Земли.
Большое значение в связывании атмосферного азота имеет жизнедеятельность клубеньковых бактерий, обитающих на корнях бобовых растений. Ферменты этих бактерий превращают молекулярный азот в соединения, которые затем усваиваются растениями. Из растений связанный азот поступает в организмы животных, в основном, в виде аминокислот и белков. После гибели живых организмов органические вещества превращаются в неорганические соединения, снова усваиваемые растениями. Часть азота в почвах превращается в молекулярный азот и переходит в атмосферу. Молекулярный азот образуется также при полном окислении органических веществ.
Соединения азота попадают в атмосферу с выбросами промышленных предприятий и транспорта, а в природные воды – с бытовыми и промышленными отходами.
Слишком большое количество растворимых соединений азота в почве приводит к росту их содержания в продуктах питания и питьевой воде, это может стать причиной серьезных заболеваний. Соединения азота накапливаются в водоемах и вызывают зарастание озер и водохранилищ. Пока подобные явления наблюдаются лишь в отдельных районах, где в окружающую среду попадает много соединений азота. В целом же природа пока справляется с тем количеством связанного азота, которое производится человеком.

См. также АЗОТ.
Сера
содержится в атмосфере в небольших количествах, в основном, в виде сероводорода и диоксида серы. Довольно много этого элемента (в виде сульфат-ионов) находится в гидросфере. В литосфере сера встречается в виде простого вещества (самородная сера) и в составе многочисленных минералов – сульфидов и сульфатов металлов. Кроме того, соединения серы есть в углях, сланцах, нефти, природном газе. Сера входит в состав многих белков, поэтому она всегда содержится в организмах животных и растений.
Выделяясь из глубин Земли, газообразные соединения серы (преимущественно диоксид серы и сероводород) растворяются в подземных водах. Здесь они образуют малорастворимые сульфиды (главным образом пирит – дисульфид железа FeS2) и сульфаты (в частности, сульфат кальция CaSO4). Образуется также самородная сера:
2H2S + SO2 = 3S + 2H2O
Газообразные соединения серы попадают в почву, атмосферу и Мировой океан, где их поглощают серные бактерии. Поглощение соединений серы бактериями происходит и в почве.
Малорастворимые сульфиды, содержащиеся в горных породах, в результате жизнедеятельности некоторых бактерий частично окисляются, превращаясь в легко растворимые сульфаты:
FeS + 2O2 = FeSO4
Водорастворимые сульфаты выносятся с поверхности суши с речным стоком, поставляя сульфат-ионы в Мировой океан.
В результате активного связывания серы в земной коре, гидросфере и живых организмах, содержание сероводорода и диоксида серы в атмосфере мало и непостоянно. Под действием кислорода и озона эти вещества постепенно превращаются в серную кислоту:
2SO2 + О2
SO2 + О3 = SО3 + О2
SО3+ H2О = H2SO4
H2S + 2О3 = H2SO4 + О2
Серная кислота возвращается на землю с атмосферными осадками
Хозяйственная деятельность людей приводит к увеличению содержания соединений серы в атмосфере и гидросфере. В результате изменений в методах животноводства и земледелия (выпас, вспашка, мелиорация) увеличились выбросы серосодержащих соединений в виде пыли. Еще больше серы попадает в атмосферу в форме диоксида серы при обжиге сульфидных руд. Это, в свою очередь, вызывает увеличение потока серы, попадающей из атмосферы в океаны и на поверхность суши. Природные воды загрязняются также удобрениями с полей и стоками промышленных предприятий.

