ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 28.04.2024
Просмотров: 25
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
| ски  | «С.Ж. АСФЕНДИЯРОВ АТЫНДАҒЫ ҚАЗАҚ ҰЛТТЫҚ МЕДИЦИНА УНИВЕРСИТЕТІ» КЕАҚ НАО «КАЗАХСКИЙ НАЦИОНАЛЬНЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ ИМЕНИ С.Д. АСФЕНДИЯРОВА» | ||
| Химия кафедрасы | Тест тапсырмалары | . | |
| | |||
«Физикалық химия» пәнінен 6В07201 - «Фармацевтикалық өндіріс технологиясы» мамандығының студенттеріне арналған ТЕСТ ТАПСЫРМАЛАРЫ
2022-2023 оқу жылы
-
Химиялық термодинамика зерттейді:-
химиялық энергияның электрлік, жылу, механикалық, беттік және тағы басқа энергия түрлеріне айналу заңдылықтарын -
химиялық реакцияның жылдамдықтарын -
химиялық процестердің өту механизмін -
жеке заттардың химиялық қасиетін -
тепе - теңдіксіз жүйелерді
-
-
Ашық термодинамикалық жүйе:-
қоршаған ортамен массамен де энергиямен де алмасады -
қоршаған ортамен энергиямен алмаспайды -
қоршаған ортамен массамен де, энергиямен де алмаспайды -
қоршаған ортамен энергиямен алмасады, массамен алмаспайды -
қоршаған ортамен массамен алмасады, энергиямен алмаспайды
-
-
Гетерогенді жүйе:-
екі және одан да көп фазадан тұрады -
әрбір нүктеде қасиеті бірдей болады -
біртекті -
бірфазалы -
бір немесе бірнеше беттік бөліну болмайды
-
-
Гомогенді жүйеде фаза саны Ф:-
Ф=0 -
Ф=1 -
Ф >1 -
Ф= -2 -
Ф >2
-
-
Гетерогенді жүйеде фаза саны Ф:-
Ф =0 -
Ф =1 -
Ф >1 -
Ф<0 -
Ф<1
-
-
Гомогенді термодинамикалық жүйе:
1) бірнеше фазадан тұрады
-
жүйе ішінде беттік бөліну болады -
бір фазадан тұрады және әртүрлі нүктеде қасиеті бірдей болады -
әртүрлі нүктеде қасиеттері әртүрлі болады -
біртекті емес
-
Термодинамикалық параметрлер ішінен термодинамикалық функцияны таңда-
m -
V -
Н -
Р -
С
-
-
Интенсивті термодинамикалық параметрді таңда:-
m -
n -
C -
U -
V
-
-
Тек экстенсивті термодинамикалық параметрлері бар жауапты таңда-
Т, m, Н, S, U -
m, V,T,G,V -
U, S, F, р, С -
C,V, p,T, m -
m, V, U, Н, О
-
-
Келесі термодинамикалық параметрді тікелей өлшеуге болады-
масса -
энтальпия -
ішкі энергия -
энтропия -
Гиббс энергиясы
-
-
Келтірілген термодинамикалық жүйелерден гетерогенді жүйені таңда-
кристалдық тұз -
қанттың судағы қанықпаған ерітіндісі -
натрий хлоридінің судағы қанықпаған ерітіндісі -
натрий хлоридінің судағы сулы ерітіндісі және тұнба -
<сұйық су-мұз> жүйесі
-
-
Жабық термодинамикалық жүйені таңда-
адам -
өсімдік -
суыған тас -
әлем -
жасуша
-
-
Ашық термодинамикалық жүйені таңда-
суыған пеш -
суы бар термос -
Дьюар ыдысындағы сұйықтық -
өсімдік -
жабық ыдыстағы натрий хлоридінің ерітіндісі
-
-
Тікелей өлшенетін термодинамикалық жүйенің параметрін ата-
интенсивті -
экстенсивті -
тепе - теңдіктегі -
негізгі -
күй функциясы
-
-
Тікелей өлшенбейтін термодинамикалық жүйенің параметрін көрсет-
интенсивті -
экстенсивті -
тепе - теңдіктегі -
негізгі -
күй функциясы
-
-
Адам термодинамикалық жүйе ретінде-
гомогенді -
гетерогенді, ашық -
монофазалы -
жабық -
оқшауланған
-
-
Эндотермиялық реакция үшін
-
Q>0 -
H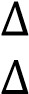 =0
=0 -
H<0 -
Q<0,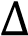 Н>0
Н>0 -
 S=0
S=0
-
Экзотермиялық реакция үшін-
Q>0, Н<0
Н<0 -
 H=0
H=0 -
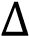 S=0
S=0 -
Q<0
-
5)
-
Термодинамиканың бірінші заңының математикалық өрнегі-
Q = U+A
= U+A -
Q = U∙p V
V -
Q = U - p
U - p V
V -
Q =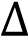 U - A
U - A -
Q = U + p
U + p A
A
-
-
Гесстің термохимиялық заңының ең маңызды салдарының бірі, химиялық реакцияның жылу эффектісін анықтайды ...-
термохимиялық реакция теңдеуінің стехиометриялық коэффициенттерін ескере отырып, реакция өнімнің түзілу жылуларының қосындысынан реакцияның бастапқы зат түзілу жылуларының қосындысының айырымы -
реакция бастапқы заттардың түзілу жылуларының қосындысынан өнімнің түзілу жылуларының қосындысының айырымы -
бастапқы заттардың түзілу жылуларының қосындысы -
реакция өнімдерінің түзілу жылуларының қосындысы 5) реакция өнімдерінің түзілу жылуларының айырымы
-
-
Реакцияның жылу эффектісі бастапқы заттардың және соңғы өнімдердің табиғаты мен күйіне байланысты, бірақ реакция жолына тәуелді емес. Заңның авторын көрсет 1) Кирхгофф заңы
-
Авогадро заңы -
Гесс заңы -
Фарадей заңы -
Массалар әрекеттесу заңы
-
А+В=2АВ реакциясының түзілу жылулары А=5 кДж/моль, В=10 кДж/моль, АВ=20 кДж/моль белгілі болса, реакцияның жылу эффектісі нешеге тең болады?
1) 25
-
-25 -
5 -
-5 -
10
-
А+В=2АВ реакциясының жану жылулары А=5 кДж/моль, В=10 кДж/моль, АВ=20 кДж/моль тең болса, реакцияның жылу эффектісі нешеге тең болады?-
25 -
-25 -
5 -
-5 -
10
-
-
Идеал газдар үшін Ср мен Сv арасындағы айырым нешеге тең?-
8,314 Дж/мольК -
9,3 Дж/мольК -
22,3 Дж/мольК
-
-
0 -
белгілі бір газ түрінің табиғатына байланысты
-
5 л көлемді метр кубпен өрнекте (м3)-
510-3 -
5103 -
510-6 -
5106 5) 510-2
-
-
Көлемі 3 сантиметр куб. Көлемді метр кубпен өрнекте (м3)-
310-3 -
3103 -
310-6 -
3106 -
310-2
-
-
Процестің жұмысы 15 Дж, ішкі энергиясы 5 Дж тең болса, жылу мөлшерінің мәні қанша болады?-
20 Дж -
10 Дж -
-10 Дж -
-20 Дж -
30Дж
-
-
Гиббстің бос энергиясын анықтайтын теңдеуді көрсет:-
G = ∆H - T∆S -
∆G = T∆S -
∆G = ∆U - T∆S -
∆G = ∆H + T∆S -
∆G = ∆U + T∆S
-
-
∆G = ∆H - T∆S теңдеуіндегі T∆S шамасы нені сипаттайды-
жүйенің бос энергиясын -
жүйенің байланысқан энергиясын -
изобаралық-изотермиялық потенциал -
изохоралық-изотермиялық потенциал -
Гельмгольц энергиясын
-
-
Өлшем бірлігі Джоуль болатын шаманы көрсет-
көлем -
температура -
жылу мөлшері -
жылусыйымдылық -
энтропия
-
-
Жылусыйымдылықтың өлшем бірлігін көрсет-
Дж/моль -
Дж/мольК -
Дж/г -
4) Дж/К
-
5) Дж
-
Келтірілген заттардың қайсысының түзілу жылуы нөлге тең болады?-
С2Н4 -
СО2 -
СН4 -
СО
-
5) Н2
-
∆S>0 болатын реакцияны көрсет-
2Н20 = 2Н2+ О2 -
N2+ ЗН2 = 2NН3 -
J2 + H2 = 2HJ -
Сl2 + Н2 = 2НСl -
2NO + 02= 2N02
-
-
Энтропияның өлшем бірілігін көрсет-
Дж/мольК -
Дж/моль -
Кал/град -
Кал∙моль∙град -
Дж/град
-
-
Жылусыйымдылықтың анықтамасы --
Жылусыйымдылық - 1 моль заттың жоғары оксидтерге дейін толық жану реакциясының жылу эффектісі -
Жылусыйымдылық – бірлік мөлшердегі затты бір градусқа қыздыру үшін қажет жылу мөлшері -
Жылусыйымдылық – химиялық реакция мен процестердің жылу эффектілерін зерттейтін химиялық термодинамика бөлімі -
Жылусыйымдылық оқшауланған жүйедегі процестің шекті өтуі, бағыты, мүмкіндік критериі 5) Жылусыйымдылық – бірлік мөлшердегі затты он градусқа қыздыру үшін жұмсалатын жылу мөлшері
-
-
Изобаралық термодинамикалық процеске тән-
тұрақты көлем -
тұрақты температура -
Qv=ΔU -
QP=ΔН -
концентрация
-
-
Изохоралық термодинамикалық процеске тән-
тұрақты көлем -
тұрақты температура -
Qv=ΔU -
QP=ΔН -
концентрация
-
-
«Абсолютті нөл кезіндегі жеке кристалдық заттардың энтропиясы нөлге тең болады»-
термодинамиканың нөл заңы -
термодинамиканың бірінші заңы -
термодинамиканың екінші заңы
-
-
термодинамиканың үшінші заңы -
Кирхгофф заңы
-
Заттардың стандартты түзілу және жану жылулары негізінде анықтауға болады-
абсолютті энтропиясын -
заттардың біреуінің қайнау температурасын -
химиялық реакцияның жылуын -
химиялық реакцияның тепе -теңдік константасын -
ішкі энергия өзгерісін
-
-
Қайтымды изобаралық -изотермиялық процестің максимал жұмысы қандай абсолюттік шамаға тең-
энтропия -
Гиббс энергиясына -
энтальпия -
изохоралық-изотермиялық потенциалға -
Гельмгольц энергиясы
-
-
Қайтымды изохоралық -изотермиялық процестің максимал жұмысы қандай абсолюттік шамаға тең-
энтропия -
Гиббс энергиясына -
энтальпия -
изохоралық-изотермиялық потенциалға -
Гельмгольц энергиясы
-
-
кДж/моль өлшенетін шама-
S -
V
-
-
H -
Т -
P
-
Химиялық жүйедегі реакцияның өту өлшемі-
ішкі энергия -
жүйенің температурасы -
реакция өнімдерінің түзілу жылуы -
Гиббс энергиясы -
қоршаған ортаның температурасы
-
-
<мұз-су-бу> жүйесі-
екі компонентті жүйе, үшвариантты -
үш компонетті жүйе, бивариантты -
бір компонетті жүйе, инвариантты
-
4) үш компонентті жүйе, моновариантты 5) екі компонетті жүйе, бивариантты
-
QР=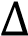 H теңдеуі қай заңмен сипатталады
H теңдеуі қай заңмен сипатталады
1) Лавуазье-Лаплас заңы
-
Термодинамиканың бірінші заңы -
Гесс заңының бірінші салдары -
Изобаралық процестің жылу эффектісі -
Изохоралық процестің жылу эффектісі
-
QV= U теңдеуі қай заңмен сипатталады
U теңдеуі қай заңмен сипатталады -
Лавуазье-Лаплас заңы -
Термодинамиканың бірінші заңы -
Гесс заңының бірінші салдары -
Изобаралық процестің жылу эффектісі -
Изохоралық процестің жылу эффектісі
-


