Файл: Отчет по лабораторной работе по физике студент Группа Факультет Преподаватель Барнаул 2022.docx
Добавлен: 17.10.2024
Просмотров: 14
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
КОНТРОЛЬНЫЕ ВОПРОСЫ
-
Что такое удельная и молярная теплоемкости вещества? От чего они зависят, в каких единицах измеряются? -
Что такое коэффициент Пуассона ? -
Сформулируйте первое начало термодинамики. -
Что такое внутренняя энергия идеального газа? От чего она зависит? -
Дать определение работы газа и количества теплоты.
ОТЧЕТ
ТЕОРЕТИЧЕСКИЙ КОНСПЕКТ (ответы на контрольные вопросы):

Коэффициент Пуассона равен отношению теплоемкостей
Согласно первому началу термодинамики, термодинамическая система (например, пар в тепловой машине)
может совершать работу только за счёт своей внутренней энергии или каких-либо внешних источников энергии.
Первое начало термодинамики объясняет невозможность существования вечного двигателя 1-го рода, который
совершал бы работу, не черпая энергию из какого-либо источника. Сущность первого начала
Q = DU + A (1)
Уравнение (1), выражающее первое начало термодинамики, является определением изменения внутренней энергии
системы (DU), так как Q и А — независимо измеряемые величины.
Внутреннюю энергию системы U можно, в частности, найти, измеряя работу системы в адиабатном процессе (то есть
при Q = 0): Аад = — DU, что определяет U с точностью до некоторой аддитивной постоянной U0:
U = U + U0 (2)

 Первоеначало термодинамики утверждает, что U является функцией состояния системы, то есть каждое состояние
Первоеначало термодинамики утверждает, что U является функцией состояния системы, то есть каждое состояние термодинамической системы характеризуется определённым значением U, независимо от того, каким путём система
приведена в данное состояние (в то время как значения Q и А зависят от процесса, приведшего к изменению
состояния системы). При исследовании термодинамических свойств физической систем первое начало
термодинамики обычно применяется совместно со вторым началом термодинамики.
-
Исходя из определения идеального газа, в нем отсутствует потенциальная составляющая внутренней энергии
(отсутствуют силы взаимодействия молекул, кроме ударного). Таким образом, внутренняя энергия идеального газа
представляет собой только кинетическую энергию движения его молекул. Внутренняя энергия зависит от
температуры.
-
При расширении газ совершает работу против внешней среды, передавая ей при этом энергию. При сжатии
наоборот, газ воспринимает работу, совершенную внешней средой и увеличивающей его внутреннюю энергию. При
этом осуществление работы возможно при наличии по меньшей мере двух движущихся тел, одно из которых
оказывает силовое воздействие на другое. Из сказанного следует, что работа есть одна из форм передачи энергии от
одного тела к другому. Количество работы представляет собой меру передаваемой энергии. Количество энергии,
полученное телом в форме работы, называется совершенной над телом работой, а отданную энергию в форме работы
– затраченной телом работой.
Количество теплоты - энергия, переданная системе внешними телами путем теплообмена (процесс обмена
внутренними энергиями при контакте тел с разными температурами). Можно говорить о двух формах передачи
энергии от одних тел к другим: работе и теплоте. Энергия механического движения может превращаться в энергию теплового движения и наоборот. При этих превращениях соблюдается закон сохранения и превращения энергии,
применительно к термодинамическим процессам этим законом и является первое начало термодинамики,
установленное в результате обобщения многовековых опытных данных.

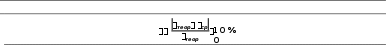
ВЫВОДЫ: Результаты экспериментальных расчетов по вычислению коэффициента Пуассона для воздуха
приближенно совпадают с истинным значением. Погрешность эксперимента можно считать удовлетворительной.
Лабораторная работа №24 Таблица 1.
