Файл: Лекция Предмет, разделы и задачи токсикологической химии. Пищеварение и метаболизм посторонних веществ ядов. Вещества, которые изолируются минерализацией биологического материала (металлические яды).docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.04.2024
Просмотров: 155
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
В случаях осознанного отравления меди сульфатом, содержание её в крови хорошо коррелировалось с тяжестью интоксикации; при отравлении содержание меди в крови достигало 2,87 мг/л, а в серьезных случаях – 7,98 мг/л. Содержание ионов меди в сыворотке крови в последнем случае составляло 2,57 мг/л при измерении её концентрации в первые двенадцать часов и 0,23 мг/л по истечению этого времени, что связано с переходом в эритроциты.
Смерть обычно наступает в 1-7 день после приема 10-20 г растворимой соли меди и часто этому предшествует рвота, гемолиз крови, печеночная и почечная недостаточность и шок. В случаях с летальным исходом содержание меди в мг/л или мг/кг в тканях человека было следующим:
| Объекты исследования | кровь | мозг | печень | Почка |
| Средний уровень | 36 | 6,8 | 285 | 39 |
| Диапазон концентраций | 2,5-66 | 2-11 | 8,3-1401 | 10-61 |
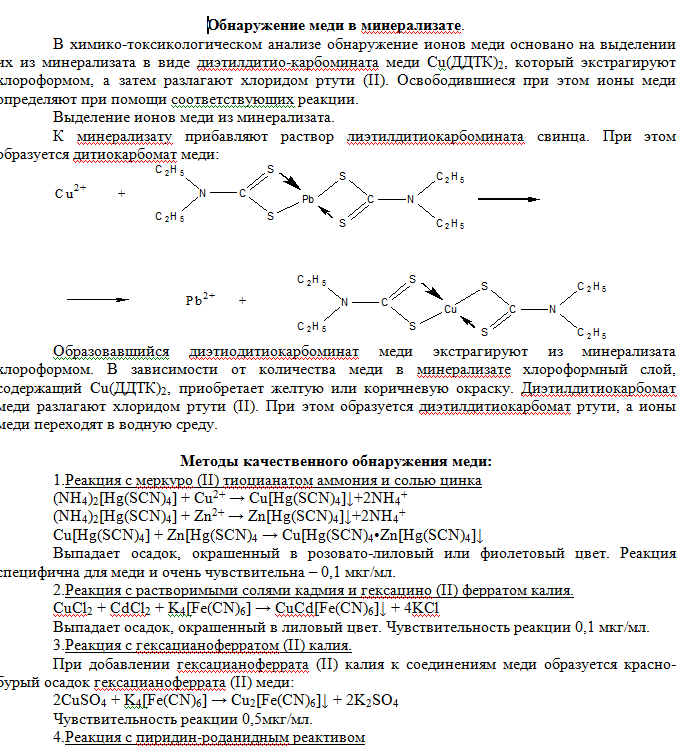
При добавлении по каплям 1-2 мл пиридино-роданидного реактива (смесь равных объемов 50%-го водного раствора пиридина с 20%-ым раствором роданида аммония) и 1 мл хлороформа к раствору содержащему ионы меди (II) – слой органического растворителя окрашивается в изумрудно-зеленый цвет.

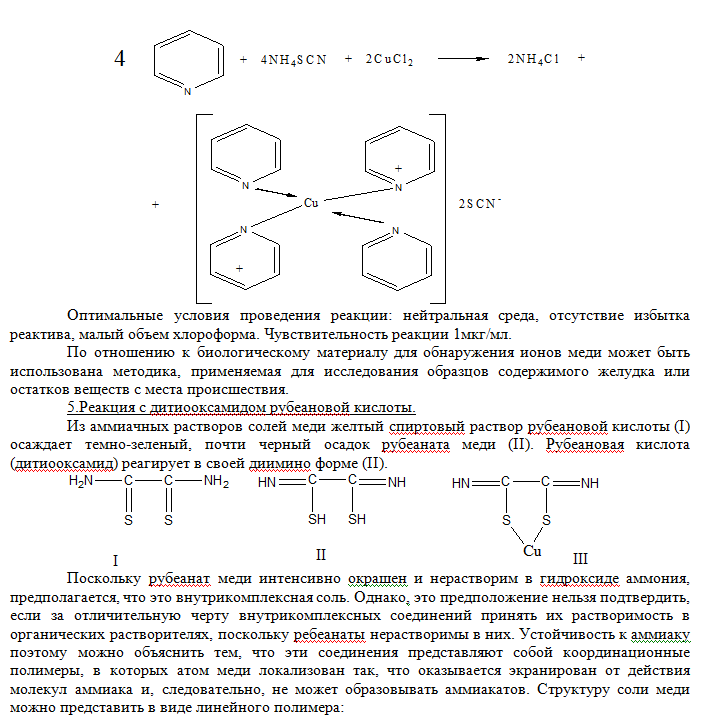
Реакция с рубеановой кислотой (дитиооксамидом) на медь чрезвычайно чувствительна. Если в качестве маскирующих агентов использовать малоновую кислоту и этилениамин, то медь можно обнаружить с рубеановой кислотой без помех со стороны всех других ионов металлов. Чувствительность реакции 0,006 мкг/мл.
Выполнение реакции.
На фильтровальную бумагу наносят каплю исследуемого раствора, выдерживают над аммиаком и добавляют каплю 1%-го спиртового раствора рубеановой кислоты (дитиооксамида). Появление черного или оливково-зеленого пятна или кольца указывает на присутствие меди (II).
Для анализа содержимого желудка или остатков с места происшествия на ионы меди (II) применяются также реакция с меркуро (II) тиоцианатом аммония и солью цинка, описанная выше как один из вариантов обнаружения меди в минерализате.
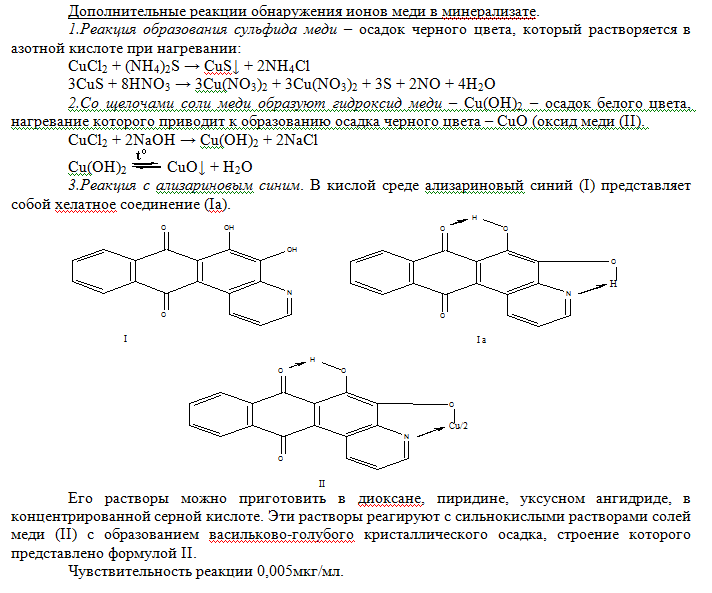
Количественное определение.
Исходя из широкого варьирования количества меди в органах и тканях трупа человека ( от миллиграммовых до нескольких десятков миллиграмм) в научной литературе описано несколько методов определения меди при химико-токсикологических исследованиях.
1.Объемный метод. Комплексонометрическое титрование ионов меди (II) после выделения их экстракцией в виде (ДДТК)2Cu с последующей реэкстракцией в водный слой. В качестве индикатора при титровании трилоном Б используется мурексид; рН 7,0-8,0. Определяется при 10мг ионов меди (II) в 100г биологического объекта 98% с относительной ошибкой 2,2%, при 1мг – 96% со средней относительной ошибкой 6,5%. Граница определения 0,5мг.
2.Экстракционное тирование дитизоната меди (II) при рН 3,3. Ионы меди образуют с дитизоном внутрикомплексное соединение, которое эксрагируется хлороформом. Дитизонат меди разлагают хлоридом ртути (II). При этом образуется дитизонат ртути, а ионы меди переходят в водную фазу. Их оттитровывают раствором ЭДТА при индикаторе эрихром черный Т (переход окраски из черной в синюю).
Фотоколоримтрические методы.
1.Определение с диэтилитиокарбаматом. Этот метод дает возможность определять очень малые следы меди, если образующееся соединение экстрагировать.
Диэтилдитиокарбамат образует с ионами меди (II) комплексное соединение, окрашивающее раствор в желтый или коричневый цвет. Окраска получается мгновенно и сохраняется, не ослабевая, в течении 1 часа.
Полученное окрашенное комплексное соединение растворимо в четыреххлористом углероде, хлороформе, амиловом спирте, амилацетате. Наиболее устойчивые растворы диэтилдитиокарбаната меди в хлороформе. Молярный коэффициент светопоглощения Е≈13000 при λ=435 нм.
Определяется при 10 мг ионов меди (II) в 100 г биологического материала 98%, при 0,1 мг – 72%, со средней относительной ошибкой соответственно 41% и 15,3%. Ионы меди (II) определяются в пределах 0,1-1 мг. Граница определения 0,1 мг.
2.Дитизоновый метод. При рН 0,5 и выше фиолотово-красный дитизонат меди экстрагируется хлороформом или четырёх-хлористым углеродом.
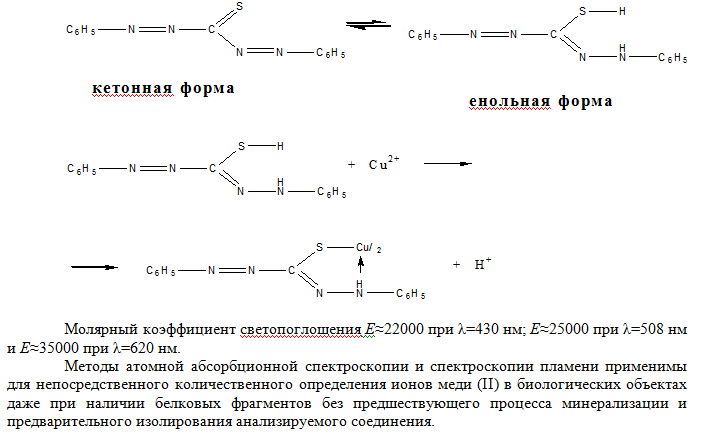
В сильно кислых средах это соединение экстрагируется очень медленно. В условиях проведения анализа дитизон находится в енольной форме:
Висмут
Среди элементов периодической системы висмут – последний практически не радиоактивный элемент. И он же открывает шеренгу тяжёлых металлов – естественных α-излучателей.
Традиционные потребители висмута – металлургическая (лёгкоплавкие сплавы), фармацевтическая (лекарственные средства) и химическая промышленность (красители, пигменты). Последние десятилетия к ним добавилась ядерная техника и электроника.
В медицинской практике применяются малорастворимые соединения висмута (алюминаты, карбонаты, галлаты, нитраты, салицилаты, цитраты в виде основных солей), как вяжущие антоцидное средство при лечении язв диареи, сифилиса, дерматитов, эрозии, экземы, бородавок. К лекарственным средствам, содержащим висмут и включённых в номенклатуру разрешённых к применению в Украине препаратов относятся: нитрат висмута основной, ксероформ (триброфенолят висмута основной),дерматол (галлат висмута основной), бисмоверол (основная соль висмута и моновисмутовинной кислоты), пентеабисмол, хинина йодвисмутат.
Содержание в крови: концентрация висмута в крови пациентов, лечивших язву желудка и двенадцатипёрстной кишки, находилась в пределах от 0,001 до 0,012 мг/л.
Метаболизм и выделение. Малорастворимые соединения висмута принимаемые перорально в значительной степени выводятся с калом. Препараты висмута вводимые в организм в виде инъекции (обычно субсалицилаты, тиогликоляты, тригликоляты, йодвисмутаты, тартраты, цитраты) выводятся мочой в течение нескольких недель. Человеческий мозг, лёгкие и печень содержат менее чем 0,4 мг/кг. Содержание висмута в моче в норме составляет 0,018 мг/л. В то время как при лечении язвы препаратами, содержащими висмут, содержание его в моче составляет 0,480 мг/л.
При лечении сифилиса путём введения внутримышечно висмута субсалицилата (60-2100 мг в пересчёте на висмут) и умерших через 1-251 день, содержание элементов в ткани было следующим:
| Средняя концентрация висмута у больных подвергшихся лечению мг/л или мг/кг | ||||||
| кровь | мозг | легкон | печень | желчь | почка | Моча |
| 0,5 | 0,6 | 0,9 | 6,8 | 3,9 | 33 | 1,2 |
Токсичность
. Проявление токсичности висмута подобны тем, которые наблюдаются при отравлении свинцом или ртутью. Усиленное слюноотделение, обесцвечивание языка, дёсен, кожи, боли в абдоминальной полости, тошнота. Повреждение почек является основным результатом приёма завышенной дозы висмута. Однако наблюдается явления энцефалопатии и периферической невропатии. Иногда наблюдается тошнота, рвота и нефротоксичность при внутримышечном введении висмута тиогликолята; причём функція почек возвращалась в норму через несколько недель. Подобная картина наблюдается и при пероральном прийме тригликолямата ви смута. Постоянное употребление субгаллата ви смута перорально, обачно назначаемого при желудочно-кишечных заболеваний, приводит к дрожанию мышц, нарушению координации движения, потери памати, замешательство, раздрожительность и временной потери зрения. В ряде случаев постоянное применши субсалицилата висмута приводит к энцефалопатии, концентрація ви смута в крови при этом составляла 0,072 мг/л.
При отравлении висмутом, которое является результатом постоянного и длительного применения субнитрата висмута перорально концентрация его в крови была в пределах от 0,05 до 1,60 мг/л, а в моче – 0,15-10,25 мг/л. Все пациенты, которые выжили в первые 7-14 дней после появлення признакою отравления, не зависимо от пути введения ви смута в организм, поправлялись без особого ущерба для здоровья.
Обнаружение висмута в минерализате.
Для обнаружения висмута в минерализатах вначале выполняют предварительные реакции на ионы этого металла с тиомочевиной и 8-оксихинолином (о-оксихинолином). При положительном результате этих реакций висмут выделяют из минерализата в виде диэтилдитиокарбамата, который экстрагируют хлороформом. После прибавления кислоты к хлороформной вытяжке происходит разложение диэтидитиокарбамата висмутом. Образовавшиеся при этом ионы висмута переходят в водную фазу, которую используют для обнаружения указанных ионов.
Реакция с тиомочевиной. Во время взаимодействия ионов висмута с тиомоевиной могут образовываться различного состава тиомочевинные комплексы, имеющие лимонно-желтую окраску:

Кроме ионов висмута с диэтилдитиокарбаматом натрия образует комплексные соединения и другие ионы, содержащиеся в минерализате. Для маскировки этих ионов добавляют раствор трилона Б (комплексона (III)). образовавшийся комплекс диэтилдитиокарбамата висмута экстрагируют хлороформом, затем разлагают азотной кислотой. Висмут при этом переходит в водную фазу в виде Bi(NO
3)3. Хлороформный слой отбрасывают.
При дальнейших исследованиях необходимо учитывать, что разбавление водой минерализата приводит к гидролизу нитрата висмута, который в виде белого аморфного соединения выпадает в осадок:
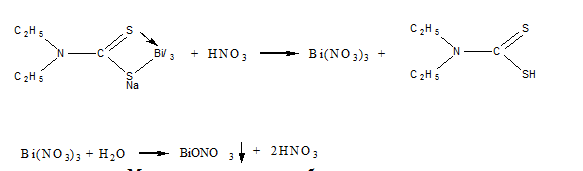
4.Тест Рейнша. Методика теста. Методика теста применяется для обнаружения висмута в моче, содержимом желудка и остатках веществ с места происшествия.
При нагревании медной пластинки, предварительно очищенной азотной кислотой, с анализируемым раствором в присутствии концентрированной хлороводородной кислоты её поверхность окрашивается в блестящий черный цвет при наличии паров висмута в исследуемом объекте. Чувствительность теста – 2 мг/л.
Если на поверхность, почерневшей в процессе теста медной пластинки, нанести реактив, содержащий хини и иодид калия, висмут медленно образует оранжево-коричневую суспензию.
5.Реакция с цинхонином и иодидом калия. Многие, преимущественно одноосновные органические соединения, и среди них цинхонин, образует в слабокислых растворах солей висмута и иодида калия нерастворимые двойные иодиды с общей формулой BiI3•B•HI, где В – молекула цинхонина.
На фильтровальную бумагу, пропитанную раствором цинхонина (один из алкалоидов хинного дерева) помещают каплю слабокислого анализируемого раствора. Образование оранжево-красного пятна указывает на присутствие ионов висмута. Предел обнаружения 0,14 мкг.
6.Люминисценция в водородном пламени. Водородное пламя вызывает васильково-синее свечение ионов висмута. Метод позволяет обнаружить весьма небольшие количества висмута, если анализируемый образец предварительно смещать с карбонатом щелочноземельного металла и смесь внести в пламя. Предел обнаружения – 0,004 мкг.
7.Реакция с тиоциоатом хром-калия. Минеральнокислые растворы солей висмута, взаимодействуя с гексатиоцианатохромато (III) калия K3[Cr(SCN)6], дают нерастворимый кирпично-красный осадок гексатиоцианатохромато (III) висмута
 Bi3++[Cr(SCN)6]3- K3[Cr(SCN)6]↓
Bi3++[Cr(SCN)6]3- K3[Cr(SCN)6]↓На фильтровальную бумагу наносят каплю анализируемого раствора, высушивают и добавляют каплю спиртового раствора реагента. Вновь высушивают и добавляют каплю разбавленной (1:2) серной кислоты. В зависимости от содержания висмута образуется кирпично-красно пятно или кольцо. Предел обнаружения 0,4 мкг.

