Файл: Блок i организационнопрововые основы судебномедицинской деятельности в рф. Порядок и проведение судебно медицинских и химикотоксикологических исследований.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 29.04.2024
Просмотров: 30
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Прибор разбирают, место налёта в восстановительной трубке нагревают на горелке. На холодных частях трубки образуется белый налет оксида мышьяка, кристаллы которого имеют под микроскопом форму октаэдра.
Белый налет в трубке растворяют в 2 каплях 5% раствора азотной кислоты. Раствор упаривают на предметном стекле досуха. Сухой остаток растворяют в 1 – 2 каплях 10% соляной кислоты.
В раствор вносят кристаллы хлорида цезия. Если осадка не появилось, то можно говорить об отсутствии сурьмы. Далее добавляют несколько кристаллов иодида калия. В присутствии мышьяка под микроскопом кристаллы красного цвета в виде правильных шестилучевых звезд гексаиодарсенат цезия и гексаиодарсенит цезия.
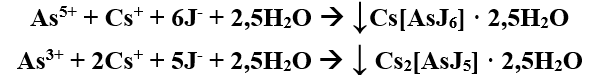
На осадок действуют 1 – 2 каплями пиридина. При наличии мышьяка осадок растворяется, а по краям капли образуется скопление зеленовато – желтых игольчатых кристаллов. При наличии сурьмы кристаллы теряют окраску, но сохраняют форму.
Предел обнаружения – 0,1 мкг мышьяка в пробе.
4.Количественное определение яда
1.Атомно – абсорбционная СФМ при 193,7нм
Аликвоту исследуемого минерализата (5 мкл) вносят графитовую печь электротермического атомизатора. Цикл работы состоит из стадий:
– испарения
– пиролиза (три стадии)
– атомизации
– очистки
После окончания цикла и индикации результатов измерения, значения массовой концентрации элемента – аналита вычисляют по амплитуде анализируемого сигнала. Измерение концентрации для каждой пробе проводят дважды и вычисляют среднее арифметической. Массовую долю металла в биоматериале (в мкг⁄мл) вычисляют по формуле:
где С – концентрация элемента в анализируемом растворе, мкг⁄мл; Со – концентрация элемента в фоновом (холостом) растворе, мкг⁄мл; V – объём анализируемого минерализата, л; Р – навеска пробы, мл.
2. ФЭК.
Проводят реакцию AsН3 c ДДТК серебра в пиридине. Мышьяковистый водород получают в специальном приборе, так чтобы проба не содержала влаги. Химизм образования ДДТК мышьяка не выяснен, образующийся комплекс имеет устойчивую красно – фиолетовую окраску, но в присутствии воды легко гидролизуется.
Оптическую плотность измеряют на ФЭК при 540 нм в кювете с толщиной слоя в 10 мм. Раствор сравнения – 1 мл раствор 20% раствора серной кислоты.
Концентрацию металла определяют по стандарту (0,1 мг/мл). Для пересчета количества мышьяка на 100 мл биоматериала используют формулу:
Сх = Аиссл ∙ Сст ∙ V1 ∙ 100
Аст ∙ V2 ∙ В
Сx – количество мышьяка в мг на мл биоматериала; Аиссл., Аст. – оптические плотности исследуемого и стандартного растворов; V1 – общий объем минерализата; V2 – аликвота, взятая для определения, мл; В – навеска биологического материала, мл.
Метаболизм. Мышьяк обладает способностью кумулироваться. При остром отравлении он концентрируется в основном в ЖКТ и паренхиматозных органах, при хроническом отравлении накапливается в костях и ороговевших тканях (волосы, ногти, кожа). Выделяется мышьяк медленно через почки, кишечник, потовые железы и с молоком.
Токсикологическое значение.
Ангидрид мышьяковистой кислоты применяется в медицине, в сельском хозяйстве (как инсектицид), в стекольной и кожевенной промышленностях. Арсениты и арсенаты некоторых металлов применяются в качестве ядохимикатов. Сюда относится парижская (швейнфуртская) зелень. Определенное токсикологическое значение имеют органические соединения мышьяка, применяемые в медицине (новарсенол, осарсол и др.). Известны случаи отравлений мышьяковистым водородом. Очень токсичными являются боевые отравляющие вещества (люизит, адамсит и др.), содержащие мышьяк. Соединения пятивалентного мышьяка в организме превращаются в более токсичные соединения трехвалентного мышьяка.
БЛОК V
ХТА группы токсикологически важных веществ, изолируемых экстракцией и сорбцией («Лекарственные яды»)
7.Составить примерный план анализа при подозрении на отравление алкалоидами – производными изохинолина (папаверин).
Алкалоид папаверин содержится в опии в количестве 0,1 – 1,5%. Папаверин обладает основными свойствамиза счет третичного атома азота в молекуле. Экстрагируется из щелочных фракций (рН 8 – 10,0)
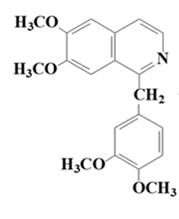
Перечь объектов исследования.
Приказ Минздравсоцразвития РФ от 12.05.2010 № 346н
– комплекс внутренних органов (содержимое желудка, 1/3 печени, желчь, одну почку); биологические жидкости (всю мочу, но не более 200 мл и 200 мл крови); лекарственные препараты
Изолирование – возможно применение общих методов, изолирование проводят из щелочных фракций:
– Метод Стаса – Отто – изолирование этиловым спиртом, подкисленным щавелевой или винной кислотой; Метод А.А.Васильевой – изолирование водой, подкисленной органической кислотой; Метод В.А.Карташова – изолирование нейтральным ацетоном; Метод прямой экстракции липофильными растворителями
Схема изолирования общим методом А.А. Васильевой.
1.Настаивание измельченного объекта с водой, подкисленной щавелевой кислотой до рН 3, в течении двух часов. Воды берем в количестве 1:2 по отношению к навеске объекта. Водное извлечение фильтруем.
2.Экстрагирование веществ кислого характера из водного фильтрата хлороформом при рН = 2 (трехкратная экстракция), отделение органической фазы и концентрирование извлечение упариванием (фракция «кислое извлечение»). При этом разрушаются комплексы папаверина с белками, он приобретает положительный заряд за счет протонирования и переходит в водную фазу. Данную фракцию отбрасываем.
3.Подщелачивание оставшегося после разделения фаз водного слоя раствором аммиака до рН 10, экстрагирование веществ основного характера трехкратной экстракцией хлороформом, отделение органической фазы и концентрирование упариванием (фракция «щелочное извлечение»). Папаверин в щелочной среде находится в молекулярной форме и экстрагируется в неполярный растворитель – хлороформ.
Методы очистки.
С целью очистки извлечений из биологического материала в химико – токсикологическом анализе широко используются различные виды и варианты хроматографии. Наиболее часто для очистки извлечений используется тонкослойная хроматография (ТСХ) и колоночная хроматография (КХ).
Фракцию «щелочное извлечение» исследуют на наличие папаверина.
1.ТСХ.
В тонкослойной хроматографии роль неподвижной фазы выполняет фиксированный тонкий слой сорбента (0,1 – 0,5мм), содержащий определенное количество воды, нанесенный на хроматографическую пластинку из стекла, фольги, полимера. В качестве сорбентов чаще используют силикагель и окись алюминия. Для лучшего удерживания на пластинке в сорбент добавляют связующий компонент – гипс, крахмал и др. Роль подвижной фазы выполняет индивидуальный растворитель или их смесь, так называемая «хроматографическая система».
В процессе хроматографирования, по мере того как растворитель поднимается вверх по пластинке за счет капиллярных сил, происходит разделение смеси веществ согласно их коэффициентам распределения между подвижной и неподвижной фазами
Методика. 5 – 10 мкл извлечения исследуют методом одномерной восходящей хроматографии на пластинках «Силуфол УФ254» или «Сорбфил ПТСХ-ПА-УФ».
Для разделения и идентификации всего применяются
многокомпонентные системы растворителей (для веществ основного характера):
диоксан – хлороформ – ацетон – 25 % раствор аммиака (47,5:45:5:2,5)
ацетон – хлорофром – 25% раствор аммиака (245:12:1).
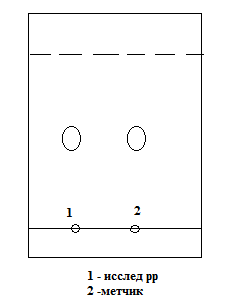
Схема детектирования. После того как система растворителей поднимется на 10 см выше линии старта, пластинку вынимают из камеры, подсушивают на воздухе и опрыскивают реактивом Драгендорфа, модифицированным по Мунье.
Расчет Rf. Величина Rf – отношение длины пробега анализируемого вещества (а) к длине пробега растворителя (b): Rf = a / b
При проявлении пятен и соответствующих значений Rf = 0,75 – 0,80, выполняют частные реакции и проводят количественное определение.
Окраска пятен. Желто – оранжевые
2.Химические реакции.
2.1. Обнаружение с помощью общеалкалоидных реактивов. С реактивом Драгендорфа образуется оранжевый осадок:
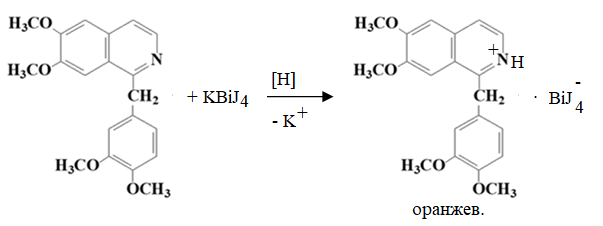
2.2. Реакция с серной кислотой, образуется фиолетовое окрашивание (оксониевая соль):
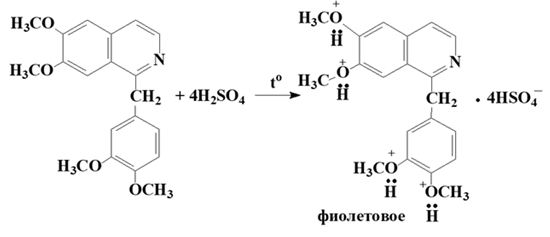
2.3. Реакция окислительной конденсации с реактивом Марки – при этом образуется сульфат метиленбиспапаверина, который легко окисляется при добавлении бромной воды, а при добавлении аммиака образует фиолетовый осадок, растворяющийся в этаноле с образованием раствора, окрашенного в фиолетовый цвет:
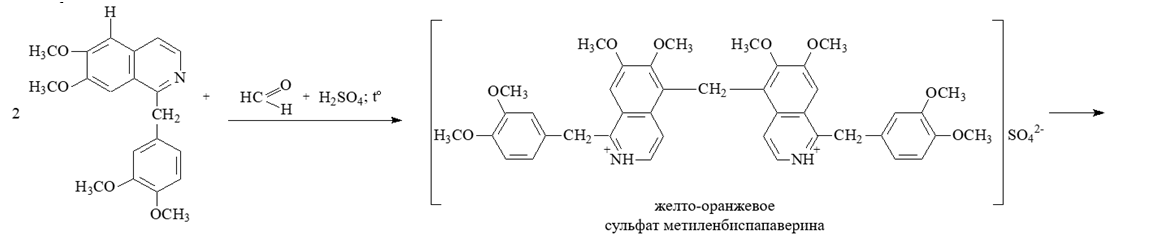

2.4. Характерной реакцией на папаверин является каролиновая проба: к исследуемому порошку прибавляют концентрированную серную кислоту, уксусный ангидрид и нагревают. Появление ярко-желтого окрашивания и зеленой флуоресценции указывает на наличие папаверина:
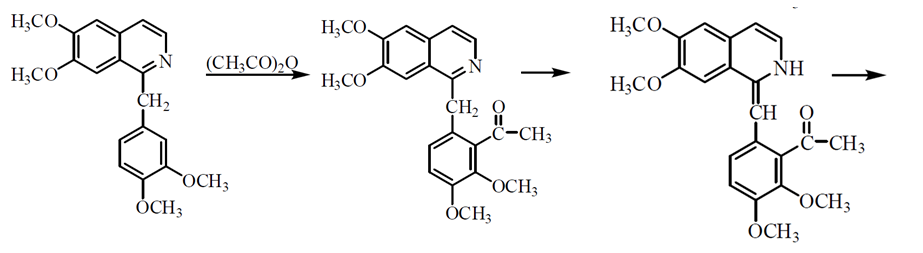
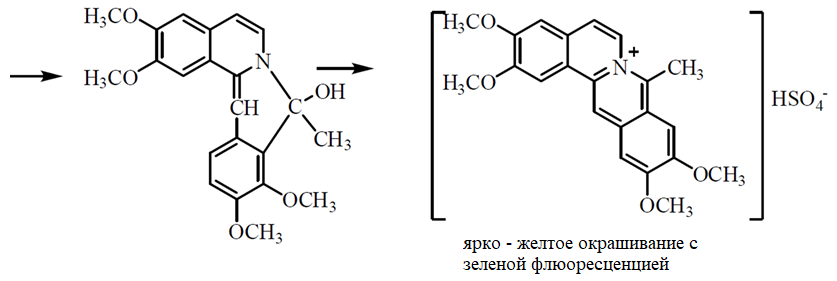
2.5. Микрокристаллические реакции
. На предметное стекло наносят несколько капель исследуемого раствора и выпаривают досуха. К сухому остатку прибавляют каплю 0,1 н. раствора соляной кислоты. Рядом наносят каплю 10 % раствора хлорида кадмия, а затем соединяют эти растворы. При наличии папаверина появляются сростки из тонких пластинок, имеющих форму куба.
3.Исследование извлечения методом СФМ в УФ – области спектра.
В молекуле папаверина имеется цепь сопряженных двойных связей, которые обеспечивают поглощение веществами излучения в УФ – области спектра. Длины волн, соответствующие максимумам поглощения в спектре исследуемого соединения, должны совпадать с таковым в спектре стандарта.
Основание папаверина в 1 н. растворе соляной кислоты имеет максимум поглощения при 250, 284 и 310 нм. Раствор папаверина в 1 н. растворе серной кислоты имеет максимумы поглощения при 250. 254 и 310 нм
4. Исследование методом ВЭЖХ.
ВЭЖХ, или жидкостная хроматография высокого давления, является вариантом колоночной жидкостной хроматографии, где элюент подается на колонку под большим давлением, что ускоряет проведение анализа. Разделение веществ проводится на колонках, заполненных мелкодисперсным сорбентом (силикагель, окись алюминия) или полимерным сорбентом.
Папаверин имеет значительную молекулярную массу и содержит реакционноспособные группировки. Роль неподвижной фазы выполняет силикагель с привитой жидкой углеводородной фазой, элюентом служит ацетонитрил или метанол, детектор – спектрофотометр.
Часть извлечения после очистки методом ТСХ вводят в колонку жидкостного хроматографа.Определение проводят на 2 или 4 хроматографических колонках; на хроматограмме появляется пик, время удерживания или объем которого должен совпасть с параметрами удерживания ацетона – стандарта.
Время удерживания на колонке характерно для каждого из разделяемых веществ, поэтому служит качественной характеристикой вещества. Исправленное время удерживания рассчитывается как разность абсолютного времени удерживания вещества и времени удерживания несорбируемого компонента:
t испр = t абс – t н.к.
Удерживаемый объем также является качественной характеристикой анализируемого вещества. Удерживаемый объем V – это объем газа-носителя, необходимый для вымывания всего количества вещества из колонки, который численно равен произведению скорости газа – носителя U на время удерживания t:

