ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 05.05.2024
Просмотров: 210
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
114
| Нейтральные моносахариды (мольные %) | Fuc | 58,2 | 72,7 | 86,3 | 86,0 | 60,8 |
| Gal | 20,0 | 15,7 | 4,7 | 6,0 | 3,3 | |
| Man | 1,8 | 6,8 | 1,5 | 1,5 | 26.0 | |
| Rha | 4,2 | 1,4 | 0 | 0 | 0 | |
| Xyl | 4,1 | 1,7 | 1,2 | 1,6 | 6,0 | |
| Glc | 11,7 | 1,6 | 6,3 | 4.9 | 3,9 |
* — % от веса сухой обезжиренной водоросли; ** — % от веса фракции.
Таким образом, из F. evanescensпри разных температурах были выделены сульфатированные фуканы (фракции FeFl и FeF2), практически не отличающиеся по моносахаридному составу, содержанию сульфатов и молекулярным массам. Аналогичные сульфатированные фуканы из этой водоросли были выделены ранее при 85°С (продолжительность экстракции 5 часов) (Bilan et al., 2002) и при 60°С (продолжительность экстракции 5 часов) (Zvyagintseva et al, 2003). Дополнительной экстракцией с небольшим выходом была получена фракция фукоидана FeF3 с высоким содержанием маннозы (26% от суммы нейтральных моносахаридов) и уроновых кислот (50% от фракции) (табл. 5.1). Наличие глюкозы в составе моносахаридов указывало на присутствие во фракциях F1 и F2 ламинарана. Можно отметить, что исходное содержание ламинарана в обеих водорослях невелико.
Фракцию FeFl из F. evanescensразделяли дробным осаждением этанолом на фукоидан (FeFl-f) и ламинаран (FeFl-1), характеристика фракций представлены в таблице 5.2. Доля глюкозы в моносахарид ном составе фракции FeFl-f в результате дробного осаждения уменьшилась в 3,9 раза и возросла доля фукозы. Ранее было показано, что ламинаран из
F. evanescensпредставляет собой 1,3;1,6-(3-В-глюкан с очень высоким содержанием (3-1,6-связанных (до 35%) остатков глюкозы (Звягинцева и др., 1994).
Таблица 5.2 Характеристика фукоидана (FeFl-f) и ламинарана (FeFl-1), полученных осаждением этанолом из фракции FeFl, выделенной из F. evanescens
экстракцией при 20°С
| Фракция | FeFl | FeFl-f | FeFl-1 |
| Выход, %* | 2,5 | 1,7 | 0,7 |
| Уронаны, %** | 0,3 | 0,7 | H.O. |
115
| Фукоидан, %** | 65,0 | 73,4 | H.O. | |
| Сульфаты, %** | 22,7 | 23,0 | H.O. | |
| Нейтральные моносахариды (мольные %) | Fuc | 86,3 | 91,0 | 79,0 |
| Gal | 4,7 | 4,6 | 1,1 | |
| Man | 1,5 | 1,4 | 0 | |
| Rha | 0 | 0 | 0 | |
| Glc | 6,3 | 1,6 | 19,8 | |
| Glc | 6,3 | 1,6 | 19,8 | |
* — % от веса сухой обезжиренной водоросли; ** — % от веса фракции, и.о.- не определяли
Сравнительный анализ полисахаридов фракций CcFl и CcF2, выделенных из
С. costataпоследовательно при 20°С и при 60°С показал, что фракция CcFl из С. costataсодержала значительную долю глюкозы по сравнению с фракцией CcF2. Можно предположить, что почти весь ламинаран извлекался из С. costataпри холодной экстракции (табл. 5.1).
Молекулярно-массовое распределение фукоиданов во фракциях CcFl и CcF2 из С. costataбыло неоднородным и находилось в интервале от 20 до 600 кДа с главным максимумом при 300 кДа и двумя пиками меньшей интенсивности с максимумами при 80 и 560 кДа. Фракция CcF2 содержала полисахариды с меньшей молекулярной массой, с максимумом при 70 кДа. Определение молекулярной массы полисахаридов выполняли методом ВЭЖХ. Разделение фукоиданов проводили на последовательно соединенных колонках Shodex Asahipak GS-520 HQ и GS-620 HQ (7,5 мм x 300 мм) при 50°С, элюируя Н20 (0,8 мл/мин). Колонки калибровали, используя как стандарты пуллуланы с молекулярными массами от 180 до 667000 Да и голубому декстрану
Сравнительная оценка содержания сульфатных групп в фукоиданах CcFl и CcF2 проводилась путем сравнения величин отношений значений интенсивностей валентных колебаний при 1260—1264 см-1 (0=S=0 группы) и при 1082 см * (углеродный скелет сахарного кольца) относительно локальной базовой линии в области 1580—880 смл(рис. 5.1). Сравнение полученных величин (0,92 и 0,67 соответственно) показало, что содержание сульфатных групп во фракции CcFl было на 25% больше, чем во фракции CcF2, т.е. при холодной экстракции был получен более сульфатированный фукоидан. Кроме того, фракция фукоиданов (CcF2) содержала меньше Gal, но больше Man, чем фракция CcFl (табл. 5.1).
При последовательной экстракции С. costataбыли получены фракции фукоиданов разные по составу и молекулярной массе.Тогда как анало-
116
м I I III I II
R = ABS„„ / ABS„j = 0,923
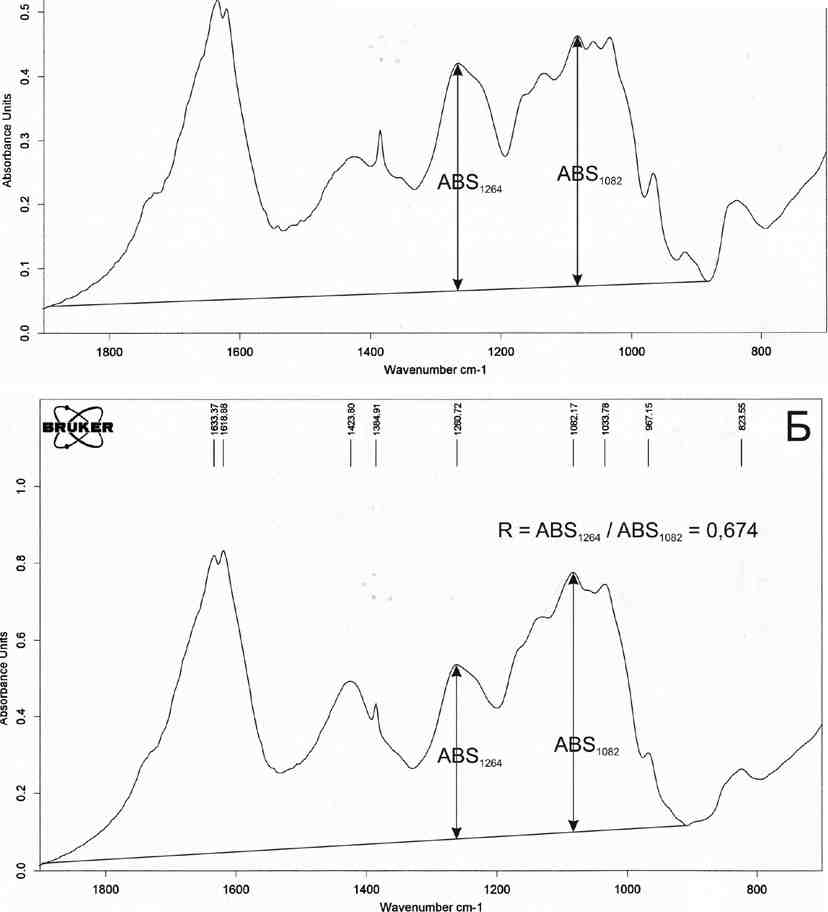
гичные фракции фукоиданов FeFl и FeF2 из F. evanescens практически не различались (табл. 5.1). Интересно отметить, что, при дополнительном экстрагировании Е evanescensв более жестких условиях (60°С, 12 ч) была получена фракция фукоидана FeF3, свойства которой (высокое содержание альгиновых кислот и значительная доля Man в составе моносахаридов, низкое содержание сульфатов) были близки к свойствам фракции CcF2 из С. costata(табл. 5.1). Возможно, фракции фукоиданов CcF2 и FeF3 извлекаются при разрушении клеточных стенок, Рис. 5.1. ИК-спектры фракций CcFl (А) и CcF2(B), причем для p. evanescens ЭТОТ выделенных из С. costataэкстракцией при темпе- ппопесс TDe6veT более жестких ратуре 20 и 60°С соответственно условий. Была показана воз-
можность фракционирования фукоиданов, используя разные технологические режимы экстракции. При комнатной температуре из С. costataэкстрагировали преимущественно галактофуканы, а из F. evanescens— сульфатиро-ванные фуканы. При более жестких условиях экстракции (60°С) из С. costataвыделили фукоидан преимущественно аскофилланового строения. Для F.evanescens, имеющего более жесткий таллом, фукоидан аскофилланового строения был получен при экстрагировании в течении 12 часов при 60°С (фракция FeF3).
Приведенные примеры показали, что технологии выде-
6
200 300
Объем элюции, мл
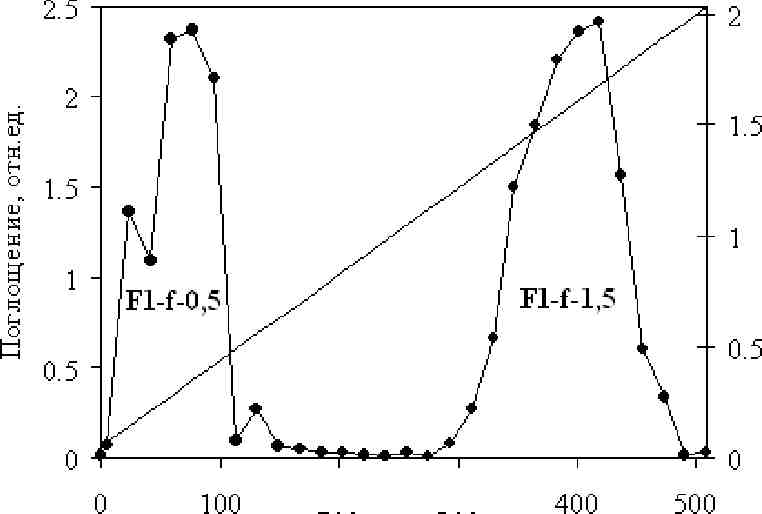
Рис. 5.2. Хроматография фракции CcFl-f на DEAE-целлюлозе (3,5 X 14 см) линейным градиентом
Н20- 2М NaCl
117
ления водорастворимых полисахаридов из водорослей разных порядков должны быть индивидуальными.
Для дальнейшей детальной характеристики состава полисахаридов фракцию CcFl, выделенную из С. costataхолодной экстракцией, очистили гидрофобной хроматографией на ПХ-1 от примеси ламинарана, получили фракция CcFl-f, которую дополнительно фракционировали ионообменной хроматографией на DEAE-целлюлозе. Сорбированные на DEAE-целлюлозе полисахариды элюировали линейным градиентом Н20—2М NaCl (рис. 5.2). Получили подфракций CcFl-f-0,5 и CcFl-f-1,5, характеристика этих фракций приведена в таблице 5.3.
Таблица 5.3 Характеристика подфракций CcFl-f-0,5 и CcFl-f-1,5, полученных хроматографией на DEAE-целлюлозе фракции фукоидана CcFl-f из
С. costata
| Фракция | CcFl-f | CcFl-f-0,5 | CcFl-f-1,5 | |
| Выход, %* | 100 | 29 | 69 | |
| Mw, кДа | 80-800 | 20-200,200-800 | 40-600 | |
| Fuc/ Gal | 1/0,27 | 1/0,28 | 1/0,28 | |
| Na S03- %* | 17,3 | 6,7 | 23,8 | |
| Моносахариды (мольные %) | Fuc | 55,1 | 22,6 | 70,2 |
| Gal | 18,1 | 6,4 | 19,8 | |
| Man | 9,2 | 37,0 | 7,0 | |
| Rha | 11,5 | 4,2 | 0 | |
| Xyl | 4,3 | 4,6 | 0 | |
| Glc | 1,8 | 9,6 | 0 | |
| GlcA | и.о. | 15,5 | 3,0 | |
* — % от веса фракции фукоидана; н.о. — не определяли.
Подфракция CcFl-f-0,5 содержала низкосульфатированный гетерогенный по моносахаридному составу фукоидан с высоким содержанием маннозы и глюкуроновой кислоты (табл. 5.3). В этой подфракций присутствовали примерно в равных количествах фукоиданы с молекулярными массами от 20 до 200 и от 200 до 800 кДа (рис. 5.3).


