ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 05.05.2024
Просмотров: 203
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
33
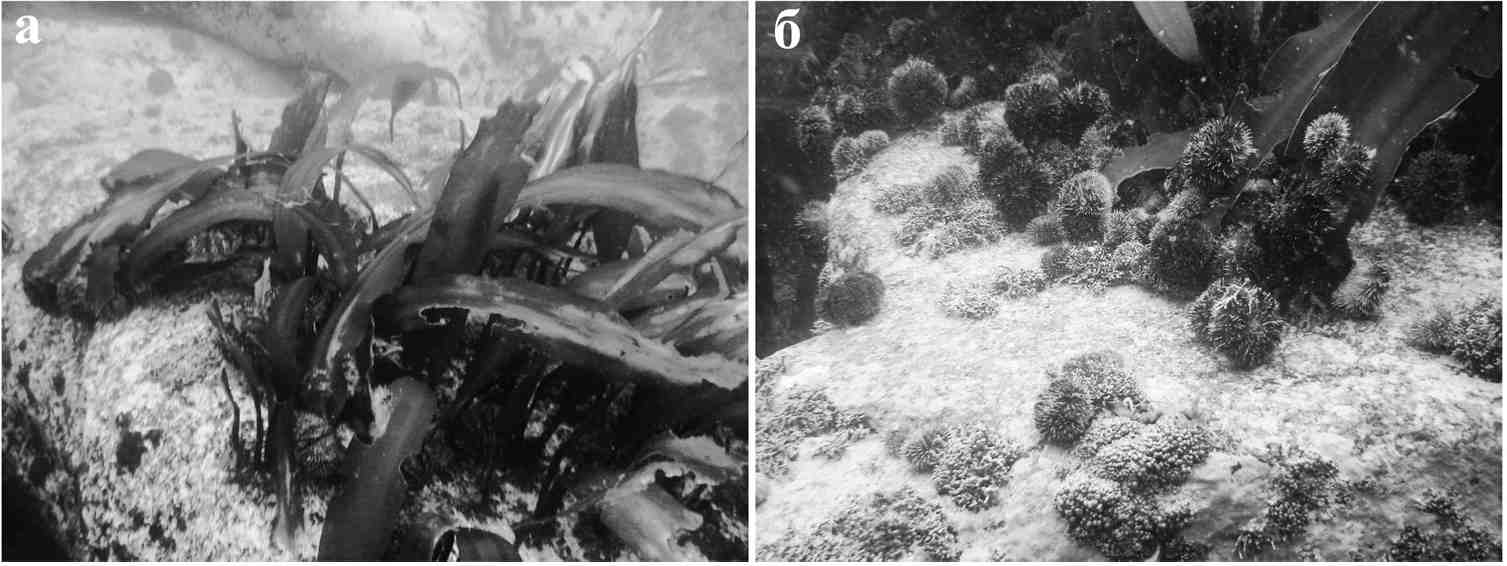
Рис. 1.17. Восстановленное поле ламинарии в северном Приморье (а). Серый морской еж на восстановленном поле ламинарии (б)
Биотехнологии культивирования разрабатываются также и для других, не менее важных в промысловом отношении бурых водорослей - коста-рии и ламинарии цикориеподобной, позволяющие уже на первом году культивирования получать до 40—60 т костарии и на второй год культивирования до 80 т ламинарии цикориеподобной с одного гектара. Все эти мероприятия направлены на сохранение и увеличение запасов бурых водорослей, что должно обеспечить промышленность разносторонним сырьем для получения полезной продукции.
Фукоиданы и ферменты, катализирующие их превращения
Как известно, бурые водоросли морей Дальнего Востока России представляют собой богатый, легко возобновляемый источник уникальных по структуре и свойствам полисахаридов (ламинаранов, альгиновых кислот и фукой данов). Полисахариды являются главным компонентом биомассы водорослей и выполняют ряд важнейших биологических функций: служат энергетическим резервом, участвуют в построении клеточных стенок, образуют наружные капсулы и межклеточный матрикс, препятствуют дегидратации, создают барьер для проникновения в клетку солей из морской воды или, напротив, обеспечивают избирательное поглощение катионов, необходимых для построения минерального скелета. Основное внимание в нашей работе будет уделено фукоиданам - биологически активным сульфатированным полисахаридам, которые синтезируются бурыми водорослями, и аналоги которых до сих пор не обнаружены в наземных организмах.
Фукоиданы в последние годы стали объектом повышенного внимания и интенсивного исследования. Они представляют собой обширный класс биополимеров, содержание и структура которых варьирует в зависимости от вида водоросли, мест ее произрастания, сезона сбора и многих других факторов. Постоянно растущий интерес к этим полисахаридам объясняется их низкой токсичностью и разнообразной биологической активностью, которая может быть использована при создании медицинских препаратов нового поколения. Биологическая активность этих полисахаридов в отличие от их структуры изучается чрезвычайно интенсивно. Трудности в установлении структуры фукоиданов обусловлены влиянием на их структурные характеристики самых разнообразных факторов как внешних, так и внутренних, связанных с источником выделения. В силу недостатка информации о структуре биологически активных фракций фукоиданов сведения о связи структура/активность для этих полисахаридов в настоящее время практически отсутствуют.
Гистохимически фукоиданы определяются как основной компонент внеклеточного матрикса (ВКМ) концептакулов фукоидов (McCully, 1968; Speransky et al., 2001). Концентрация этих полисахаридов в ВКМ концептакулов в несколько десятков раз выше, чем в межклетниках сердцевины (Speransky et al., 2001). Для определения локализации фу-коидана было предложено использовать иммуноцитохимическую технику окрашивания. С помощью этого метода удалось обнаружить, что
35
фукоидан локализован в клеточных стенках. Однако он был обнаружен не только в эпидермальных клетках, но и во внутреннем кортикальном слое. Было показано, что в водоросли S. japonicaфукоидан сосредоточен в основном на расстоянии 50—150 мкм от поверхности слоевищ (Mizuno et al., 2009). Предполагается, что фукоиданы, благодаря их гигроскопичности, помогают в высвобождении репродуктивных клеток. Фукоиданы предохраняют растения, произрастающие на литорали, от высыхания и обеспечивают стабильность клеточных стенок (Mabeau et al., 1990). Предположительно, благодаря своим антиоксидантным свойствам (Ни et al., 2001; Le Tutour et al., 1998; Xue et al., 2001) фукоиданы могут защищать растения в естественных условиях от оксидативного стресса, вызванного флуктуациями температуры, света, солености и др. Обсуждалась также экранирующая функция фукоидана против высоких интенсивностей света и ультрафиолетовой радиации (Holtkamp, 2009).
Этот полисахарид был впервые выделен из бурых водорослей более 100 лет назад шведским ученым Килин (Kylin, 1913) из университета г. Упсала, который назвал его фукоидином. Непременным и часто главным компонентом молекул фукоиданов служат остатки сульфатированной a-L-фукозы. В состав фукоиданов обычно входят и другие моносахариды: галактоза, манноза, ксилоза, уроновые кислоты, а также ацетильные группы. Родственные биополимеры обнаружены в некоторых морских беспозвоночных (морских ежах и голотуриях), принадлежащих к типу иглокожих (Berteau, 2003). Полисахариды животного происхождения содержат только фукозу и сульфатные группы, и, соответственно, представляют собой сульфатированные a-L-фуканы, построенные из повторяющихся тетрасахаридных блоков.
Содержание фукоиданов в бурых водорослях колеблется в довольно широких пределах: от 0,4 до 20,4% - и зависит от вида водоросли и сезона сбора. Самое высокое содержание фукоидана (20,4%) было обнаружено А.И. Усовым с соавторами в Saundersellasimplex, принадлежащей к порядку Dicyosiphonales (Усов et al., 2001). Достаточно высокое содержание фукоидана наблюдается в водорослях порядка Fucales: от 13,4% до 16,5 %
— у Fucusvesiculosusи от 10,0% до 11,5% — у Ascophyllumnodosum(Репина et al., 2004). В дальневосточных представителях порядка Laminariales содержание фукоидана меньше: от 0,6 до 6,5%, а водорослях порядка Fucales
— от 1,5 до 7,9% (Имбс и др., 2009; Skriptsova et al., 2010). Такое различие в содержании фукоидана, предположительно, определяется сезонными изменениями абиотических факторов: температуры, концентрации элементов минерального питания, освещенности (Rioux et al., 2009), и зависит от репродуктивного статуса водоросли.
36
Фукоиданы, выделенные из одного вида водоросли, произрастающей в разных условиях, различаются не только моносахаридным составом, но и степенью сульфатирования. Известно, что фукоиданы из Laminariasaccharina, произрастающей в Баренцевом море, более сульфатированы и состоят из остатков фукозы и глюкуроновой кислоты, тогда как полисахариды беломорской популяции этой водоросли наряду с фукозой и глюкуроновой кислотой содержат глюкозу (Usov et al., 1998).
Фукоиданы хорошо растворяются в воде, поэтому их можно экстрагировать из водорослей водой (Zvyagintseva et al., 1999) или разбавленными кислотами (Hemmingson et al, 2006; Yoon et al, 2007) при комнатной температуре или небольшом нагревании. Для предотвращения экстрагирования альгинатов часто для экстракции используют 2% раствор хлорида кальция, который превращает содержащийся в водорослях альгинат в нерастворимую кальциевую соль (Bilan et al, 2002; Ponce et al, 2003). Для разрушения комплекса фукоидана с белком и облегчения экстракции полисахаридов иногда используются протеолитические ферменты (Rocha et al., 2005).
Бурые водоросли накапливают большое количество полифенольных соединений (до 14% от сухой массы водоросли (Ragan; Jensen, 1978)), которые, будучи прочно связанными с полисахаридами, уменьшают их растворимость в воде. Водоросли содержат и другие низкомолекулярные соединения, которые можно предварительно удалить обработкой биомассы органическими растворителями, например, смесью метанола, хлороформа и воды в соотношении 4:2:1. Такая смесь эффективно удаляет как полярные, так и неполярные вещества, но не растворяет полисахариды (Whyte; Southcott, 1970). Водные экстракты водорослей, как правило, содержат кроме фукоидана другие полисахариды: ламинаран, водорастворимые альгинаты, а также белки, полифенолы и прочие водорастворимые вещества. Фукоидан можно осадить из экстракта в виде нерастворимой соли с катионным детергентом — триметилцетиламмония бромидом (цетавлоном, цетримидом) (Bilan et al., 2002). Распространенным способом получения высокоочищенных фракций фукоиданов является ионообменная хроматография на различных анионообменных носителях (Chizhov et al., 1999). Новые анионообменные смолы, например, Macro Prep DEAE Support обладают большей емкостью и высокой разрешающей способностью по сравнению с традиционно используемыми ДЭАЭ-сефадексом и ДЭАЭ-целлюлозой. Более или менее гомогенные по отношению масса - заряд фракции иногда дополнительно очищают с помощью гель-фильтрации (Rocha et al., 2005). Процесс разделения контролируют, используя фенол-сернокислотный метод определения общих Сахаров, можно также использовать окрашивание сульфатированных полисахаридов раствором толуидинового синего.
37
Структуру фукоиданов, так же, как и структуры других полисахаридов, устанавливают при помощи классических методов углеводной химии, с применением современных физико-химических методов. Обычно исследование структуры включает в себя несколько этапов:
1. Установление качественного и количественного состава моносахаридов, из которых построен полисахарид. Идентификация и количественное определение неуглеводных заместителей (composition analysis).
2. Определение размера цикла, конфигурации гликозидного центра для каждого моносахаридного остатка, положения углеводных и неуглеводных заместителей (linkage analysis).
3. Определение последовательности моносахаридных остатков, обнаружение истинной или замаскированной регулярности полимера (sequence analysis).
Для определения моносахаридного состава чаще всего используют идентификацию моносахаридов после кислотного гидролиза полисахарида методом ГЖХ, реже ВЭЖХ. С нашей точки зрения, предпочтительнее является метод ВЭЖХ, т.к. при идентификации моносахаридов методом ГЖХ приходится проводить дериватизацию, например, получать ацетаты полиолов, что увеличивает трудозатраты и время анализа. Абсолютные конфигурации можно установить с помощью ГЖХ. Для этой цели получают ацетилированные или триметилсилилированные гликозиды в результате реакции моносахаридов с оптически активными спиртами.
С целью получения более точной информации о структуре исследуемого полисахарида чаще всего используют методы ЯМР- и ИК-спектроскопии. К сожалению, методы масс-спектрометрии пока неприменимы для больших сульфатированных молекул фукоиданов, однако, этот метод с успехом используется для установления структуры олигосахаридов -структурных фрагментов фукоиданов. ИК-спектры дают информацию о присутствии в полисахаридах сульфатных групп, о чем свидетельствует широкая полоса поглощения при 1240—1260 смл. Менее интенсивные полосы поглощения соответствуют сульфатам, находящимся в аксиальном (850 см4) или экваториальном (830 см_1) положениях. Спектры ЯМР нативных фукоиданов обычно слишком сложны и поэтому менее информативны, чем спектры их производных. Для получения интерпретируемых ЯМР спектров проводят химические модификации полисахарида с целью упрощения его структуры. Наиболее часто используют сольволитическое десульфатирование и/или дезацетилирование. Для десульфатирования полисахарид в виде


