Файл: 4 апта 40сра QU формуласы сйкес келеді изохоралык процесті жылулы эффектісі Формуласы арылы анытауа болады dSnr in V2V1 nr in P1P2.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 18.10.2024
Просмотров: 56
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
4 апта 40сұрақ
1.Q=∆U формуласы сәйкес келеді
+изохоралык процестің жылулық эффектісі
2. Формуласы арқылы анықтауға болады:
dS=nR In V2/V1 = nR In P1/P2
+изотермиялық
3. Идеал газдар үшін Ср мен Су арасындағы айырмашылық қандай:
+8,314 Дж/моль К
4. Жылу суық денеден ыстық денеге өте алмайды:
+термодинамиканың екінші заңы
5. Фазалық ауысу кезiнде энтропия өзгерісін қандай формуламен анықтайды:
+S = ∆Q/T
6. Изобаралык термодинамикалық процесске тән:
+QV = ∆H
7. Энтропияға S сәйкес келетін сипаттамаларды таңдаңыз:
+Жүйенің бір күйден екінші күйге ету жолына байланысты емес, бірақ жүйенің бастапқы және соңғы күйімен анықталады
8. Заттардың түзiлуi мен жануының стандартты жылу негiзiнде:
+Химиялық Реакциялардың жылуы;
9. р∆V көбейтіндісімен өлшенетін шаманың өлшем бірлігін көрсетіңіз
+Джоуль
10. Жүйенің күй функциясы жүйені жүргізу жолынан:
+ тәуелді емес
11. Энтропия:
+жүйенің тәртiпсiздiгiнiң сандық өлшемі
12. Қайтымсыз процестер үшін 2 термодинамика заңы:
+dS > dQ/T
13. Энтропия артады:
+Газ тәріздес өнімдердің көлемі өсуімен жүретін реакцияларда
14. Температураны өзгерткендегі реакцияның жылу эффектісінің өзгерісі жылу сыйымдылыққа тең болады:
+Кирхгофф заңы
15. Термодинамиканың екінші заңы процестерге қолданылады ...
+дене температурасының өзгеруімен
16. Қандай жүйелер ашық болуы мүмкін: *
+қоршаған ортамен жылу және материалдық алмасу мумкін болатын жүйелер
17. Әмбебап газ тұрақтысының (R) сандық мәні қандай?
+ 8, 314 Дж. Моль -1 К -1
18. Қандай процестің жұмысы оны жузеге асыру жолына байланысты емес:
+ тепе-теңдік процесі
19. Жылусыйымдылығын өлшеу бірліктерін таңдаңыз:
+ Дж/мольк
20. Изохоралық термодинамикалық процесске тән:
+ Qv = U
21. Температураның абсолюттік нөлге жақындағандағы дұрыс түзілген кристалдың энтропиясы қандай мәнге ұмтылады:
+ нөлге ұмтылады
22. Қайтымды процесс
+ тiкелей және кері бағытта жүруі мумкiн процесс
23. Термодинамиканың екінші басталу теңдеуі:
+ екінші типтегі мәңгілік қозғалтқышты құру мүмкін еместігі туралы постулаттың аналитикалық нысаны;
24. Оқшауланған жүйенің энтропиясы тепе-теңдікке жеткенде қалай өзгереді:
+ өседі және өзінің максималды мәнiне жетеді;
25. Химиялық реакцияға түсетін жүйенің жылу сыйымдылығын өзгерту арқылы анықтауға болады:
+ химиялық реакцияның жылу эффектінің температуралық коэффициенті;
26. Жүйенің ретсіздігін көрсететін шама:
+ Энтропия
27. Энтропия азаяды:
+ Газ тәріздес өнімдердің көлемі азаюмен жүретін реакцияларда.
28. TdS≥dU + р∆V теңдеуі мынаны көрсетеді:
+ энтропия процесс бағытының өлшемі ретінде оқшауланған жүйелер үшін ғана қолданыла алады.
29. Оқшауланған жүйе:
+ барлық жүйе дұрыс емес
30. Өздiгiнен жүретін үдеріс
+ сырткы денелердің әсерiнсiз үдеріс
31. TdS = PdV +dU бұл теңдеу:
+ Термодинамиканың екі бастамасының бірлескен
32. Термодинамиканың екінші заңы шағылыстырады...
+ жабык жуйелердегi Термодинамикалық процестердің бағыттылығы
33. Жылу суык денеден ыстык денеге өте алмайды:
+ термодинамиканың екінші заңы.
34. «Абсолютті нөлдегі жеке кристалды заттың энтропиясы нелге тең»
+ термодинамиканың үшінші Заңы
35. Термодинамиканың I және II заңының бірлескен теңдеуін көрсетіңіз:
+ dU > TdS – pdV
36. Энтропия бірліктерін таңдаңыз:
+ Дж/мольк
37. Келтірілген қайтымды процестердің қайсысында энтропия өзгерісі болмайды?
+ адиабаттық
38. Энтропия өзгерісі болатын реакцияны табыңыз:
2H2O=2H2 + O2
39. Оқшауланған жүйеде жүретін процесс бағытының өлшемі ретінде термодинамикалық функциялардың қайсысын қолдануға болады:
+S
40. Q = dН формуласы сәйкес келеді *
+ изобаралык процестің жылулык эффектісі.
5 апта 22сұрақ
µ=µ*+RTlnf теңдеуі:
+нақты газдың химиялық потенциалы
41. а мәнін мына формула бойынша есепптеуге болады:
+

42.Стандартты емес жағдайдағы химиялық потенциял анықталады:
+
43.Қандай теңдеуде қате бар:
+H=f(S.T)
44.Изобарлық-изоэнтропиялық потенциал
+H
45. Қай процесс қайтымды термодинамикалық процесс деп аталады?
+ жүйе сырттан қосымша энергияны қажет етпей, бастапқы күйіне келе алатын процесс
46.ү+- бұл...
+орташа активтілік коэффициенті
47.Қандай тұжырымдама тұжырымдамаға сәйкес келмейді-фугитивтілік....
+фугитивтілік жоғарғы қысымдағы процесте кезінде қысымның орнына қолданылады
48.Изобарлық-изотермиялық потенциал-
+G
49. ±a – бұл
+электролиттің орташа иондық активтілігі
50.Қандай тұжырымдамаға сәйкес келмейді-химиялық потенциал
+ бұл жүйенің ішкі энергиясының оның компоненттерінің массасының өзгеруіне байланысты өзгеруін анықтайтын шама
51.Қандай функцияларды термодинамикалық деп атайды?
+T,P,V,S
52.Изохоралық-изоэнтропиялық потенциял
+U
53.Активтілік, активтілік коэффициенті:
+нақты ерітінділер қасиеттерін сипаттау
54.Изохоралық-изотермиялық потенциял
+F
55. Қысым және температура тұрақты жағдайда химиялық тепе-теңдік шарты қай теңдеуде көрсетілген:
+dG=0
56.Кез-келген процесстің қарқындылық факторы .... аталады?
+Химиялық потенциал
57.Қандай праметрлер табиғи деп аталады?
+бұл мәндер жүйенің термодинамикалық күйіне тікелей сипаттама беретін параметрлер
58.Жүйенің бос энергиясының шексіз өзгерісінің жүйеге енгізілген компоненттің шексізт аз мөлшеріне қатынасы ....... құрайды.
+ жүйеде осы компоненттің химиялық потенциалы
59. Фугитивтілік (ұшқыштық) бұл-
+Жоғары қысымдағы идеал газдар үшін термодинамикалық қатынасты пайдаланып, реал газдардың қасиеттерін есептеу үшін қолданылатын термодинамикалық функция
60.Тепе-теңдік емес жүйелерде зат өздігінен өтеді.
+ химиялық потенциалы үлкен фазадан, химиялық потенциалы аз фазаға дейін
61.Активтіллік коэффициенті деп аталады...
+ идеал ерітіндегі компонет активтілік компонеттінің нақты ертіндегі концентрациясына қатынасы
6 апта 26сұрақ 4 еу жетпид
62.Бір уақытта қарма-қарсы бағытта жүретін реакциялар
+қайтымды
63.Химиялық реакцияның изохоралық теңдеуі
+ dlnKc/dT=U/RT2
64.Химиялық тепе-теңдік күйі сипатталады
+тура және кері реакциялар жылдамдығының теңдігі
65.Тепе-теңдік константасын білдіру әдісіне Гиббс энергиясының өзгеруі
+тәуелді емес
66.Температураның тепе-теңдік константасына әсер ету өлшемі:
+энтальпияның өзгеруі
67.Температураны төмендету тепе-теңдіктің.....реакцияға ауысуын тудырады.
+экзотермиялық
68.Соңына дейін жүретін реакциялар
+қайтымсыз
69.Тепе-теңдік күйінде
+ G=0
70.Қайтымсыз өздігінен жүретін процесстерге
+G<0
71.Қандай жағдайда реакция өздігінен жүре алмайды
+G>0
72.Интегралдық түрдегі изобаралық теңдеу
+
73.Химиялық тепе-теңдік күйінде туа реакция жылдамдығы .... кері реакция жылдамдығы
+тең
74.Қандай жағдайда тепе-теңдік константасы температураға тәуелді емес
+H=0
75.Температураның жоғарылауымен химиялық реакция жылдамдығының тұрақты мәні төмендейді ,тепе-теңдік жағына қарай жылжиды.........
+бастапқы зат
76.Идеал жүйелердегі Kp және Kc тепе-теңдік константаларына әсер ететін факторлар:
+әрекеттесетін заттардың табиғаты және температурасы
77.dln Kp/dT>0, онда реакция
+эндотермиялық
78.Қандай жағдайда реакция өздігінен алға бағытта жүреді?
+G<0
79.Динамикалық тепе-теңдік күйіндегі жүйеге катализаторды енгізу
+тікелей және кері бағытта жүреді ,жылдамдықтары бірдей
80.Қайтымсыз өздігінен жүретін процесстерге
+G<0
81.Температураның жоғарылауымен химиялық реакция жылдамдығының тұрақтысы жоғарылайды,тепе-теңдік жағына қарай жылжиды......
+реакция өнімдері
82.dln Kp/dT<0, онда реакция
+экзотермиялық
83. Kp және Kc тұрақтыларының химиялық тепе-теңдік арасындағы байланыс
+
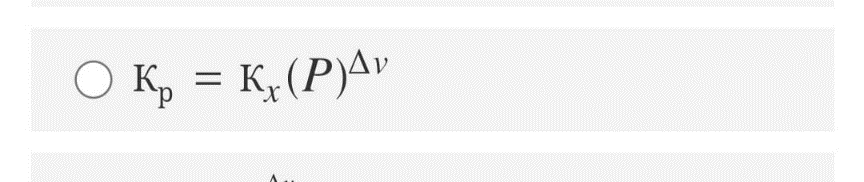
84.Химиялық реакцияның изобаралық теңдеуі
+dTlnKp/dT=H/RT2
85.Химиялық тепе-теңдік константасы(К)
+к1/к2
86.Егер жүйеге тепе-теңдік күйінде сыртқы әсер етілсе , онда тепе-теңдік осы әсердің әлсіреуіне қарай ауысады.
+ Ле-Шательенің ұстанымы
87.Егер тепе-теңдік константасы бірден кіші болса ,онда тепе-теңдік жүйесі басым болады
+бастапқы заттар
2 апта 36 сұрақ
88.Термодинамиканың бірінші заңы
+жылу кубылыстарына арналган энергиянын сакталу заңы
89.Термодинамика ғылымы нені зерттейді?
+жылу кубылыстарына арналган энергия сакталу заны
90.Берілген термодинамикалық жүйелерден гомогенді таңдаңыз:
+глюкоза ертындысы
91.Изобарлық процесте
+P=const
92.Менделеев-Клапейрон теңдеуі:
+PV=m/M*RT
93.Берілген термодинамикалық параметрлерден термодинамикалық функцияны таңдаңыз
+Т
94.Адиобаталық процесс кезінде жүйеде жұмыс неге тең?
+A=-ΔU
95.Идеал газдың жұмысы қай процессте нөлге тең?
+изохоралык
96.кДж/моль мөлшері өлшенеді
+∆H
97.Изотермиялық процесс кезінде жүйе энергиясы қалай анықталады?
+Q=A=m/MRTlnV2/V1
98. Экзотермиялық реакция үшін:
+ΔН < 0
99. Бөлшектердің былыққан соқтығысуы кезінде энергияны беру формасы
+Ышкы энергия
100. Изохоралық процесте
+V=const
101. Қысым 230мм сынап бағанасы.Атмосферадағы қысымды есептеңіз.
+0,3атм
+102.Универсал газ тұрақтысы (R)
8,314 дж/моль*к
103. Изотермиялық процесс үшін термодинамиканың бірінші заңының математикалық өрнегін көрсетіңіз
+Q=A
104.Изохоралық процесс үшін термодинамиканың бірінші заңының математикалық өрнегін көрсетіңіз
+Q=ΔU
105.Изохоралық процесте
+V=const
106.Термодинамиканың бірінші заңының анықтамасы:
+Жылу кубылыстарына арналган энергиянын сакталу заны
107.Екі атомды газдың жылу сыйымдылық формуласы
+Жылу кубылыстарына арналган энергиянын сакталу заны
108. Газ заңдары дегеніміз не?
+газдын быр параметрнын маны тагайындалып калган екы мандер арасындагы сандык тауелдылык
109.Газдың сығылу жұмысы оның ішкі энергиясының өзгерісіне тең . бұл қандай процеске сәйкес келеді?
+адиабаталык
110.Изотермиялық процесте
+T=const
111.Эндотермиялық реакция үшін
+ΔН >0
112.Егер сыртқы күштер идеал газбен , уақыттың кез келген мезетінде атқарылған жұмыс газдың қоршаған денелерге беретін Q жылу мөлшерінде тең болатындай етіп , жұмыс істесе ,онда бұл процесс....аталады.
+изохоралык
113.Жылу сыйымдылығын (Cv) таңдаңыз
+дж/моль*к
114.Майер теңдеуі
+Ср = Сv + Р
115.Тұрақты қысымдағы жүйе жылуларының өзгерісі қалай аталады?
+энтальпия
116.Қанадай процесс кезінде ең көп жұмыс атқарылады?
+изобаралык
117.Уақыттың кез келген мезетінде берілген жылу мөлшері газдың атқарған жұмысына тең болатындай етіп, идеал газға жылу берілу қай процесте жүзеге асырылады?
+изотермиялык
118.Интенсивті шамаларға жатады:
+тыгыздык концентрация температура
119.Бір атомды газдың жылу сыйымдылық формуласы
+U=3m/2M RT
120.Ішкі энергия дегеніміз не?
+Барлык молекулалардын кинетикалык энергиясымен осы болшектердн озараасерлесуынен потенциялдык энергиясынын косындысы
121.Изобаралық процесс үшін термодинамиканың бірінші заңының математикалық өрнегін көрсетіңіз
+Q=ΔU+A
122.Егер сыртқы күштер идеал газбен , уақыттың кез келген мезетінде атқарылған жұмыс газдың қоршаған денелерге беретін U жылу мөлшерінде тең болатындай етіп , жұмыс істесе ,онда бұл процесс....аталады
