ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 08.02.2024
Просмотров: 205
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Алъдегидтер — молекула құрамындағы сутек атомы альдегид тобына
О
(

 — С ) алмасқан көмірсутектердің туындылары.
— С ) алмасқан көмірсутектердің туындылары. Н
Альдегидтердің жалпы формуласы: R — С Н R – көмірсутек
радикалы. Радикал табиғатына байланысты альдегидтер қаныққан, қанықпаған және ароматты болып бөлінеді. Альдегидтер мен кетондардың касиеттері бір-біріне ұқсас. Сондықтан оларды ұқсастығы мен өзгешеліктерін салыстырып қарастырайық.
Атаулары және изомерленуі. Халықаралық атаулар жүйесі бойынша көмірсутектің атына -аль деген жалғау қосып атайды. Көміртек атомдары карбонил тобы жағынан бастап нөмірленеді. Тривиальді атау бойынша альдегидтерді өздері тотыққанда түзілетін қышқылдардың атымен атайды. Мысалы:
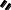
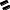 2 1 О 3 2 1 O
2 1 О 3 2 1 OСН3 — С СН3 —СН2 — С

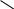 Н H
Н Hэтаналь пропаналь
(сірке альдегиді) пропион альдегиді
Альдегидтердің изомерленуі көмірсутек қаңкасының құрылысына байланысты және класаралық (кетондармен) изомері болады. Мысалы, С4Н8О изомерлері:
О О
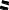
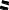
СН3 —СН2 — СН2 — С СН3 —СН2 — С

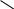
Н СН3 Н
бутаналь 2-метилпропаналь
(н-май альдегиді) (изомай альдегиді)
О

СН3— СН2— С — СН3 бутанон-2
Кетондардың изомерленуі көміртек радикалының құрылысына және карбонил тобының орнына байланысты болады:
1 2 3 4 5 1 2 3 4 5
СН3— С— СН2 — СН2 — СН3 СН3 СН2— С —СН2СН3
пентанон-2 пентанон-3
(метилпропилкетон) (диэтилкетон)
Басқа қосылыстар сияқты карбонилді қосылыстардың физикалық және химиялық касиеттерін сипаттау үшін олардың электрондық құрылысын ескеру керек. Карбонил тобындағы көміртек атомы sр
2-гибридтенген. Онымен байланысқан атомдар бір жазықтықта жатады. Арасындағы бұрышы 120°. Карбонил тобындағы қос байланыстың алкендердегі байланыстан өзгешелігі — ол электртерістігі әр түрлі атомдар арасында түзілген. Электрон тығыздыры электртерістігі жоғары оттек атомына қарай ығысқан. Осыдан оттек атомында электрон тығыздығы көбейіп, көміртек атомында азаяды да, полюстену пайда болады.
О
Ацетон СН3—С—СН3 түссіз сұйықтық, сумен кез келген мөлшерде араласады. Еріткіш ретінде кең түрде қолданылады, органикалық синтезде изопрен, ацетат талшығын және т.б. алады. Әсіресе нитроцеллюлоза, ацетилцеллюлозаны еріту үшін пайдаланылады.
Молекулаларында көмірсутек радикалдарымен байланысқан альдегид тобы бар органикалық қосылыстарды альдегидтер деп атайды. Альдегидтердің ең қарапайым өкілі метаналь СН2=О (формальдегид). Альдегидтер тотығу-тотықсыздану реакцияларына түседі. Альдегид тотығып — карбон қышқылына, тотықсызданып — спиртке айналады. Альдегидтер қосылу реакциясына түседі. Реакция қос байланыс үзілу арқылы жүреді. Альдегидтердің полимерлену және поликонденсациялану реакцияларының нәтижесінде пластмассалар алынады. Құмырсқа альдегиді мен сірке альдегидінің өндірісте маңызы өте зор. Одан сірке қышқылын, этил спиртін және көптеген органикалық қосылыстар алады.
Ацетон, диметилкетон, СН
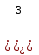 СОСН
СОСН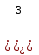 – иісі бар, түссіз, жанғыш сұйық зат. Балқу t – 94,9°С, қайнау t 56,2°С. Су, спирт, күрделі эфир, түрлі май, бензин және органик. еріткіштермен кез келген мөлшерде араласады. Сілті қатысында галогендермен әрекеттеседі. Ацетон — жалыны түссіз, өзіне тән иісі бар мөлдір сұйық зат. Көптеген органикалық заттарды жақсы ерітеді. Эмаль, лакті (оның ішінде тырнаққа жағылған лакті де) ерітуге, қатты заттардың бетіне жұғып қалған майлы бояулар мен киімге жұққан майлы дақтарды кетіруге пайдаланылады. (Дацты кетіру мақаласын қараңыз). Ацетон аңетат талшықтарды да ерітетін болғандықтан, одан тоқылған маталарды тазарту үшін, алдымен сол матаның кішкене бөлігіне әсерін байқап алған дұрыс. Ацетат маталар аңетонның әсерінен еріп кетуі немесе қаудырлап күйіп қалуы мүмкін. Ацетон өрт қаупін туғызатындықтан, оны оттан алыс ұстау керек.
– иісі бар, түссіз, жанғыш сұйық зат. Балқу t – 94,9°С, қайнау t 56,2°С. Су, спирт, күрделі эфир, түрлі май, бензин және органик. еріткіштермен кез келген мөлшерде араласады. Сілті қатысында галогендермен әрекеттеседі. Ацетон — жалыны түссіз, өзіне тән иісі бар мөлдір сұйық зат. Көптеген органикалық заттарды жақсы ерітеді. Эмаль, лакті (оның ішінде тырнаққа жағылған лакті де) ерітуге, қатты заттардың бетіне жұғып қалған майлы бояулар мен киімге жұққан майлы дақтарды кетіруге пайдаланылады. (Дацты кетіру мақаласын қараңыз). Ацетон аңетат талшықтарды да ерітетін болғандықтан, одан тоқылған маталарды тазарту үшін, алдымен сол матаның кішкене бөлігіне әсерін байқап алған дұрыс. Ацетат маталар аңетонның әсерінен еріп кетуі немесе қаудырлап күйіп қалуы мүмкін. Ацетон өрт қаупін туғызатындықтан, оны оттан алыс ұстау керек.
Кетондар - құрамында екі көмірсутек радикалымен байланысқан карбонил тобы >C=O бар органикалық қосылыстар класы. Жалпы формуласы RCOR^1. Кетондар алифатты, алициклді, ароматты немесе гетероциклді қатарларға бөлінеді. Алифатты қатардағы ең қарапайым кетондар - ацетон CH
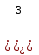 COCH
COCH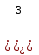 , ароматты қатарда - бензофенон C
, ароматты қатарда - бензофенон C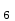 H
H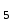 COC
COC H
H . Кетондар органикалық еріткіштерде жақсы ериді. Кетондар реакцияларын екі түрге бөледі:карбонилге қосылу реакциялары (сутектің, көгерткіш қышқылдың т.б. қосылуы); карбонил топтағы оттектің орнын басу реакциялары (галогендермен, гидроксил амимен т.б. алмастыру). Кетондарды алу әдістері альдегидтерге ұқсас. Оны екіншілік спирттерді тотықтыру, карбон қышқыл тұздарын құрғақ айдау т.б. әдістермен алады. Кетондар еріткіштер ретінде және түрлі органикалық синтезде кеңінен қолданылады.
. Кетондар органикалық еріткіштерде жақсы ериді. Кетондар реакцияларын екі түрге бөледі:карбонилге қосылу реакциялары (сутектің, көгерткіш қышқылдың т.б. қосылуы); карбонил топтағы оттектің орнын басу реакциялары (галогендермен, гидроксил амимен т.б. алмастыру). Кетондарды алу әдістері альдегидтерге ұқсас. Оны екіншілік спирттерді тотықтыру, карбон қышқыл тұздарын құрғақ айдау т.б. әдістермен алады. Кетондар еріткіштер ретінде және түрлі органикалық синтезде кеңінен қолданылады.Маңызды альдегидтер
| Аты | Формула | Балқу | Қайнау температурасы |
| Формальдегид | HCHO | −92 °C | −19 °C |
| Ацетальдегид | CH3CHO | −123 °C | 20,8 °C |
| Пропаналь | CH3CH2CHO | −81 °C | 48,8 °C |
| Бутаналь | CH3CH2CH2CHO | −97 °C | 75 °C |
| Акролеин | CH2=CH-CHO | −88 °C | 52,5 °C |
| Кротонды альдегид | CH3-CH=CH-CHO | −76,5 °C | 104 °C |
| Бензальдегид | C6H5-CHO | −56 °C | 179 °C |
Дәріс:15
Тақырыбы: Күрделі эфирлер. Майлар. Көмірсулар. Дисахаридтер. Сахароза. Крахмал.
Мақсаты: Жай және күрделі эфирлер туралы ұғымдарын тереңдете отырып, құрамы, құрылысы, атаулары, изомерлері, қасиеттерін түсіндіру.
Жоспары:
-
Эфирлер. Жай және күрделі эфирлер. -
Қазақстандағы май, қант, целлюлоза өндірісі.
Эфирлер-құрамында оттек бар органикалық қосылыстар; спирттер молекуласындағы гидроксил тобының сутек атомын радикалға алмастырғанда эфирлер алынады. Олар жай және күрделі эфирлер болып негізгі екі топқа бөлінеді. Жай эфирлердің жалпы формуласы R – O – R немесе R– O– R' (R, R' – органикалық радикалдар). Екі радикалы бірдей жай эфирлер – симметриялы эфирлер, радикалдары әр түрлі жай эфирлер аралас эфирлер деп аталады.
Күрделі эфирлер – қышқыл құрамындағы сутек атомын (карбон қышқылдарындағы карбоксил тобының сутек атомын) алкил немесе арил радикалдарымен алмастырғанда түзілетін қосылыстар. Күрделі эфирлер спирттер органикалық карбон қышқылдарымен әрекеттескенде түзіледі, реакцияны эфирлеу деп атайды, реакция қайтымды. Катализатор ретінде қышқылдың сутегі ионы алынады. Күрделі эфирлерді алудың кең тараған әдістеріне эфирлену (қышқыл мен спирттің әрекеттесуі) реакциясы жатады. Бұл – белгілі бір сатысында тепе-теңдік күйге келетін қайтымды реакция. Күрделі эфирлердің ең маңызды химиялық қасиеттерінің бірі – сабындану реакциясы (гидролиз). Күрделі эфирлер табиғатта кең таралған. Олардың көбі эфир майларының құрамында болады. Глицерин мен май қышқылдарының күрделі эфирлері табиғи майлардың негізін құрады. Күрделі эфир техниканың, өндірістің әр түрлі салаларында кең қолданылады. Мысалы, күкірт қышқыл күрделі эфирлері алкилдеу реакцияларында, қағаз өндірісінде, фосфор қышқыл күрделі эфирлері өсімдіктер зиянкестеріне қарсы қолданылады. Кейбір эфирлер тамақ және парфюмерия өндірісінде, дәрі-дәрмек дайындауда, органикалық шыны жасауда, еріткіш ретінде, т.б. қолданылады. Күрделі эфирлер табиғатта кең тараған. Олар биологиялық өте маңызды қосылыстар. Гүлдер мен жемістердің құрамында күрделі эфирлер болуына байланысты олардың хош иістері болады. Өсімдік және жануарлар майлары күрделі эфирлерге жатады. Карбон қышқылдарының күрделі эфирлерін қышқылдардың карбоксил тобындағы сутек атомының орнын көмірсутек радикалы басқан сутектің немесе спирттердегі гидроксил тобының орнын
органикалық қышқылдың радикалы басқан туындылар деп қарастыруға болады.
Атаулары. Күрделі эфирлердің аттары олардың құрамына кіретін қышқылдар мен спирттердің қалдығынан құралады (27-кесте). Халықаралық номенклатура бойынша қышқылдың атына спирт радикалының атын қосымша етіп, - оат жалғауын жалғап атайды:
H - COOC2H5 - құмырсқа қышқылының этил эфирі (этилформиат немесе метилметаноат)
CH3 - COOC2H5 сірке қышқылының этил эфирі (этилацетат немесе этилэтаноат)
Күрделі эфирлердің изомерлерін оны құруға қатысқан қышқыл мен спирттің радикалдарына байланысты топтардың изомерленуі бойынша анықтайды. Күрделі эфирлер карбон қышқылдарымен класаралық изомерлер. Мысалы, С3Н6O2 изомерлері:HCOO C2H5 – этилформиат.
Алынуы:
1.Күрделі эфирлер көбіне табиғи өнімдерден алынады.
2.Этерификация реакциясында карбон қышқылдары мен спирттерді минерал қышқылдар қатысында әрекеттестіріп, нәтижесінде, күрделі эфир мен су түзіледі. Эфирлену реакциясы кезінде карбоксил тобының гидроксилі мен спирт молекуласындағы сутектен су молекуласы түзілетіні реакцияға изотоптар енгізу арқылы анықталды. Құрамында оттектің 180 изотопы бар спиртпен әрекеттестіргенде, оттектің ауыр изотопы судың емес күрделі эфирдің құрамында екендігі белгілі болды:
Физикалық қасиеттері. Қарапайым карбон қышқылдарының күрделі эфирлері түссіз сұйықтықтар, суда ерімейді. Күрделі эфирлердің көбінің иістері жағымды. Молекула арасында сутектік байланыс жоқ болғандықтан, сәйкес қышкылдарға қарағанда күрделі эфирлердің қайнау температуралары төмен болады.
Химиялық қасиеттері.
Гидролиздену реакциясы. Күрделі эфирлердің гидролизі этерификация реакциясына кері реакция, қышқыл немесе сілті қатысында жүреді. Күрделі эфир сумен әрекеттесіп айырылып, реакция нәтижесінде қышқыл және спирт түзіледі:
CH3COOC2H5 + H2O → CH3 - COOH + C2H5OH
Диэтил эфирі С2Н5—О—С2Н5. Оңай қайнайтын (34,6°С) сұйық зат, суда ерімейді, судан жеңіл, өзіне тән иісі бар. Ауамен қопарылғыш қоспа түзеді. Еріткіш ретінде, жасанды жібек алуға, медицинада наркоз жасауға қолданылады.

