Файл: Кейс 1 Орта мектепте химияны оытуды масаттары, оушылара химиялы орта білім беруді міндеттері.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.04.2024
Просмотров: 50
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
-
7 сынып «Негіздік және қышқылдық оксидтердің түзілуі» 8 сынып «Оксидтер»
7 сыныпта «Негіздік және қышқылдық оксидтердің түзілуі» тақырыбы тәжірибе жүзінде түсіндірілген. Металл және бейметалл оксидтерінің сипаты бойынша қорытынды шығарылған. Сәйкесінше, металл оксидтері -негіздік оксид, беметалл оксидтері-қышқылдық оксид болып табылатындығын тәжірибе жүзінде көрсеткен.
8 сынып «Оксидтер» тақырыбында оксидтерге анықтама беріліп олардың жіктелуі мен аталуы түсіндіріліп, оксидтерді алу әдістері қарастырылған. Осидтердің жіктелуі кесте түрінде беріліп,мысалдар келтірілген. Оксидтері алудың 3 түрі қарастырылған және кесте түрінде мысалдар келтірілген.
-
Массасы 260 г ацетилен C2H2 толық жанғанда түзілетін көміртек диоксидінің массасын есептеңіздер
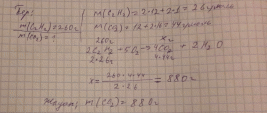
Кейс 5
-
Химиялық номенклатураның түрлері және олар оқыту барысында қалай пайдаланылады
Химиялық номенклатура әртүрлі химиялық қосылыстарды оларды құрайтын элементтердің типі мен санына қарай атауға мүмкіндік беретін ережелер жүйесі деп аталады. Номенклатура химиялық қосылыстарды анықтауға, жіктеуге және жүйелеуге мүмкіндік береді.
Химиялық номенклатураның мақсаты - химиялық заттарға дескриптор деп аталатын атаулар мен формулаларды тағайындау, олар оңай танылып, конвенцияны біріктіруге болады.
Химиялық номенклатура бойынша қосылыстардың екі үлкен тобы ажыратылады:
-
Органикалық қосылыстар сутегі, оттегі, күкірт, азот, бор және галогендердің молекулаларына байланысты көміртегі барларға қатысты; -
Бейорганикалық қосылыстар, бұл көміртек молекулаларын қамтымайтын химиялық қосылыстардың бүкіл әлеміне сілтеме жасайды.
Конвенцияларды реттейтін немесе белгілейтін негізгі мекеме - Халықаралық таза және қолданбалы химия одағы немесе IUPAC.
-
Тривиалды аталымдар (Тривиальные названия) - химия дамуының ерте сатыларында қолданылған химиялық заттардың аталымы. Тривиалды атаулардың мысалдары: ашудастар, мыс купоросы (тотыяйын), әк, бор, т.б. -
Дәстүрлі аталымдар (Традиционные названия) - химиялық құрамын көрсететін химиялық заттардың аталымы; бұл тәсіл жүйелі атауларға дейін қолданылған. Кейбір дәтүрлі атаулар кейде жүйелі атаулармен бірдей болады. Дәстүрлі атауларға мысалдар: мыс сульфаты, қорғасын нитраты және т.б. -
Жүйелі аталымдар (Систематические названия) - химиялық қосылыстардың бүгінгі аталымы. Қосылыстардың жүйелі атауларында оны құрайтын атомдардың не топтардың аты, олардың саны келтіріледі. Бейорганикалық қосылыстар үшін металдың не катионның тотығу дәрежесі көрсетіледі, ал қышқыл қалдық не анион маңызды құрамдас элементінің тотығу дәрежесімен (валенттілігімен) сипатталады. Мысалы: мыс (ΙΙ) сульфаты, темір (ΙΙΙ) сульфаты, калий манганаты (VΙΙ). Органикаық қосылыстар үшін жүйелі атаулары оларға сәйкес алкандардан туындайды. Мысалы этан қышқылы өз аталуын этаннан алған: этан қыщқылы-сірке қышқылылның жүйелік аталуы.
| Сабақтың жоспарланған кезеңдері | Сабақтағы жоспарланған жаттығу түрлері | Ресурстар |
| Сабақтың басы 8 мин | Ұйымдастыру кезеңі Топқа бөлу: Оқушылар қораптың ішінен белгілі бір ұяшықтарды таңдап 3 топқа бөлінеді. (ұяшықтарда хим.ыдыстардың 3 түрі берілген) | Суреттер мен ұяшықтар Қағаз қиындылары |
| Сабақтың ортасы 32 мин | Жаңа сабақты түсіндіру Номенклатура-қандай да бір ғылымдағы атаулар жүйесі Органикалық химияда тривиалды,рационалды және жүйелік атаулар қолданылады. Қазіргі уақытта халықаралық теориялық және қолданбалы химия одағы шығарған жүйелік атаулар қолданылады.Бұл атаулар жүйесі ИЮПАК номенклатурасы деп аталады. Қаныққан көмірсутектердің алғашқы төрт мүшесі тривиалды атқа ие: метан,этан,пропан және бутан. Олардан кейінгілерінің атаулары грек сандарына –ан жалғауы жалғануы арқылы жасалады: С5Н12-пентан, С6Н14- гептан және т.б. Егер алкан молекуласынан бір атом сутекті үзіп тастаса бір валентті қалдық-көмірсутек радикалы түзіледі. Алкандардың бір валентті радикалдарының жалпы атауы-алкилдер.Алкилдер атауы –ан жалғауын –ил жалғауына алмастыру арқылы жасалады: метан-метил, этан-этил т.б.  Бір қос байланысы бар тармақаталмаған көмірсутектердің атауы сәйкес қаныққан көмірсутектегі –ан жұрнағын –ен жұрнағына алмастыру арқылы жасалады: CH2=CH2 этен Бір үш байланысы бар тармақталмаған қанықпаған көмірсутектерді (алкиндер) сәйкес қаныққан көмірсутектегі –ан жұрнағын –ин жұрнағына алмастырады. Спирттер-көмірсутек құрамындағы сутек атомының орнын гидроксил топтары алмастырған көмірсутек туындылары.Оларды атау үшін сәйкес көмірсутекке –ол жұрнағы жалғанады. Альдегидтер-молекула құрамындағы сутек атомы альдегид тобына алмасқан көмірсутектердің туындылары. Көмірсутекке –аль жұрнағын жалғау арқылы аталады. Карбон қышқылдары-молекуласында бір немесе бірнеше карбоксил тобы бар көмірсутектердің туындылары. Кері байланыс орнату. 1) Сабақ түсінікті болды ма? 2) Түсінбегендеріңіз бар ма? «2 жұлдыз - 1ұсыныс» арқылы бағалау. Сергіту сәті. (Қызықты қимыл қозғалыстары) | Электрондық оқулық (оқу жоспарындағы сайт) Бақылау парағы Химиялық құрал-жабдықтар, реактивтер |
-
Массасы 37 г нитробензол сутек қатысында тотықсыздандырғанда 18,5 г анилин алынған. Анилиннің шығымы қандай?

Кейс 6
-
8 класс бойынша оқушылардың білімі мен білігіне қойылатын талаптарды сипаттаңыз
Оқушылардың білімі мен білігі олардың алған білімін қаншалықты игере алғаны жайлы ақпарат береді. Оқушылардың білімі мен білігін тексеру арқылы мұғалім сабақ түсіндірудегі кемшіліктері жайлы ақпарат алады. Ол бойынша қателіктерін түзете алады. Оқушылардың біліміі мен білігін тексеру әдістері күнделікті,дүркінді және қорытынды болып бөлінеді.
8 сынып оқушыларының білімі мен білігін тексеруге қойылатын талаптар:
-
Жүйелілік -
Жан-жақтылық -
тапсырмаларды, сұрақтарды шешуде жаңа білімді дұрыс қолдану; -
өз көзқарасын дәлелдей алады, белгілі бір шешіммен келіседі немесе келіспейді, шығармашылық мәселелерге өз шешімін ұсына алады.
Күнделікті өткен тақырыптан жаңа ой түйе алады
-
8 сынып «Химиялық реакциялар типтері» 9 сынып «Қайтымды және қайтымсыз реакциялар»
| Химиялық реакция типтерімен (қосылу,айырылу,орынбасу,алмасу) танысады. Олардың әрқайсысына мысал келтіріп,ерекшеліктерін анықтайды. | Қайтымды және қайтымсыз реакция ұғымдарымен танысып, олардың мәнін түсінеді.Оларға мысал келтіріп, ерекшеліктерін аанықтайды. Химиялық тепе теңдік ұғымымен танысады. Реакцияның жүру бағытына байланысты тура немесе кері болуын анықтайды. |
-
Құрамында 40% C, 6,6% H, 53,4% O болатын карбон қышқылының молекулалық формуласын табыңыздар
1) возьмем массу этого в-ва за 100 грамм, тогда:
масса (с)=40г
масса (Н) =6.6г
масса(О)=53.4г
2) теперь расчитаем количество каждого из составляющих:
n(С)=40:12=3,3моль
n(Н)=6.6:1=6,6моль
n(О)=53,4:16=3.3 моль
3) теперь видим, что количества элементов относятся, как 1:2:1, то есть СН2О-простейшая формула вещества, но так как в карбоновой кислоте не может быть одного атома кислорода, умножим все на 2. Получаем: С2Н4О2 или СН3-СООН.это уксусная кислота.
Кейс 7
-
Сабақ қандай негіздерге сүйеніп жіктеледі? Галогендер тақырыбының сабақтарын типтерге және түрлерге жіктеп көрсетіңіз
Химияны оқыту методикасының оқулықтары мен оқу құралдарына химия сабақтары типтерге, түрлерге және нұсқаларға жіктеледі.
Химиядан сабақ беру методикасынан дидактикалық міндеті бойынша химия сабақтарын бес типке бөледі:1) жаңа білім мен білікті игеру(жаңа материалды оқып үйрену); 2) теориялық білім мен білікті жетілдіру және қолдану; 3) білімді қорыту және жүйеге түсіру;4) бақылау−есепке алу; 5) аралас сабақтар;
Жаңа материалды оқып үйрену сабақтары дәріс сабағы, әңгіме сабағы кітаппен жұмыс істеу сабағы,үйлестіріліп берілетін материалдармен жұмыс істеу сабағы болып бөлінеді.
Сабақтың екінші типіне оқушылардың алған білімін жетілдіру сабақтарын қайталау, қорытындылау, жүйеге түсіру және сарамандық сабақтар жатады.
9 сыныптағы Галогендер тақырыбы 8 сыныпта алған білімді одан әрі тереңдетіп қайталау. Сондықтан ол химия сабақтарының екінші типіне, яғни теориялық білім мен білікті жетілдіру және қолдану сабағы. Ал оның ішінде қайталау сабағына жатады.
-
Хлордың химиялық сипаттамалары
Хлор - периодтық жүйенің VII тобының негізгі топшасының химиялық элементі. Ол үшінші периодта және 17 атом нөміріне ие (атом ядросында 17 протон). Металл емес реактивті. Ол Cl әріптерімен белгіленеді.
Бұл галогендердің типтік өкілі. Бұл түссіз, бірақ өткір өткір иісі бар газдар. Әдетте улы. Барлық галогендер суда тез сұйылтылады. Ылғал ауамен байланысқан түтін.
Cl атомының сыртқы электрондық конфигурациясы 3s2 3p5 құрайды. Сондықтан қосылыстарда химиялық элемент -1, + 1, +3, +4, +5, +6 және +7 деңгейлерін көрсетеді. Атомның ковалентті радиусы 0,96 Ом, иондық радиусы 1,83 Ом, атомның электронға жақындығы 3,65 эВ, иондану деңгейі 12,87 эВ.
Жоғарыда көрсетілгендей, хлор кез-келген металдармен (кейбір жағдайларда бромды ығыстыру кезінде қыздыру немесе ылғалды қолдану арқылы) және бейметалдармен қосылыстар құруға мүмкіндік беретін жеткілікті белсенді металл емес. Ұнтақ түрінде ол металдармен тек жоғары температура әсер еткенде ғана әрекеттеседі.
Жанудың максималды температурасы - 2250 ° C. Ол оттегімен оксидтер, гипохлориттер, хлориттер және хлораттар түзе алады. Құрамында оттегі бар барлық қосылыстар тотықтырғыш заттармен әрекеттескенде жарылғыш болады.Хлор оксидтері өздігінен жарылуы мүмкін екенін ескеру керек, ал хлораттар кез-келген инициаторларға әсер еткенде ғана жарылады.
-
Құмырсқа альдегидін күміс оксидімен тотықсыздандырғанда, 2 г күміс түзіледі. Альдегидтің қандай массасы тотыққан?
Уравнение:
HCOH + Ag2O = HCOOH + 2Ag
Рассчитаем количество вещества серебра:
n = m/M = 2г/108г/моль = 0,0185моль
По уравнению реакции:
n(HCOH) = 1/2n(Ag) = 0,0093моль
Масса:
m = n*M = 0,0093моль*30г/моль = 0,28 грамм
Кейс 8
-
Химияның алғашқы ұғымдарын екі жүйе бойынша жіктеп, сызбанұсқа сызыңыздар: а) зат ұғымдарының жүйесі; ә) химиялық реакция ұғымдарының жүйесі
| зат ұғымдарының жүйесі | химиялық реакция ұғымдарының жүйесі. |
| Орта мектептегі химия курсында «химиялық реакция» ұғымының компоненттері нақты ажыратылады:
| Орта мектептегі химия курсында «химиялық реакция» ұғымының 6 компоненті нақты ажыратылады, олар бірлікте қарастырылып, біртіндеп қалыптасады: 1. Реакциялардың мәнін көрсететін белгілер. 2. Пайда болу заңдылықтары мен ағымы. 3. Сандық сипаттамалар. 4. Классификация. 5. Практикалық қолдану. 6. Зерттеу әдістері. |
-
Заттардың (металдар және бейметалдар) физикалық қасиеттерін танып білу. Физикалық және химиялық құбылыстар.
Мақсаты: жай және күрделі заттардың физикалық қасиеттерін зерттеу, Химиялық және физикалық құбылыстарды анықтау.Химиялық және физикалық құбылыстардың ұқсастығы мен айырмашылығын ажыратып білу, заттардың өзгерістерін сипаттау.
Қажетті құрал-жабдықтар: химиялық заттардың үлгілері: темір Fe, мыс купорос CuSO4 ∙ 5H2O, күкірт S, мүсәтір спирті NH4OH, алюминий Al, көмір C, ас тұзы NaCl, малахит Cu2(OH)CO3, мыс сым Cu, әк CaO.
Тапсырма № 1
Берілген заттардың ұлгілерін қарап, жай және күрделі заттарға жіктеңдер. Физикалық қасиеттерін зерттеп таблицаға жазыңдар.
Агрегаттық күйі: қатты, сұйық, газтәрізді.
Тұсі: сары, қара, түссіз.
Иісі: иісі бар, жоқ.
Суда ерігіштігі: жақсы ериді, аз ериді, ерімейді.
Температура: қайнау, балқу.
Тапсырма №2
1. Мыс сымының кішкене бөлігін алып,балғамен ұрып жаншу.
2. Сымның пішіні өзгергеніне назар аудару.
3. Мыс сымының кішкене бөлігін ұстағышпен қысып, спиртшамының жалынына ұстау.
Сұрақтарға жауап беру:
