ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 05.05.2024
Просмотров: 192
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
S. japonica(Zvyagintseva et al., 2003), S. gurjanovae(Шевченко и др., 2007) и U. pinnatifida(Lee et al., 2004) также относящихся к отряду Laminariales. При исследовании фукоидана обеими группами исследователей применялись одни и те же методы: десульфатирование и метилирование с последующим анализом производных фукоидана с помощью ЯМР-спектроскопии.
Для анализа фукоидана, выделенного по методу (Zvyagintseva et al., 2003) из S. cichorioides, собранной в шельфовой зоне российского побережья Японского моря, мы применили два метода масс-спектрометрии - тан-демный ИЭР МС в режиме столкновительной диссоциации, который положительно зарекомендовал себя при анализе фукоолигосахаридов из A. nodosumи F. evanescensи тандемный МАЛДИ МС, которым ранее не анализировали сульфатированные фукоолигосахариды в режиме МС/МС отрицательных ионов (точнее режим называется potential lift TOF/TOF, где вторичные ионы образуются при скачкообразном подъеме ускоряющего напряжения и регистрируются вторым времяпролетным анализатором). Использование МАЛДИ МС для полианионных олиго-сахаридов сопряжено с определенными трудностями, поскольку сульфатные группы очень лабильны и могут отрываться в источнике ионов. Нами было найдено, что использование фенилозазона D-эритро-жптозы (arabinoosazone в оригинальной статье (Chen et al., 1997)) в качестве матрицы позволяет минимизировать фрагментацию.
Образец высокосульфатированного фукоидана LcF2 (Fuc, 98%, Man, 2%.), выделенный по методике (Zvyagintseva et al., 2003), был подвергнут автогидролизу. Этанольный экстракт продуктов автогидролиза Lc-AHL (выход 66% от образца LcF2) был проанализирован с помощью масс-спектрометрии ИЭР (рис. 3.10) и МАЛДИ (рис. 3.11) в режиме регистрации отрицательных ионов.
74
I J 8 S
Е I «,-Г1
ё2о Я§
QJf-Ml
220
СЛ
-U±
520 m/z
Рис. ЗЛО. ИЭР масс-спектр отрицательных ионов олигосахаридов, полученных автогидролизом фукоидана из бурой водоросли S. cichorioides
и
50 А
0 1|лЦ4|1ц1,к,,|]|„ L,,L,.....I
*i+
500
Ю |
200
300
400
600
700
800
900 m/z
Рис. 3.11. МАЛДИ масс-спектр отрицательных ионов олигосахаридов, полученных автогидролизом фукоидана из бурой водоросли S. cichorioides
Анализ масс-спектров, полученных двумя методами, дал следующий состав смеси: моносульфат и дисульфат фукозы с
m/z243.0 и 344.9 (основные компоненты) и набор олигосахаридов со степенью полимеризации 2—5 и числом сульфатов на молекулу до 3. Стоит отметить, что интенсивность сигнала иона дисульфатированной фукозы с m/z344.9 была выше при регистрации состава смеси методом МАЛДИ МС.
Далее были получены тандемные масс-спектры большинства ионов, находящихся в смеси. Для того, чтобы идентифицировать фрагментные ионы, имеющие одинаковое значение m/z, но возникающие из восстанавливающего либо невосстанавливающего концов молекулы, образец был восстановлен NaBD4. В результате, ионы, сохраняющие заряд на
75
восстанавливающем конце (Y-ионы), имели на 3 Da большую массу и были идентифицированы однозначно. Полученные данные совпали с результатами исследований фрагментации олигосахаридов каррагинана с помощью ИЭР МС/МС, где было четко показано, что наличие сульфатной группы в остатке сахара провоцировало образование соответствующих Y-ионов, в то время как В- и С-ионы могли образовываться при разрыве гликозидных связей также и между несульфатированными остатками Сахаров (Yu et al., 2006). В тандемных масс-спектрах олигосахаридов из S. cichorioid.esС-ионы практически не наблюдались.
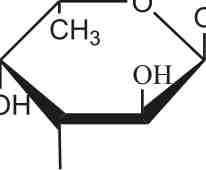
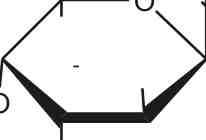
На рисунках 3.12 и 3.13 показаны наиболее информативные тандемные масс-спектры дисульфатированной фукобиозы, полученные разными масс-спектрометрическими методами. Тандемный масс-спектр ИЭР (рис. 3.12) двухзарядного иона [Fuc2(S03Na)2-2Na]2" с m/z234.011 содержал интенсивные сигналы ионов с В с m/z225.007 и Y с m/z243.017 формирующихся при разрыве гликозидных связей. Та же картина повторилась и в тандемном МАЛДИ масс-спектре (рис. 3.13), где интенсивности указанных сигналов примерно совпадали. Отсюда следует, что сульфатные группы находились в среднем по одной на восстанавливающем и на невосстанавливающем остатках фукозы. Сигналы 0,2Х0/0,2А0, имеющие высокие интенсивности в ИЭР МС/МС спектрах фукоолигосахаридов из A. nodosum, содержащих большой процент (1^4)-связанных остатков фукозы, в данных масс-спектрах имеют гораздо меньшие интенсивности, особенно полученных с помощью МАЛДИ МС/МС.
На положение сульфатных групп в остатках фукозы на невосстанавливающем конце дисахарида указывают сигналы
0,2А1 (сульфат при С4), а также группа сигналов 0,3ХГ По всей видимости, интенсивность сигнала 0,2Х зависит от наличия сульфатной группы в положении С2 и она тем меньше, чем выше вероятность сульфатирования при С2, поскольку интенсивности ионов такого типа были высоки в тандемных ИЭР масс-спектрах несульфатированных олигосахаридов (Zhang et. al., 2006) с остатком уроновой кислоты на восстанавливающем конце. Для более протяженных молекул общая картина сохранялась - остатки фукозы были связаны преимущественно (1^3)-связью и сульфатированы в положениях С2 или С2/С4.
Таким образом, в условиях автогидролиза были получены мультисуль-фатированные моно- и олигосахариды, не образующиеся в продуктах деградации с использованием сольволитического десульфатирования. Особенностью тандемных масс-спектров фрагментов фукоидана из S. cichorioidesбыло отсутствие или сверхнизкая интенсивность фрагмент-ных ионов 0,2А/0,2Х, возникающих в случае наличия в смеси структур,
76
содержащих в цепи (1^4)-связанные остатки фукозы, как в случае с фукой даном из A. nodosum(Daniel et al., 2007). Из вышесказанного следует, что исследуемые фрагменты содержали 2- и реже 4-сульфати-рованные (1^3)-связанные остатки фукозы в качестве превалирующей
[M(2Na)-2Na]

сн3
03SO
°>3Х,
[M2Na-NaHS04-Na]
130 140 150 160 170 180 190 200 210 220 230 240 250 260 270 280 290 300 310 320 330 340 350 360 370 m/z
Рис. 3.12. Тандемный ИЭР масс-спектр иона [Fuc (SO Na) -2Na]2" c m/z 234.011
100-
£75
CD
о
x <D
\-I
3J50
с;
<D
О О
Ь25
О
HSO/ (UA 0,2д
05
СО
CD
о> о
см
см
оо
т—f
±4-4
в
о Y
CN „ CN
200
0,2
X,
о
ОО
CN
* Р" Г )
[M{2Na)-Na]
4t
[M(2Na)-NaHS04-Na]
°'3Xn/°'3Xf
CM ^Г
*
CD
CO
-**!*-*•
100
300
400
m/z
Рис. 3.13. Тандемный МАЛДИ масс-спектр иона [Fuc (SO Na) -Na]" c m/z
77
структурной единицы. Сигнал фрагментного иона, характерный для СЗ сульфатирования. в МС/МС спектрах моно- и дисульфатированной фукозы отсутствовал (Daniel et al., 2007). Применение тандемной МАЛДИ МС (а это было сделано впервые для таких образцов) для анализа смеси мультисульфатированных олигосахаридов с использованием специально подобранной матрицы (арабиноозазона) с целью уменьшения фрагментации образца в источнике ионов, по сравнению с ИЭР МС показало повышенную чувствительность к таким компонентам. Полученные данные согласуются с результатами исследований, выполненных ранее в ТИБОХ ДВО РАН (Zvyagintseva et al., 2003). Положение минорных включений остатков гексозы в структуре фукоидана из S. cichorioidesостается невыясненным, поскольку в режиме отрицательных ионов гексозосодержащих олигосахаридов зарегистрировано не было.
Исследование структуры фукоидана из Fucusevanescens
С помощью методов углеводной химии и ЯМР-спектроскопии М. Билан с соавторами было показано, что основная цепь фукоидана из F. evanescensпредставляет собой линейный полимер, построенный из сульфатирован-ных в основном при С-2 и частично ацетилированных остатков a-L-Fucp, соединенных чередующимися (1->3)- и (1->4)-гликозидными связями (Bilan et al., 2002). При этом была установлена структура только основной цепи фукоидана. Кусайкин с соавторами выделили из
Для анализа фукоидана, выделенного по методу (Zvyagintseva et al., 2003) из S. cichorioides, собранной в шельфовой зоне российского побережья Японского моря, мы применили два метода масс-спектрометрии - тан-демный ИЭР МС в режиме столкновительной диссоциации, который положительно зарекомендовал себя при анализе фукоолигосахаридов из A. nodosumи F. evanescensи тандемный МАЛДИ МС, которым ранее не анализировали сульфатированные фукоолигосахариды в режиме МС/МС отрицательных ионов (точнее режим называется potential lift TOF/TOF, где вторичные ионы образуются при скачкообразном подъеме ускоряющего напряжения и регистрируются вторым времяпролетным анализатором). Использование МАЛДИ МС для полианионных олиго-сахаридов сопряжено с определенными трудностями, поскольку сульфатные группы очень лабильны и могут отрываться в источнике ионов. Нами было найдено, что использование фенилозазона D-эритро-жптозы (arabinoosazone в оригинальной статье (Chen et al., 1997)) в качестве матрицы позволяет минимизировать фрагментацию.
Образец высокосульфатированного фукоидана LcF2 (Fuc, 98%, Man, 2%.), выделенный по методике (Zvyagintseva et al., 2003), был подвергнут автогидролизу. Этанольный экстракт продуктов автогидролиза Lc-AHL (выход 66% от образца LcF2) был проанализирован с помощью масс-спектрометрии ИЭР (рис. 3.10) и МАЛДИ (рис. 3.11) в режиме регистрации отрицательных ионов.
74
I J 8 S
Е I «,-Г1
ё2о Я§
QJf-Ml
220
СЛ
-U±
| 225.007 | [Fuc,S03Na-H20-Na]" |
| 231.010 | [Fuc3(S03Na)3-3Na]3 |
| 234.013 | [Fuc2(S03Na)2-2Na]2- |
| 243.018__[Fu_C|_S0_3_Na-Na]-_279.697'>243.018 | [FuC|S03Na-Na]- |
| 279.697 | [Fuc4(S03Na)3-3Naf |
| 298.037 | [Fuc3(S03Na)2-H20-2Na]2- |
| 307.042 | [Fuc3(S03Na)2-2Naf |
| 328.383 | [Fuc5(S03Na)3-3Na]3" |
| 344.956 | [FuC|(S03Na)2-Nar |
| 371.065 | [Fuc2S03Na-H20-Na]- |
| 380.071 | [Fuc4(S03Na)2-2Na]2- |
| 389.075 | [Fuc2S03Na-Na]- |
| 453.099 | [Fuc3(S03Na)2-2Na]2" |
| 535.131__[Fuc_3_S0_3_Na-Na]-_520_m/zРис.'>535.131 | [Fuc3S03Na-Na]- |
520 m/z
Рис. ЗЛО. ИЭР масс-спектр отрицательных ионов олигосахаридов, полученных автогидролизом фукоидана из бурой водоросли S. cichorioides
и
50 А
0 1|
*i+
| m/z | Состав |
| 225.0 | [Fuc,S03Na-H20-Na]- |
| 243.0 | [Fuc,S03Na-Na]" |
| 344.9 | [Fuc,(S03Na)2-Na]- |
| 371.0 | [Fuc2S03Na-H20-Na]- |
| 389.1 | [Fuc2S03Na-Na]- |
| 473.0 | [Fuc2(S03Na)2-H20-Na]- |
| 491.0 | [Fuc2(S03Na)2-Na]- |
| 517.1 | [Fuc3S03Na-H20-Na]" |
| 535.1 | [Fuc3S03Na-Na]- |
| 619.1 | [Fuc3(S03Na)2-H20-Na]- |
| 637.1 | [Fuc3(S03Na)2-Na]- |
| 739.1 | [Fuc3(SO,Na)3-2Na]- |
| 783.2 | [Fuc4(S03Na)2-Na]- |
| 885.3 | [Fuc4(S03Na)j-2Na]- |
| 929.4 | [Fuc5(S03Na)2-Na]- |
500
Ю |
200
300
400
600
700
800
900 m/z
Рис. 3.11. МАЛДИ масс-спектр отрицательных ионов олигосахаридов, полученных автогидролизом фукоидана из бурой водоросли S. cichorioides
Анализ масс-спектров, полученных двумя методами, дал следующий состав смеси: моносульфат и дисульфат фукозы с
m/z243.0 и 344.9 (основные компоненты) и набор олигосахаридов со степенью полимеризации 2—5 и числом сульфатов на молекулу до 3. Стоит отметить, что интенсивность сигнала иона дисульфатированной фукозы с m/z344.9 была выше при регистрации состава смеси методом МАЛДИ МС.
Далее были получены тандемные масс-спектры большинства ионов, находящихся в смеси. Для того, чтобы идентифицировать фрагментные ионы, имеющие одинаковое значение m/z, но возникающие из восстанавливающего либо невосстанавливающего концов молекулы, образец был восстановлен NaBD4. В результате, ионы, сохраняющие заряд на
75
восстанавливающем конце (Y-ионы), имели на 3 Da большую массу и были идентифицированы однозначно. Полученные данные совпали с результатами исследований фрагментации олигосахаридов каррагинана с помощью ИЭР МС/МС, где было четко показано, что наличие сульфатной группы в остатке сахара провоцировало образование соответствующих Y-ионов, в то время как В- и С-ионы могли образовываться при разрыве гликозидных связей также и между несульфатированными остатками Сахаров (Yu et al., 2006). В тандемных масс-спектрах олигосахаридов из S. cichorioid.esС-ионы практически не наблюдались.
На рисунках 3.12 и 3.13 показаны наиболее информативные тандемные масс-спектры дисульфатированной фукобиозы, полученные разными масс-спектрометрическими методами. Тандемный масс-спектр ИЭР (рис. 3.12) двухзарядного иона [Fuc2(S03Na)2-2Na]2" с m/z234.011 содержал интенсивные сигналы ионов с В с m/z225.007 и Y с m/z243.017 формирующихся при разрыве гликозидных связей. Та же картина повторилась и в тандемном МАЛДИ масс-спектре (рис. 3.13), где интенсивности указанных сигналов примерно совпадали. Отсюда следует, что сульфатные группы находились в среднем по одной на восстанавливающем и на невосстанавливающем остатках фукозы. Сигналы 0,2Х0/0,2А0, имеющие высокие интенсивности в ИЭР МС/МС спектрах фукоолигосахаридов из A. nodosum, содержащих большой процент (1^4)-связанных остатков фукозы, в данных масс-спектрах имеют гораздо меньшие интенсивности, особенно полученных с помощью МАЛДИ МС/МС.
На положение сульфатных групп в остатках фукозы на невосстанавливающем конце дисахарида указывают сигналы
0,2А1 (сульфат при С4), а также группа сигналов 0,3ХГ По всей видимости, интенсивность сигнала 0,2Х зависит от наличия сульфатной группы в положении С2 и она тем меньше, чем выше вероятность сульфатирования при С2, поскольку интенсивности ионов такого типа были высоки в тандемных ИЭР масс-спектрах несульфатированных олигосахаридов (Zhang et. al., 2006) с остатком уроновой кислоты на восстанавливающем конце. Для более протяженных молекул общая картина сохранялась - остатки фукозы были связаны преимущественно (1^3)-связью и сульфатированы в положениях С2 или С2/С4.
Таким образом, в условиях автогидролиза были получены мультисуль-фатированные моно- и олигосахариды, не образующиеся в продуктах деградации с использованием сольволитического десульфатирования. Особенностью тандемных масс-спектров фрагментов фукоидана из S. cichorioidesбыло отсутствие или сверхнизкая интенсивность фрагмент-ных ионов 0,2А/0,2Х, возникающих в случае наличия в смеси структур,
76
содержащих в цепи (1^4)-связанные остатки фукозы, как в случае с фукой даном из A. nodosum(Daniel et al., 2007). Из вышесказанного следует, что исследуемые фрагменты содержали 2- и реже 4-сульфати-рованные (1^3)-связанные остатки фукозы в качестве превалирующей
| | /|--------О. /СН3 |
| | ■o3so |
| он | |
| /1--------О | о d"*Yi |
| -'-03SOy | |
[M(2Na)-2Na]

| | /1--------О, /СН3 |
| ОН | 03SO |
| А--------О | J о \f"Bl |
| с ' н0> | |
сн3
03SO
°>3Х,
[M2Na-NaHS04-Na]
130 140 150 160 170 180 190 200 210 220 230 240 250 260 270 280 290 300 310 320 330 340 350 360 370 m/z
Рис. 3.12. Тандемный ИЭР масс-спектр иона [Fuc (SO Na) -2Na]2" c m/z 234.011
100-
£75
CD
о
x <D
\-I
3J50
с;
<D
О О
Ь25
О
HSO/ (UA 0,2д
05
СО
CD
о> о
см
см
оо
т—f
±4-4
в
о Y
CN „ CN
200
0,2
X,
о
ОО
CN
[M{2Na)-Na]
4t
[M(2Na)-NaHS04-Na]
°'3Xn/°'3Xf
CM ^Г
*
CD
CO
-**!*-*•
100
300
400
m/z
Рис. 3.13. Тандемный МАЛДИ масс-спектр иона [Fuc (SO Na) -Na]" c m/z
77
структурной единицы. Сигнал фрагментного иона, характерный для СЗ сульфатирования. в МС/МС спектрах моно- и дисульфатированной фукозы отсутствовал (Daniel et al., 2007). Применение тандемной МАЛДИ МС (а это было сделано впервые для таких образцов) для анализа смеси мультисульфатированных олигосахаридов с использованием специально подобранной матрицы (арабиноозазона) с целью уменьшения фрагментации образца в источнике ионов, по сравнению с ИЭР МС показало повышенную чувствительность к таким компонентам. Полученные данные согласуются с результатами исследований, выполненных ранее в ТИБОХ ДВО РАН (Zvyagintseva et al., 2003). Положение минорных включений остатков гексозы в структуре фукоидана из S. cichorioidesостается невыясненным, поскольку в режиме отрицательных ионов гексозосодержащих олигосахаридов зарегистрировано не было.
Исследование структуры фукоидана из Fucusevanescens
С помощью методов углеводной химии и ЯМР-спектроскопии М. Билан с соавторами было показано, что основная цепь фукоидана из F. evanescensпредставляет собой линейный полимер, построенный из сульфатирован-ных в основном при С-2 и частично ацетилированных остатков a-L-Fucp, соединенных чередующимися (1->3)- и (1->4)-гликозидными связями (Bilan et al., 2002). При этом была установлена структура только основной цепи фукоидана. Кусайкин с соавторами выделили из


