Файл: 1. Цели и задачи пробоотбора. Представительность пробы. Факторы, учитывающиеся при пробоотборе. Виды проб.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.02.2024
Просмотров: 863
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
2. Отбор проб сыпучих материалов. Генеральная проба и ее разделка.
6. Особенности пробоотбора жидких сред при анализе на содержание суперэкотоксикантов.
10. Общие требования к отбору проб почв и донных отложений
11. Общие требования к отбору биопроб и пищевых продуктов.
12. Особенности отбора проб из воздуха.
16. Специальные методы пробоподготовки. Разложение с использованием ионитов.
Стеклянные пробоотборные сосуды (пипетки) используют для улавливания и транспортировки газообразных проб с последующим извлечением аликвотной части пробы газовым шприцем для анализа. Заполнение этих сосудов осуществляют путем вакуумирования или продувки анализируемым воздухом. Стекло подвергается специальной обработке, чтобы избежать механических повреждений при перевозке контейнера. Пипетки оснащены двумя высоковакуумными стеклянными кранами с тефлоновыми пробками и клапаном с тефлоновой прокладкой для отбора пробы в лаборатории шприцем (рис. 3.1).
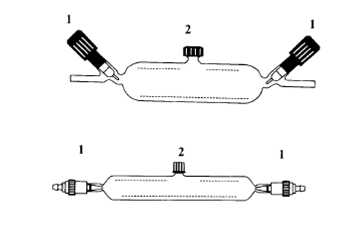 Рисунок 3.1 – Стеклянные пробоотборные сосуды (пипетки): 1 – вакуумные краны, 2 – клапан с тефлоновой прокладкой для отбора пробы воздуха шприцем
Рисунок 3.1 – Стеклянные пробоотборные сосуды (пипетки): 1 – вакуумные краны, 2 – клапан с тефлоновой прокладкой для отбора пробы воздуха шприцемЕмкость используемых для отбора проб стеклянных пипеток – от 50 мл до 2 л. Для этих целей выпускаются также пипетки из нержавеющей стали. Их вместимость – от 75 мл до 500 мл и они могут выдержать давление до 13000 кПа.
Другими распространенными контейнерами для отбора загрязненного воздуха являются мешки из полимерных пленок. Они обладают очень низкой проницаемостью для постоянных (N2, O2, H2, Ar и др.) и большинства других газов. Пробоотбор может проводиться в широком температурном диапазоне, мешки могут использоваться многократно, а при хранении газообразной пробы в них потери контролируемых компонентов минимальны. После использования и продувки таких мешков чистым инертным газом их «память» минимальна. Эти мешки прочны, эластичны и быстро восстанавливают первоначальную форму.
Техника отбора проб воздуха проста. Так при использовании полиэтиленовых мешков большого объема (20 – 40 л) на месте взятия пробы его сначала несколько (5 – 6) раз «промывают» анализируемым воздухом. Для этого мешок берут за края обеими реками и несколько раз подряд быстрыми движениями сверху вниз заполняют его воздухом, который тут же выпускают, сжимая мешок. Процедуру повторяют несколько раз, а затем заполняют мешок воздухом и завязывают горловину мешка бечевкой.
Наиболее популярными контейнерами этого типа являются мешки из пленки Тедлар – высококачественной поливинилфторидной пленки толщиной 2 мм, которые изготавливают без применения пластификаторов. Пленка из поливинилфторида менее проницаема для газов, чем тефлон, и стойка к действию различных химических веществ. Мешки из этих материалов используют для отбора проб воздуха, содержащего не коррозионные газы, пары растворителей, углеводороды, хлорсодержащие соединения, СО, SO2, H2S, меркаптаны и другие химические загрязнители воздуха. Мешок имеет клапан (вентиль) из полипропилена, через который его заполняют воздухом с помощью гибкого шланга из полимерного материала. Отбор анализируемой пробы производится шприцем, которым прокалывают полимерную прокладку вентиля.
Пятислойные мешки непроницаемы не только для любых газов, но и для УФ-излучения, способного разрушать вещества пробы или инициировать фотохимические реакции. Кроме того, они инертны к большинству химических соединений, прочны, упруги, гибки и могут быть использованы повторно.
Таким образом, к недостаткам отбора проб воздуха в контейнеры можно отнести: ограниченный набор определяемых соединений; ограниченный предел обнаружения примесей; сорбцию компонентов на стенках контейнеров; возможность протекания химических реакций при хранении пробы в контейнере в присутствии влаги и кислорода воздуха.
Погрешности при отборе загрязненного воздуха в контейнеры возникают главным образом из-за потерь исследуемых веществ, связанных с нарушением герметичности пробоотборных устройств, из-за проницаемости пленочных материалов, из-за сорбции микроколичеств веществ внутренней поверхностью пробоотборных емкостей, а также из-за химических реакций компонентов пробы между собой и с материалом контейнера в присутствии влаги, света и кислорода воздуха (особенно в случае реакционноспособных веществ).
Ряд погрешностей могут быть в значительной мере устранены путем многократного «промывания» пробоотборных емкостей исследуемым воздухом с целью установления равновесия между содержанием веществ в исследуемом воздухе и на поверхности пробоотборных емкостей, а также путем определения допустимых сроков и условий хранения отобранных проб.
Отбор проб воздуха с одновременным концентрированием
При концентрировании микропримесей из воздуха насчитывается значительно больше факторов, способных стать причинами погрешностей, чем при концентрировании из других сред. Среди них можно выделить следующие.
1. Неправильное измерение объема исследуемого воздуха. Объем воздуха при отборе проб измеряют обычно с помощью «сухого» ротаметра, реже – с помощью жидкостного реометра.
Принцип работы ротаметра. Ротаметр состоит из конической трубки, расходящейся вверх, внутри которой перемещается поплавок-индикатор. Измеряемый поток жидкости или газа проходит через трубку снизу вверх и поднимает поплавок. Чем выше поплавок, тем больше площадь вокруг него, через которую может течь поток. Поднявшись настолько, что сила тяжести FG уравновешивает подъёмную силу Fr со стороны потока, поплавок останавливается. Таким образом, каждому положению поплавка соответствует определенный расход. Калибровка ротаметров может производиться по воздуху или воде при н.у., а также по параметрам измеряемой среды. Ротаметр часто используется для определения расхода агрессивных жидкостей.
Трубки ротаметров могут быть стеклянными (рассчитаны на давление до 2,5 МПа) и металлическими (до 70 МПа). Поплавки в зависимости от свойств жидкости или газа изготовляют из различных металлов либо пластмасс.
Однако в процессе эксплуатации показания ротаметров меняются из-за изменения массы поплавка и кольцевого зазора ротаметра вследствие воздействия на поплавок веществ, уносимых воздухом из поглотительных приборов, из-за старения пластмассы, из которой часто изготавливают трубки и поплавки ротаметров, загрязнения капилляров реометра и др.
2. Пренебрежение агрегатным состоянием изучаемых веществ. Для концентрирования веществ, находящихся в парогазообразном состоянии обычно используют поглотительные приборы, заполненные водой, органическими растворителями, растворами или сорбентами, фильтрующими тканями, бумагой и др. Для концентрирования аэрозолей практически непригодны жидкости, поскольку они не обеспечивают эффективного улавливания аэрозолей.
3. Выбор сред для концентрирования. Концентрирование с использованием жидких поглотительных сред основано на сорбции поглощаемых соединений или их химическом взаимодействии с поглощающей средой (хемосорбцией). Концентрирование с использованием твердых поглотительных сред основано на сорбции изучаемых соединений, реже – на хемосорбции.
Эффективность поглощения зависит от скорости и продолжительности аспирации исследуемого воздуха через поглотительную среду. Скорость аспирации воздуха можно считать оптимальной, если она согласуется со скоростью растворения или химического взаимодействия улавливаемых микропримесей, а также со скоростью растворения вновь образующихся веществ в поглотительной среде.
4. Наличие микропримесей. Следует учитывать возможное влияние постоянно содержащихся в воздухе окислителей и воды. Так, при поглощении H2S (путем аспирации воздуха через жидкую среду), основанном на сорбции или хемосорбции, возможно окисление этими окислителями как сероводорода, так и продукта реакции, образовавшегося в процессе поглощения.
Конденсация содержащихся в воздухе паров воды в пробоотборных установках при глубоком охлаждении последних также может существенно затруднить отбор проб. Поэтому перед пробоотборным устройством нередко помещают осушитель.
5. Полнота сорбции и десорбции. Успешное концентрирование микропримесей, загрязняющих воздух, зависит от эффективной сорбции и последующей их десорбции. При этом одним из наиболее важных моментов является селективность сорбции по отношению к изучаемым соединениям.
6. Химические или фотохимические реакции. Основными фотохимическими реакциями в атмосферном воздухе являются реакции диоксида и оксида азота, озона, атомов и возбужденных молекул кислорода, радикалов, оксида углерода, паров воды, аммиака, органических веществ и ионов. Так, например, основным поглотителем солнечного света в ультрафиолетовой области является диоксид азота. Его роль в инициировании фотохимических реакций обусловлена легкостью перехода в возбужденное состояние при поглощении энергии. Возбужденная молекула обладает повышенной реакционной способностью с органическими соединениями.
При анализе объектов окружающей среды важным фактором являются условия хранения проб. Так, пробы воздуха, отобранные на активные твердые сорбенты, можно хранить ограниченное время, а в некоторых случаях необходимо охлаждение. Сконцентрированные вещества могут взаимодействовать как между собой, так и с сорбентами. При значительной разнице температур в момент отбора и при хранении возможна десорбция сконцентрированных веществ. Такие же проблемы возможны и при концентрировании в жидкие поглотительные среды.
Отбор проб воздуха в жидкие среды
Многообразие вредных веществ и их различное агрегатное состояние в воздухе обусловливает использование разнообразных поглотительных систем, обеспечивающих эффективное поглощение микропримесей.
Отбор парогазовых веществ в жидкие поглотительные среды – наиболее распространенный способ. Анализируемые вещества растворяются или вступают в химическое взаимодействие с поглотительной средой (хемосорбция), которая обеспечивает полноту поглощения за счет образования нелетучих соединений. При этом упрощается подготовка пробы к анализу, который обычно проводят в жидкой фазе.
Отбор проб в растворы осуществляют аспирацией исследуемого воздуха через поглотительный сосуд с каким-либо растворителем (органические растворители, кислоты, спирты, вода, смешанные растворы). Скорость пропускания воздуха может меняться в широких пределах – от 0,1 до 100 л/мин.
Полнота поглощения зависит от многих факторов, в том числе от конструкции поглотительных сосудов. Наибольшее распространение получили абсорберы со стеклянными пористыми пластинками, поглотительные сосуды Рыхтера, Зайцева, Яворовского.
Для физической абсорбции, когда определяемые газообразные или парообразные вещества растворяются в поглотительной среде, не вступая с ней в химическое взаимодействие, важно обеспечить максимальную поверхность контакта фаз – газообразной (парообразной) и жидкой. В поглотителях с пористой пластинкой этот эффект достигается за счет уменьшения пузырьков воздуха при прохождении его через пористый фильтр, вследствие чего увеличивается поверхность контакта воздуха с раствором, а скорость аспирации может быть повышена до 3 л/мин.
Увеличение поверхности контакта может быть достигнуто также в результате увеличения длины пути прохождения пузырьков воздуха через раствор. Так, в поглотительных сосудах Зайцева высота столба растворителя составляет около 10 см. Однако предельная скорость аспирации не превышает 0,5 – 0,6 л/мин.
При отборе проб в поглотительные сосуды Рыхтера, в которых используют эффект эжекции скорость аспирации воздуха может достигать 100 л/мин. Эффект эжекции заключается в том, что поток с более высоким давлением, движущийся с большой скоростью, увлекает за собой среду с низким давлением.
Более эффективным является поглощение, основанное на химических реакциях исследуемых веществ с поглотительной жидкостью. Например, для поглощения аммиака и аминов применяют разбавленную серную кислоту, для поглощения фенола – раствор щелочи.
Для проверки эффективности работы поглотительного сосуда к нему присоединяют последовательно еще один или два поглотителя. Пробу воздуха с известным содержанием вредного вещества пропускают через все абсорберы и затем поглотительные растворы из каждого сосуда анализируют.
Достоинствами отбора проб в жидкие среды являются селективность (можно подобрать поглотительный раствор для широкого круга загрязняющих веществ), простота, экономичность. К недостаткам следует отнести невысокую степень концентрирования (используют для отбора проб воздуха при высоких концентрациях загрязнителей); невозможность получения представительной пробы при одновременном наличии в воздухе паров и твердых аэрозолей загрязняющих веществ; малая эффективность при необходимости отбора большого объема воздуха, вследствие обветривания раствора и связанных с этим потерь определяемых компонентов.
Отбор проб на твердые сорбенты
Отбор проб на твердые сорбенты дает возможность значительно увеличить объем пробы и скорость ее пропускания (по сравнению с пропусканием через жидкость), что позволяет короткое время накопить исследуемое вещество в количестве, достаточном для его определения. Твердые сорбенты позволяют также осуществлять избирательную сорбцию одних веществ в присутствии других; кроме того, они удобны как в работе, так и при транспортировке и хранении отобранных проб. Пробы, отобранные на твердые сорбенты, обладают высокой сохранностью. Этот метод пробоотбора характеризуется высоким коэффициентом концентрирования.

