ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.05.2024
Просмотров: 123
Скачиваний: 0
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
Гиббстің еркін энергиясы анықталатын формула:
Изокинетикалық процесс барысында жүйедегі температура өзгермейтін жүйе:
Реакциялары үшін дұрыс пікірлерді таңдаңыз:
Реакциялары үшін дұрыс пікірлерді таңдаңыз:
Төменде көрсетілген шамалардың қайсысы күй функциясы болып табылады:
H2+Br2→2HBr реакциясы үшін тепе-теңдік тұрақтысы:
Әрекеттесуші заттардың концентрациясын 2 есе арттырса, 2NO +O2=2NO2 реакция жылдамдығы:
Жалпы кинетикалық теңдеуінде бірнеше жылдамдық константасы көрсетілген реакциялар:
+H + H + M == H2 + M.
-
aA + bB ↔ cC + dD кері реакциясы үшін реттілік тең
+c+d.
-
Нөлінші ретті реакция жылдамдығы анықталатын теңдеу:
+w=k.
-
СО + Cl2 = COCl2 реакциясы:
-
Мономолекулярлы реакция. -
Екінші ретті реакция. -
Бимолекулярлы реакция. -
Бірінші ретті реакция. -
Тримолекулярлы реакция.
- 1 ... 4 5 6 7 8 9 10 11 12
Жалпы кинетикалық теңдеуінде бірнеше жылдамдық константасы көрсетілген реакциялар:
Күрделі.
-
Бірдей зататрдың бір уақытта әрекеттесіп, бірақ түрлі өнімдер түзетін реакциялар аталады:
Параллельді.
-
Бірінен соң бірі кезектесіп жүретін реакциялар аталады:
Кезектескен.
-
Бастапқы реакция өздігінен жүріп, екінші реакция бірінші реакцияның есебінен жүретін реакцияларды қалай атайды:
Қосарланған.
-
Бір уақытта қарама-қарсы екі бағытта жүретін реакциялардың аталуы:
Қайтымды.
- «Температураны әрбір 10 градусқа көтерген сайын химиялық орташа 2-4 есе артады» Вант-Гофф ережесі қолданылмайтын реакция:
Ферментативті.
-
Өз бетінше катализатор емес, бірақ катализаторға қосқанда оның активтілігін арттыратын зат аталады:
Промотор.
-
Реакция жылдамдығы азаяды:
каталитикалық удың әсерінен.
-
Субстрат:
берілген ферменттің әсер беретін қосылысы.
- Бастапқы А затының уақыт бірлігінде концентрациясының өзгерісіне сәйкес келетін кинетикалық қисықты таңдаңыз (А + В→ Д +Е)
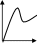
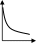

 С c c c c
С c c c c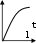 t t t t
t t t t2 3 4 5
-
1 -
2 -
3 -
4 -
5
- A реакция өнімінің концентрациямының уақыт бірлігінде концентрациясының өзгерісіне сәйкес келетін кинетикалық қисықты таңдаңыз (А+B→Д+Е)
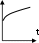
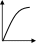
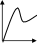

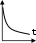 C c c c c
C c c c c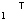 t
t2 3 4 5
1. 1
2. 2
3. 3
4. 4
5. 5
-
Реакцияның молекулярлығы дегеніміз:
Реакцияның стехиометриялық коэффициенттерінің қосындысы.
-
Бірнеше қатар кезекті стадиядан тұратын кез-келген күрделі химиялық реакцияның жылдамдығы анықталады:
Ең баяу стадияның жылдамдығымен.
-
Бимолекулярлы реакцияны көрсетіңіз (Көрсетілген теңдеу элементарлы стадия ретінде санаңыз):
H2 + J2→ 2HJ.
-
Тримолекулярлыреакцияны көрсетіңіз (Көрсетілген теңдеу элементарлы стадия ретінде санаңыз):
2NO+O2=2NO2.
-
aA+bB=mM+nN тура реакциясының ретін анықтайтын теңдеуді көрсетіңіз:
+n=a+b.
- 1 ... 4 5 6 7 8 9 10 11 12
Укажите кинетическое уравнение реакции 3 порядка
-
w=k -
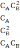 w=k
w=k -
w=k -
w=k -
w=k
-
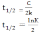 Найдите выражение для определения времени полураспада для реакции 1 порядка
Найдите выражение для определения времени полураспада для реакции 1 порядка
1)
2)
3)
4)
5)
-
Өзінің тұзының ерітіндісіне батырылған, оң зарядталатын металл пластикасы:
мыс.
-
Якоби-Даниэль химиялық гальваникалық элементінде:
Zn+CuSO4=Cu+ZnSO4.
-
Сутекті электрод потенциалын есептеуге болатын формула:
φсут = 0.059pH.
-
Көрсетілген электродтар ішінен екінші текті электродтарды таңдаңыз:
хлоркүміс.
-
Cl- иондарының концентрациясына потенциалы тәуелді болатын электрод:
хлоркүміс.
-
Хлоркүміс электроды:
ІІ текті электрод.
-
Қышқылдық-негіздік потенциометрлік титрлеу графикалық тәуелділігі салынатын координаталар:
рН – титрант көлемі.
-
Меншікті электрөткізгіштің өлшем бірлігі:
См-1*см-1.
-
Кондуктометрия - өлшеу:
электрөткізгіштікті.
-
Молярлық электрөткізгіштікті анықтауға болатын формулa:
λ= ǽ*1000/C.
-
Шексіз сұйытылған ерітінділерде иондардың тәуелсіз қозғалысының заңын ашқан:
Кольрауш.
- Қысымның жоғарылауымен газ фазасында термиялық активтену механизмі нәтижесінде ыдырайтын заттың реакциялық реті 2-ден n-ге дейін өзгереді n-нің мәнін көрсетіңіз
1) 1
2) 2
3) 3
4) 4
5) 5
- Егер реакция температурасы коэффициенті γ = 3 болса, температура 25 градустен 45 градусқа дейін жоғарылағанда реакция жылдамдығы қалай өзгереді?
9 есе көбейеді
- Егер реакцияның температуралық коэффициенті γ = 2 болса, температураны 50 градусқа көтергенде реакция жылдамдығы қалай өзгереді?
32 есе артады
- Егер реакцияның температуралық коэффициенті γ = 3 болса, онда температура 40 градусқа төмендеген кезде реакция жылдамдығы ...
81 есе азаяды
-
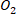 Определите молекулярность реакции 2СО +
Определите молекулярность реакции 2СО + 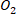 = 2С
= 2С
3
-
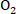 Егер ұсынылған стехиометриялық реакция теңдеуі оның механизміне сәйкес келсе, онда реакцияның 2NO+ = 2N
Егер ұсынылған стехиометриялық реакция теңдеуі оның механизміне сәйкес келсе, онда реакцияның 2NO+ = 2N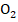 молекулалық мәні
молекулалық мәні
3
-
Реакциядағы 2СО+О2 = 2СО2 заттардың концентрациясының 2 есе артқанда реакция жылдамдығы қалай өзгереді
8 есе артады
- Егер химиялық реакция жылдамдығы реакцияға түсетін заттардың концентрациясына тәуелді болмаса, онда реакция реті қандай болады:
нөл
- Реакция жылдамдығы W = k [A]1/2[B]-1 болғандағы реакцияның реттілігін анықтаңыз
-1/2
-
Қандай жағдайларда А + В → С химиялық реакция жылдамдығының константасы реакцияның жылдамдығына тең (w = k)?
реакцияласушы заттардың концентрациялары бірге тең болған
