Файл: Курсовой проект по дисциплине Теория и технология химических процессов органического и нефтехимического синтеза на тему Технологическое проектирование установки гидроочистки дизельной фракции мощностью 1910 тыс тгод.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 25.04.2024
Просмотров: 202
Скачиваний: 2
СОДЕРЖАНИЕ
1.3 Термодинамика и кинетика процесса
1.5 Основные параметры и их влияние на процесс
1.6 Математическое моделирование процесса
1.7 Сведения о существующих технологиях (патентный обзор)
2.1 Характеристика исходного сырья, материалов, катализаторов, энергоресурсов и готового продукта
2.2 Описание технологической схемы
2.3 Технологические расчеты установки и основных аппаратов
2.3.1 Исходные данные для расчета
2.3.2 Определение часовой производительности установки
2.3.5 Определение выхода сероводорода
2.3.5 Материальный баланс установки
2.3.7 Расчет толщины корпуса и эллиптического днища реактора
2.3.8 Тепловой баланс реактора
2.3.8.1 Расчет парциальных давлений компонентов ГСС и ГПС
2.3.8.2 Определение агрегатного состояния ГСС и ГПС
2.3.8.4 Расчет потерь тепла в окружающую среду
2.3.8.5 Материальный и тепловой баланс реактора
2.3.9 Гидравлический расчет реактора
2.3.10.1 Расчет холодного сепаратора высокого давления
2.3.10.2 Расчет холодного сепаратора низкого давления
2.3.11 Расчет сырьевого теплообменника
2.3.12 Расчет конденсатора-холодильника АВО-1 по укрупненным показателям
2.3.13 Расчет водяного холодильника ВХ-1 по укрупненным показателям
2.3.14 Расчет печи П-1 по укрупненным показателям
Определяем количество теплоты, вносимое с компонентами ГПС при температуре 360 °С и давлении 3,8 МПа:
-
с дизельным топливом
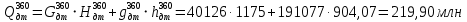 кДж/ч;
кДж/ч;-
с бензином
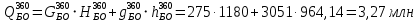 кДж/ч;
кДж/ч; -
с углеводородным газом
 кДж/ч;
кДж/ч;-
с сероводородом
 кДж/ч;
кДж/ч;-
с ЦВСГ
 кДж/ч;
кДж/ч;где
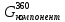 - расход компонента ГПС в паровой фазе при 36
- расход компонента ГПС в паровой фазе при 36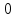 °С, кг/ч;
°С, кг/ч; - энтальпия компонента ГПС в паровой фазе при 36
- энтальпия компонента ГПС в паровой фазе при 36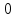 °С, кДж/кг;
°С, кДж/кг; - расход компонента ГПС в жидкой фазе при 36
- расход компонента ГПС в жидкой фазе при 36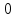 °С, кг/ч;
°С, кг/ч;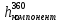 - энтальпия компонента ГПС жидкой фазе при 36
- энтальпия компонента ГПС жидкой фазе при 36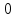 °С, кДж/кг.
°С, кДж/кг.Количество теплоты, содержащееся в ГПС при 36
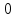 °С:
°С: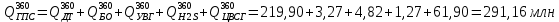 кДж/ч.
кДж/ч. Аналогичным образом рассчитываем, какое количество теплоты, содержится в ГПС при 210 °С.
Найдем энтальпию нефтяных паров гидрогенизата при 210 °С и атмосферном давлении:
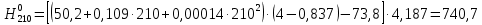 кДж/кг.
кДж/кг.Поправку к энтальпии нефтяных паров гидрогенизата при 210 °С и повышенном давлении находим аналогично п. 2.3.8.2. Тогда энтальпия нефтяных паров гидрогенизата при 210 °С и повышенном давлении равна:
H210 = 740,7 – (-11,1) = 751,8 кДж/кг.
Энтальпию жидкого гидрогенизата находим по формуле
 ,
,где α = 0,403·t + 0,000405·t2.
Тогда
α = 0,403·210 + 0,000405·2102 = 102,49;
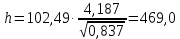 кДж/кг.
кДж/кг.Найдем энтальпию нефтяных паров бензина-отгона при 210 °С и атмосферном давлении:
 кДж/кг.
кДж/кг.Поправку к энтальпии нефтяных паров бензина-отгона при 210 °С и повышенном давлении находим аналогично п. 2.3.8.2. Тогда энтальпия нефтяных паров бензина-отгона при 210 °С и повышенном давлении равна:
H210 = 774,25 – (-49,04) = 823,3 кДж/кг.
Энтальпию жидкого бензина-отгона находим по формуле
 ,
,где α = 0,403·t + 0,000405·t2.
Тогда
α = 0,403·210 + 0,000405·2102 = 102,49;
 кДж/кг.
кДж/кг.По формуле определяем количество теплоты, уходящее с компонентами ГПС при температуре 210 °С и давлении 3,8 МПа:
-
с дизельным топливом
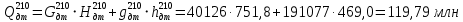 кДж/ч;
кДж/ч;-
с бензином
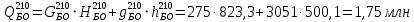 кДж/ч;
кДж/ч; -
с углеводородным газом
 кДж/ч;
кДж/ч;-
с сероводородом
 кДж/ч;
кДж/ч;-
с ЦВСГ
 кДж/ч;
кДж/ч;где
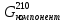 - расход компонента ГПС в паровой фазе при 210 °С, кг/ч;
- расход компонента ГПС в паровой фазе при 210 °С, кг/ч;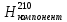 - энтальпия компонента ГПС в паровой фазе при 210 °С, кДж/кг;
- энтальпия компонента ГПС в паровой фазе при 210 °С, кДж/кг; - расход компонента ГПС в жидкой фазе при 210 °С, кг/ч;
- расход компонента ГПС в жидкой фазе при 210 °С, кг/ч;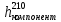 - энтальпия компонента ГПС жидкой фазе при 210 °С, кДж/кг.
- энтальпия компонента ГПС жидкой фазе при 210 °С, кДж/кг.Количество теплоты, содержащееся в ГПС при 210 °С по формуле:
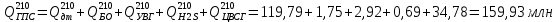 кДж/ч.
кДж/ч.Определяем количество теплоты приходящее с ГПС:
 млн кДж/ч,
млн кДж/ч,где
 — коэффициент использования теплоты, принимаем 0,96 [27].
— коэффициент использования теплоты, принимаем 0,96 [27].Найдем энтальпию нефтяных паров сырья при 100 °С и атмосферном давлении:
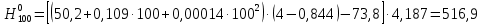 кДж/кг.
кДж/кг.Поправку к энтальпии нефтяных паров сырья при 100 °С и повышенном давлении находим аналогично п. 2.3.8.2. Тогда энтальпия нефтяных паров сырья при 100 °С и повышенном давлении равна:
H100 = 516,9 – (-129,9) = 646,8 кДж/кг.
Энтальпию жидкого гидрогенизата находим по формуле
 ,
,где α = 0,403·t + 0,000405·t2.
Тогда
α = 0,403·100 + 0,000405·1002 = 44,35;
 кДж/кг.
кДж/кг.При температуре 100 °С рассчитаем материальный баланс однократного испарения ГСС (табл. 2.38-2.39),
Таблица 2.38 – Состав паровой и жидкой фаз ГСС на выходе из теплообменника при температуре 100 °С и давлении 4,0 МПа
| Наименование | α=  | Ki | Xi=  | Yi= Ki  |
| Водород | 0,7654 | 14,7 | 0,0610 | 0,8964 |
| Метан | 0,0173 | 5,8 | 0,0034 | 0,0199 |
| Этан | 0,0117 | 2,4 | 0,0054 | 0,0129 |
| Пропан | 0,0048 | 1,2 | 0,0041 | 0,0049 |
| Изобутан | 0,0009 | 0,4 | 0,0018 | 0,0007 |
| Бутан | 0,0004 | 0,5 | 0,0007 | 0,0003 |
| Изопентан | 0,0001 | 0,3 | 0,0002 | 0,0001 |
| Н-пентан | 0,0001 | 0,2 | 0,0003 | 0,0001 |
| Сырье | 0,1992 | 0,07 | 0,9231 | 0,0646 |
| Итого | 0,9999 | - | 1,0000 | 0,9999 |
Таблица 2.39 – Материальный баланс однократного испарения ГСС на выходе из теплообменника при температуре 100 °С и давлении 4,0 МПа
| Компонент | Приход ГСС | Расход | ||||||||||||
 |  |  | ai | Жидкая фаза | Паровая фаза | |||||||||
 |  |  | хi |  |  |  | уi | |||||||
| Водород | 9173 | 0,0364 | 4541,0 | 0,7654 | 584 | 0,0026 | 289,2 | 0,0610 | 8588 | 0,3083 | 4251,7 | 0,8964 | ||
| Метан | 1648 | 0,0065 | 102,7 | 0,0173 | 242 | 0,0011 | 15,1 | 0,0034 | 1406 | 0,0505 | 87,6 | 0,0199 | ||
| Этан | 2091 | 0,0083 | 69,5 | 0,0117 | 615 | 0,0027 | 20,5 | 0,0054 | 1476 | 0,0530 | 49,1 | 0,0129 | ||
| Пропан | 1267 | 0,0050 | 28,7 | 0,0048 | 576 | 0,0026 | 13,1 | 0,0041 | 691 | 0,0248 | 15,7 | 0,0049 | ||
| Изобутан | 326 | 0,0013 | 5,6 | 0,0009 | 233 | 0,0010 | 4,0 | 0,0018 | 93 | 0,0033 | 1,6 | 0,0007 | ||
| Н-бутан | 149 | 0,0006 | 2,6 | 0,0004 | 99 | 0,0004 | 1,7 | 0,0007 | 50 | 0,0018 | 0,9 | 0,0003 | ||
| Изопентан | 55 | 0,0002 | 0,8 | 0,0001 | 42 | 0,0002 | 0,6 | 0,0002 | 13 | 0,0005 | 0,2 | 0,0001 | ||
| Н-пентан | 27 | 0,0001 | 0,4 | 0,0001 | 22 | 0,0001 | 0,3 | 0,0003 | 4 | 0,0002 | 0,1 | 0,0001 | ||
| Сырье | 237525 | 0,9416 | 1181,7 | 0,1992 | 221986 | 0,9892 | 1104,4 | 0,9231 | 15539 | 0,5578 | 77,3 | 0,0646 | ||
| Итого | 252260 | 1,0000 | 5933,0 | 1,0000 | 224400 | 1,0000 | 1448,9 | 1,0000 | 27860 | 1,0000 | 4484,1 | 0,9999 | ||
При температуре 100 0С количество теплоты каждого компонента по формуле:
 ;
; ;
;Количество теплоты ГСС при температуре 100 °С по формуле
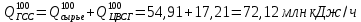 .
.Для определения температуры ГСС (tx) на выходе из теплообменника найдем количество теплоты при двух температурах:
1) t1 = 220-250 °С;
2) t2 = 300-320 °С.
При принятых температурах рассчитаем материальные балансы однократного испарения ГСС (табл. 2.40-2.43), затем построим график зависимости количества теплоты от температуры и по нему определим температуру ГСС на выходе из теплообменника, зная количество теплоты, переданное ГПС потоку ГСС.
Таблица 2.40 – Состав паровой и жидкой фаз ГСС на выходе из теплообменника при температуре 230 °С и давлении 4,0 МПа
| Наименование | α=  | Ki | Xi=  | Yi= Ki  |
| Водород | 0,7654 | 22,5 | 0,0389 | 0,8743 |
| Метан | 0,0173 | 8,2 | 0,0024 | 0,0196 |
| Этан | 0,0117 | 6,8 | 0,0019 | 0,0132 |
| Пропан | 0,0048 | 4,3 | 0,0013 | 0,0054 |
| Изобутан | 0,0009 | 2,5 | 0,0004 | 0,0010 |
| Бутан | 0,0004 | 2,4 | 0,0002 | 0,0005 |
| Изопентан | 0,0001 | 1,8 | 0,0001 | 0,0001 |
| Н-пентан | 0,0001 | 1,9 | 0,0000 | 0,0001 |
| Сырье | 0,1992 | 0,09 | 0,9548 | 0,0859 |
| Итого | 1,0000 | - | 1,0000 | 1,0000 |

