ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 27.03.2024
Просмотров: 130
Скачиваний: 0
СОДЕРЖАНИЕ
Сборник методических указаний к лабораторным работам
Сущность и основы метода ик-спектроскопии
3.4. Определение железа (III) в водных растворах методом градуировочного графика.
3.3. Определение титана (IV) методом градуировочного графика.
3.4. Определение фосфора в водных растворах методом градуировочного графика.
3.5. Определение нитрит-ионов методом градуировочного графика.
1.3. Рефрактометрическое определение сахара в молоке
1. Иономер-кондуктометр; 2. Магнитная мешалка; 3. Кондуктометрический датчик; 4. Ячейка; 5. Бюретка
6. Расчёт результатов определения тиосульфата натрия (точность расчётов – 4 значащих цифры, для массы 0,0001 г). Привести расчётные формулы и расчёты, рассчитанные значения занести в таблицы 12.18.
Результаты определения тиосульфата
Таблица 12.18.
|
с(1/1 S2O32-), моль/дм3 |
T(S2O32-), г/см3 |
n(1/1 S2O32-), моль |
ν(S2O32-), моль |
m(S2O32-), г |
|
|
|
|
|
|
|
с(1/1 Na2S2O3), моль/дм3 |
T(Na2S2O3), г/см3 |
n(1/1 Na2S2O3), моль |
ν(Na2S2O3), моль |
m(Na2S2O3), г |
|
|
|
|
|
|
5. Расчёт относительной погрешности:

-
Определение хлороводородной кислоты методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности.
1. Цели и задачи работы
2. Ход работы
3. Написать уравнения реакции катодного восстановления воды с образованием элементарного гидроксид-ионов и реакцию взаимодействии титранта с определяемым веществом. Для обеих реакций привести полное, ионное сокращенное уравнения. Написать анодный и катодные процессы.
4. Привести график зависимости потенциала от времени.
5. Внести результаты измерения в Таблицу 1. и рассчитать среднее время титрования с доверительным интервалом для каждой из аликвот, массу хлороводородной кислоты с помощью закона Фарадея.
Результаты определения тиосульфата натрия
Таблица 1.
|
№ |
Объем пробы, мл |
Время титрования, сек |
Среднее время титрования, сек |
Масса тиосульфата, мг |
Среднее значение, мг |
|
1 |
1 |
|
|
|
|
|
2 |
|
|
|||
|
3 |
|
|
|||
|
4 |
2 |
|
|
|
|
|
5 |
|
|
|||
|
6 |
|
|
6. Расчёт результатов определения соляной кислоты (точность расчётов – 4 значащих цифры, для массы 0,0001 г). Привести расчётные формулы и расчёты, рассчитанные значения занести в таблицы 12.18.
Результаты определения тиосульфата
Таблица 12.18.
|
с(1/1 Н+), моль/дм3 |
T(Н+), г/см3 |
n(Н+), моль |
ν(Н+), моль |
m(Н+), г |
|
|
|
|
|
|
|
с(1/1 HCl), моль/дм3 |
T(HCl), г/см3 |
n(1/1 HCl), моль |
ν(HCl), моль |
m(HCl), г |
|
|
|
|
|
|
7. Расчёт относительной погрешности:
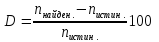
-
Вопросы для самоподготовки
-
В чем различие методов прямой кулонометрии и кулонометрического титрования?
Какие законы лежат в основе метода кулонометрии? Сформулируйте их.
Каковы особенности метода кулонометрического анализа в амперостатическом и потенциостатическом режимах?
Привести принципиальную схему установки для кулонометрического титрования.
Назвать наиболее распространенные способы фиксирования точки эквивалентности в кулонометрическом титровании.
Привести примеры кулонометрического титрования: а) электрогенерированными окислителями; б) электрогенерированными восстановителями; в) с использованием реакций осаждения и комплексообразования; г) с использованием реакций кислотно-основного взаимодействия.
Укажите достоинства и недостатки кулонометрических методов анализа. Чем ограничена область применения этих методов?


