ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 27.03.2024
Просмотров: 153
Скачиваний: 0
СОДЕРЖАНИЕ
Сборник методических указаний к лабораторным работам
Сущность и основы метода ик-спектроскопии
3.4. Определение железа (III) в водных растворах методом градуировочного графика.
3.3. Определение титана (IV) методом градуировочного графика.
3.4. Определение фосфора в водных растворах методом градуировочного графика.
3.5. Определение нитрит-ионов методом градуировочного графика.
1.3. Рефрактометрическое определение сахара в молоке
1. Иономер-кондуктометр; 2. Магнитная мешалка; 3. Кондуктометрический датчик; 4. Ячейка; 5. Бюретка
5. Расчёт относительной погрешности:
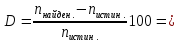
-
Определение железа (II) в присутствии железа (III) методом потенциометрического титровании.
Уравнение титрования железа (II) раствором дихромата калия в молекулярном, полном и сокращенном ионном виде:
FeSO4 + K2Cr2O7
+ H2SO4
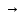 …
…
Факторы эквивалентности.
Закон эквивалентности.
Рассчитать количество вещества FeSO4 в модельной смеси в колбе вместимостью 100 см3.
Ход определения.
Результаты титрования анализируемого раствора дихроматом калия (ориентировочное титрование)
Таблица 12.7.
|
№ точки |
Объем раствора титранта V, см3 |
Значение потенциала Е, мВ |
Значение Е, мВ |
|
|
|
|
|
Результаты титрования анализируемого раствора дихроматом калия (точное титрование)
Таблица 12.7.
|
№ точки |
Объем раствора титранта V, см3 |
Значение потенциала Е. мВ |
Значение Е, мВ |
|
|
|
|
|
|
|
Построение кривых точного титрования
в координатах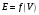 и
и
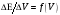 .
.
4. Расчёт результатов определения железа (II) и сульфата железа (II) (точность расчётов – 4 значащих цифры, для массы 0,0001 г). Привести расчётные формулы и расчёты, рассчитанные значения занести в таблицы 12.9.
Результаты определения железа (II) и сульфата железа (II)
Таблица 12.9.
|
с(1/1Fe2+), моль/дм3 |
T(Fe2+), г/см3 |
n(1/1 Fe2+), моль |
ν(Fe2+), моль |
m(Fe2+), г |
|
|
|
|
|
|
|
с(1/1FeSO4), моль/дм3 |
T(FeSO4), г/см3 |
n(1/1 FeSO4), моль |
ν(FeSO4), моль |
m(FeSO4), г |
|
|
|
|
|
|
5. Расчёт относительной погрешности:
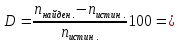
-
Определение железа (III) в растворе
-
Определение железа (III) в растворе ( рабочий электрод - платиновый)
-
1. Уравнение титрования железа (III) раствором ЭДТА в молекулярном, полном и сокращенном ионном виде:
Fe3++ H2Y2-
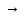 …
…
Факторы эквивалентности.
Закон эквивалентности.
Ход определения.
Результаты титрования железа (III) (ориентировочное титрование, рабочий электрод - платиновый)
Таблица 12.13.
|
№ точки |
Объем раствора титранта V, см3 |
Значение потенциала Е, мВ |
Значение Е, мВ |
|
|
|
|
|
Результаты титрования железа (III) (точное титрование)
Таблица 12.14.
|
№ точки |
Объем раствора титранта V, см3 |
Значение потенциала Е. мВ |
Значение Е, мВ |
|
|
|
|
|
|
|
Построение кривых точного титрования
в координатах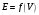 и
и
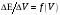 .
.
4. Расчёт результатов определения железа (III) и хлорида железа (III) (точность расчётов – 4 значащих цифры, для массы 0,0001 г). Привести расчётные формулы и расчёты, рассчитанные значения занести в таблицы 12.15.
Результаты определения модельной смеси железа (III) и хлорида железа (III)
Таблица 12.15.
|
с(1/1 Fe3+), моль/дм3 |
T(Fe3+), г/см3 |
n(1/1 Fe3+), моль |
ν(Fe3+), моль |
m(Fe3+), г |
|
|
|
|
|
|
|
с(1/1 FeCl3), моль/дм3 |
T(FeCl3), г/см3 |
n(1/1 FeCl3), моль |
ν(FeCl3), моль |
m(FeCl3), г |
|
|
|
|
|
|
5. Расчёт относительной погрешности:
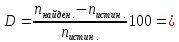

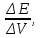 мВ/см3
мВ/см3
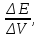 мВ/см3
мВ/см3