Файл: I. Периодический закон, периодическая система химических элементов в свете теории строения атомов.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 26.04.2024
Просмотров: 236
Скачиваний: 0
СОДЕРЖАНИЕ
Тип урока Комбинированный урок.
Тип урока Лабораторно-практическое занятие. Урок закрепление.
Тип урока Комбинированный урок.
Тип урока Лабораторно-практическое занятие. Урок закрепление
Тема занятия: Понятие о скорости химической реакции. Катализаторы. Химическое равновесие
Тип урока: Урок сообщений новых знаний
Тип урока Комбинированный урок.
Тип урока Лабораторно-практическое занятие. Урок закрепление
Тип урока Урок систематизации и обобшения.
Тип урока Комбинированный урок.
Тип урока Комбинированный урок.
Тип урока Комбинированный урок.
Тип урока Лабораторно-практическое занятие. Урок закрепление
Тип урока Лабораторно-практическое занятие. Урок закрепление
Тип урока Комбинированный урок.
Тип урока Лабораторно-практическое занятие. Урок закрепление
Тип урока Контроль знаний и умений.
Тип урока Урок комбинированный.
Тип урока Урок комбинированный.
Тип урока Урок комбинированный.
Тип урока Урок комбинированный.
Тип урока Урок комбинированный.
Тип урока Лабораторно-практическое занятие. Урок закрепление.
Тема занятий Спирты, классификация. Функциональная группа, ее электронное строение
Тема занятий Многоатомные спирты. Получение и применение
Тема занятий Фенол. Строение, физические и химические свойства
Тема занятий Альдегиды.Состав и строение альдегидов. Хиимические свойства и получение.
Тема занятий Карбоновые кислоты, строение.
Тема занятий Физические и химические свойства карбоновых кислот.
Преподаватель_____________А. С. Ингенбаева
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РЕСПУБЛИКИ КАЗАХСТАН
ТАЛДЫКОРГАНСКИЙ КОЛЛЕДЖ СЕРВИСА И ТЕХНОЛОГИИ
ПЛАН ЗАНЯТИЯ №38
| Дата | Группа |
| | С11ЭВМ |
| | С11ПУ |
| | СПМ |
| | П11М |
Предмет Химия
Тема занятие Введение в органическую химию. Особенности органических соединений. Источники органических веществ. Развитие и значение органической химии.
Тип урока Урок новых знаний.
Цель занятия | Учебная: сформирование представлений о составе , |
и строении органических соединений, их отличительных признаках; признаках; выявить причины многообразия органических веществ; | |
признаках; выявить причины многообразия органических веществ; | |
веществ; | |
| Развивающая: продолжить формирование умения составлять | |
| структурные формулы на примере органических веществ. | |
| Воспитательная: воспитывать обучающихся работать | |
группой, организованности, уметь пользоваться | |
учебниками. |
ОБЕСПЕЧЕНИЕ ЗАНЯТИЯ
А. Наглядные пособия Слайды «Особенности органических соединений. Источники органических веществ. Развитие и значение органической химии».
Б. Раздаточные материалы А.Темирбулатова, Н. Н. Нурахметов Химия 11 класс.
| Содержание этапов урока (основные и необходимые методические пояснение и рекомендации) |
| I. Организационные вопросы |
| Организовать группу к занятии. Через дежурных проверить посещаемость |
| обучающихся. |
| II. Повторение пройденного материала (виды контроля знаний) |
| 1. Фронтальная беседа с группой по вопросам. |
| - Какие органические соединения Вы знаете? |
| III. Изложение нового материала (методика) |
| 1.Раздать краткий курс лекций по теме. 2. Показать слайды и объяснять тему с словесным и деманстрационным методом. 3. Записать в тетрадях основные понятия. Органическая химия – наука об органических соединениях и их превращениях. Первоначально органическим считались вещества, найденные в живых организмах и животных.
Но в настоящее время получено очень много новых веществ, которые как считалось ранее образуются только в живых организмах. например: пластмассы, моющие средства, лекарства и многое другое. С органическими веществами человек знаком давно: он употребляет их в пищу, шьёт из них одежду, строит жилища. Первые попытки классификации веществ на органические и неорганические были предприняты ещё в 9-10 веках. Арабский алхимик Абу Бакр ар-Рази впервые разделил вещества на минерального, растительного и животного царства. Такая классификация просуществовала до 19 века. В 19 веке шведский химик Якоб Берцелиус предложил делить вещества на органические и неорганические и предложил раздел химии, изучающий эти вещества назвать органической химией. Подумаем почему он так назвал вещества? Берцелиус был представителем виталистического направления, сторонники этого направления считали, что органические вещества создаются только в живых организмах под действием особой «жизненной силы», получить их в лаборатории нельзя, такие взгляды тормозили развитие науки, но они не могли остановить поступательного процесса познания природы. Органическая химия – это химия соединений углерода.
- Помимо углерода в состав входит элемент водород. Могут еще входить О, S, N и другие элементы.
- Во все перечисленные соединения входит углерод и водород. Они горят. Все органические вещества горят. (C2H5OH), обращает внимание на характер пламени, вносит последовательно в пламя спиртовки и свечи фарфоровую чашку, показывает, что от пламени свечи образуется копоть. (спиртовое пламя бледное, бесцветное, у свечи – яркое, светящееся)
- образоваться может углекислый или угарный газ, чистый углерод ( сажа, копоть ). Уравнение горения органических соединений: СхНу+О2= СО2+Н2О При горении органических веществ образуются углекислый газ и вода. Не все органические вещества способны гореть, но все они разлагаются при нагревании без доступа кислорода, обугливаются. - Приведите примеры из жизни, когда происходит разложение органических веществ, т.е. их обугливание. Например, что происходит с продуктами, содержащими крахмал, белок? - Образуется уголь. Если пережарить картошку, оладьи, блины, хлеб, происходит обугливание крахмала, входящего в состав картофеля и муки. При подгорании яиц или мяса обугливается белок, содержащийся в этих продуктах. |
| ІV. Закреплениев нового материала (выполнение заданий, оценка знаний и др.) |
-(смотрит на формулы органических веществ, написанные на доске). В органических веществах ковалентная полярная связь.
- Сахар начнет плавиться, а поваренная соль останется без изменений.
- Данные вещества имеют разное строение кристаллических решеток.
- В поваренной соли NaCl – ионная кристаллическая решетка, а в сахаре – молекулярная.
-Вещества с ионными кристаллическими решетками имеют более высокие температуры кипения и плавления, чем вещества с молекулярными решетками.
- такие причины, как: соединение углерода в цепи разной длины; соединение атомов углерода простыми, двойными и тройными связями с другими атомами и между собой; множество элементов, входящих в состав органических веществ. - еще одна причина – разный характер углеродных цепей: линейные, разветвленные и циклические, демонстрирует модели бутана, изобутана и циклогексана. в тетради записывают: Причины многообразия органических соединений. 1. Соединиение атомов углерода в цепи разной длины. 2. Образование атомами углерода простых, двойных и тройных связей с другими атомами и между собой.ПОКАЗАТЬ ГОТОВЫЕ СТЕРЖНЕВЫЕ ФОРМУЛЫ ЭТИЛЕНА, АЦЕТИЛЕНА. 3. Разный характер углеродных цепочек: линейные, разветвленные, циклические. 4. Множество элементов, входящих в состав органических веществ. 5. Явление изомерии органических соединений.
- Это было известно с 1823 года. Берцелиус (1830 год) предложил назвать изомерами вещества, имеющие качественный и количественный состав, но обладающие различными свойствами. К примеру, было известно около 80 разнообразных веществ, отвечающих составу C6H12O2. В 1861 году загадка изомерии была разгадана. Определения понятий “химическое строение”, “изомеры” и “изомерия” записываются в тетрадь. Вещества, имеющие одинаковый состав и одинаковую молекулярную массу но различное строение молекул, а поэтому обладающие разными свойствами называются изомерами. Состав органического вещества – С2Н6О. Умение строить структурные формулы изомеров отрабатываются на примерах: C2H6O (этанол и диметиловый эфир), C4H10 (бутан и изобутан). Учитель показывает, как можно записать краткую структурную формулу
Для того, чтобы оценить роль органической химии в нашей жизни, представьте, что станет с нашей жизнью, если из нее исчезнут изделия из дерева, пластмассы, ткани, встанет транспорт из-за отсутствия топлива, исчезнут лекарства, одежда, пища, ну, и мы с вами тоже, поскольку состоим из органических соединений.
|
| V. Домашнее задание |
| Учебник А.Темирбулатовой, Н. Н. Нурахметова «Химия» 11 класс, стр. 30 – 35 прочитать, упр. 1-5 на стр. 33 выполнить в тетрадях. |
| VI. Подведение итогов урока (Выставление оценок с комментарием, выяснение положительных и отрицательных моментов урока) |
| 1. Выставление оценок с комментарием, |
| 2. Выяснение положительные и отрицательные моментов урока |
Преподаватель_____________ А.С.Ингенбаева
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РЕСПУБЛИКИ КАЗАХСТАН
ТАЛДЫКОРГАНСКИЙ КОЛЛЕДЖ СЕРВИСА И ТЕХНОЛОГИИ
ПЛАН ЗАНЯТИЯ №40
| Дата | Группа |
| | С11ЭВМ |
| | С11ПУ |
| | СПМ |
| | П11М |
Предмет Химия
Тема занятие Гомологи и изомеры. Выполнения упражнений на изомерию
Тип урока Урок обобщение.
Цель занятия | Учебная: раскрыть важнейшее положение теории строения , |
| органических соединений А.М.Бутлерова о | |
| взаимозависимости строения | |
и свойств органических веществ на явлении изомерии; | |
| Развивающая: развивать умение выделять существенное | |
через обучение составлению схем; формировать умение | |
сравнивать, классифицировать через выбор формул; | |
| Воспитательная: содействовать в ходе урока формированию | |
| следующих мировоззренческих понятий: причинно- | |
следственные связи, познаваемость мира, развитие природ; |
ОБЕСПЕЧЕНИЕ ЗАНЯТИЯ
А. Наглядные пособия Слайды с заданиями.
Б. Раздаточные материалы Н. Н. Нурахметов, К.Бекишев, Н.А.Заграничная Химия 10 класс.
| Содержание этапов урока (основные и необходимые методические пояснение и рекомендации) | ||
| I. Организационные вопросы | ||
| Организовать группу к занятии. Через дежурных проверить посещаемость | ||
| обучающихся. | ||
| II. Повторение пройденного материала (виды контроля знаний) | ||
| 1. Фронтальная беседа с группой по вопросам. | ||
| 1. Что изучает химия? (Химия – наука о веществах, их свойствах и превращениях) 2. Что такое органическая химия? (Органическая химия есть химия углеводородов и их производных, т.е. продуктов, образующихся при замене водорода другими атомами или группами атомов) 3. Каких веществ больше, органических или неорганических? (Неорганических веществ насчитывается около 100 тыс, органических - 18 млн.) 4. Что лежит в основе многообразия органических веществ? (Причиной многообразия органических веществ являются явления гомологии и изомерии) 5. Что такое гомология? (Гомология - это такое явление при котором существуют вещества, сходные по строению и химическим свойствам, но различающиеся на группу -СН2- , гомологическую разность). Учитель предлагает учащимся самостоятельно по вариантам выполнить задания (3 мин.):
| ||
| III. Изложение нового материала (методика) | ||
| 1.Раздать краткий курс лекций по теме. 2. Показать слайды и объяснять тему с словесным и деманстрационным методом.3. Записать в тетрадях основные понятия. Молекулы каждого из веществ имеют вполне определенное (единственное) строение, которое может быть передано единственной структурной формулой. Если меняется порядок связи в молекуле, то это структурная изомерия. Если изомеры имеют одинаковые заместители у атома углерода, но отличаются их взаимным расположением в пространстве, то это пространственная изомерия.  Самостоятельная работа с учебником. - Какие разновидности структурной изомерии существуют? 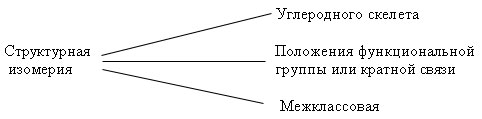 - отличаются ли свойства изомеров? (Вопрос задается к каждой разновидности) Предполагаемый ответ: “Да, свойства веществ определяются не только их количественным и качественным составом, но и порядком соединения атомов в молекуле, т.е. строением вещества” или “Физическими свойствами отличаются, а химическими нет, так как относятся к одному классу веществ”. Изучение случаев изомерии, казавшихся необъяснимыми, привело к возникновению стереохимии — учения о пространственном строении молекул, которое в свою очередь обогатило теорию строения новым содержанием. Основы стереохимии были заложены в 1874 г., когда два малоизвестных химика — голландец Я. Вант-Гофф (22 года) и француз Ж. Ле Бель (27 лет) — одновременно и независимо друг от друга опубликовали свои работы. Обсуждение с помощью графопроектора, проецируется схема:  - Для каких органических соединений характерна геометрическая изомерия? - Какая гибридизация характерна для двойной связи? Какая форма молекулы? - Возможно ли свободное вращение атомов вокруг двойной связи? - Что такое цис-изомер, транс-изомер? Ответы: Геометрическая изомерия характерна для соединений, содержащих двойные связи, и циклических соединений. Для двойной связи характерна sp2-гибридизация. Гибридные орбитали располагаются в одной плоскости под углом 120°. Свободное вращение атомов вокруг двойной связи не возможно, поэтому заместители могут располагаться либо над плоскостью, либо под плоскостью, т.е. по одну сторону (ЦИС-ИЗОМЕР) и по разные стороны (ТРАНС-ИЗОМЕР). | ||
| ІV. Закреплениев нового материала (выполнение заданий, оценка знаний и др.) | ||
| Стр. 49, 7, 8 упр. Выполнить в тетрадях. | ||
| V. Домашнее задание | ||
| Учебник А. Темирбулатовой, Н. Н. Нурахметова «Химия» 11 класс, стр. 45 - 49 прочитать, упр. 8 на стр. 49 выполнить в тетрадях. | ||
| VI. Подведение итогов урока (Выставление оценок с комментарием, выяснение положительных и отрицательных моментов урока) | ||
| 1. Выставление оценок с комментарием, | ||
| 2.Выяснение положительные и отрицательные моментов урока |
Преподаватель_____________А. С. Ингенбаева
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РЕСПУБЛИКИ КАЗАХСТАН
ТАЛДЫКОРГАНСКИЙ КОЛЛЕДЖ СЕРВИСА И ТЕХНОЛОГИИ
ПЛАН ЗАНЯТИЯ №46
| Дата | Группа |
| | С11ЭВМ |
| | С11ПУ |
| | СПМ |
| | П11М |
Предмет Химия
Тема занятие Практическая работа №7 «Изготовление моделей молекул».
Тип урока Лабораторно-практическое занятие. Урок закрепление.
Цель занятия | Учебная: Знать изготовить модели молекул различных |
атомов, собрать шаростерженевые и масштабные модели | |
молекул веществ, правила по технике безопасности при работе | |
работе в кабинете химиии. | |
Развивающая: Уметь практический построить моделей | |
используя детали готовых наборов или пластилин и палочки. | |
| Воспитательная: воспитывать обучающихся работать | |
группой, организованности, уметь пользоваться таблицами. |
ОБЕСПЕЧЕНИЕ ЗАНЯТИЯ
А. Наглядные пособия Видеоопыты «Изготовление моделей молекул».
Б. Раздаточные материалы Н. Н. Нурахметов, К.Бекишев, Н.А.Заграничная Химия 10 класс, инструкции к выполнению практических работ.
| Содержание этапов урока (основные и необходимые методические пояснение и рекомендации) |
| I. Организационные вопросы |
| Организовать группу к занятии. Через дежурных проверить посещаемость |
| обучающихся. |
| II. Повторение пройденного материала (виды контроля знаний) |
| 1. Фронтальная беседа с группой по вопросам. |
| - Какие связи мы называем ковалентной связью? |
| - Какие виды ковалентной связи бывают? |
| - Какие связи мы называем ковалентной неполярной связью? |
| - Какие связи мы называем ковалентной полярной связью? |
| - Какие связи мы называем водородной связью? |
| III. Изложение нового материала (методика) |
- Что нам нужно для выполнения этой работы? - Как мы будем делать эту работу? 2. Показать видеофильм «Изготовление моделей молекул».3. Оформить практическую работу и сделать соответствующие выводы. Практическая работа №1 «Изготовление моделей молекул». Цель работы: Знать изготовить модели молекул различных атомов, уметь собрать шаростерженевые и масштабные модели молекул веществ, соблюдать правилу по технике безопасности при работе в кабинете химиии. Оборудование: пластилин и спичечные палочки. Алгоритм проведения работы: 1. Постройте шаростерженевые и масштабные модели молекул. 2. Для построения моделей используйте детали готовых наборов или пластилин и палочки. 3. Для изготовления модели состоящих из разных атомов, используйте пластилин разных цветов. 4. Соберите шаростерженевые и масштабные модели молекул фтороводорода, хлороводорода, йодоводорода, воды, сероводорода. 5. Ответьте на такие вопросы: Какие связи между атомами этих веществ? Что означает одна палочка между атомами? Какие связи в их молекуле? Сделайте выводы. Заключение: Обратите внимание на атомы: атомы металлов или неметаллы Ход работы:
+1Н 1ē 1S1 +9Ғ 2ē, 7ē ...2S22Р5 •• Н• + •Ғ: → Н: Ғ или Н— Ғ •• В молекуле фтороводорода ковалентно-полярная связь, она имеет линейную форму, так как образуется за счет перекрывания s-орбитали атома водорода с р-орбиталью атома фтора.
+1Н 1ē 1S1 +17Cl 7ē ...3S23Р5 •• Н• + • Cl: → Н: Cl или Н— Cl •• В молекуле хлороводорода ковалентно-полярная связь, она имеет линейную форму, так как образуется за счет перекрывания s-орбитали атома водорода с р-орбиталью атома хлора.
+1Н 1ē 1S1 +53І 7ē ...5S25Р5 •• Н• + •І: → Н: І или Н— І •• В молекуле йодороводорода ковалентно-полярная связь, она имеет линейную форму, так как образуется за счет перекрывания s-орбитали атома водорода с р-орбиталью атома йода.
+1Н 1ē 1S1 +8О 6ē ...2S2 2Р4 •• Н• + •О• + •Н → Н: О: Н или О •• ⁄ \ Н Н В молекуле воды водородная связь, при образовании молекулы воды двух валентный атом кислорода с двумя валентными р-электронами образует с водородом угловую форму молекулы.
+1Н 1ē 1S1 +16S 6ē ...3S23Р4 •• Н• + • S • + •Н → Н: S: Н или S •• ⁄ \ Н Н В молекуле сероводорода ковалентно - полярная связь, при образовании молекулы сероводорода двух валентный атом кислорода с двумя валентными р-электронами образует с водородом угловую форму молекулы. |
| ІV. Закрепление нового материала (выполнение заданий, оценка знаний и др.) |
| 1 – задание |
| Отразите электронную конфигурацию атомов следующих молекул в квантовых ячейках: О2, Ғ2, НВr, N2, ОҒ2. |
| 2 – задание |
| Определите возможные валентности следующих элементов исходя из валентных орбиталей их атомов: цезия, таллия, азота, фтора, селена, неона. |
| 3 – задание При полном сгорании неизвестного вещества массой 0,34г образуются 0,64г оксида серы (IV) 0,18г воды. Определите формулу соединения. |
| V. Домашнее задание |
| Учебник Н. Н. Нурахметова «Химия» 10 класс, 5-37стр. 160-176 прочитать, |
| Подготовиться к контрольной работе по теме «Периодический закон, |
| периодическая система химических элементов в свете теории строения |
| атомов». |
| VI. Подведение итогов урока (Выставление оценок с комментарием, выяснение положительных и отрицательных моментов урока) |
| 1. Выставление оценок с комментарием, |
| 2. Выяснение положительные и отрицательные моментов урока |
Преподаватель_____________А.С.Ингенбаева
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РЕСПУБЛИКИ КАЗАХСТАН
ТАЛДЫКОРГАНСКИЙ КОЛЛЕДЖ СЕРВИСА И ТЕХНОЛОГИИ
ПЛАН ЗАНЯТИЯ №64
| Дата | Группа |
| | С11ЭВМ |
| | С11ПУ |
| | СПМ |
| | П11М |
Предмет химия
Тема занятий Спирты, классификация. Функциональная группа, ее электронное строение
Тип урока урок новых знаний
Цель занятия | Учебная: Обеспечить в ходе урока усвоение общих свойств спиртов. Продолжить формирование умений и навыков составления уравнений химических реакций, характеризующих свойства спиртов. |
Развивающая: Развивать познавательный интерес через использование данных о применении изучаемых явлений. | |
| Воспитательная: Содействовать формированию представлений о причинно-следственных связях (взаимозависимость строения и свойств). |
ОБЕСПЕЧЕНИЕ ЗАНЯТИЯ
А. Наглядные пособия __________________________________________________
Б. Литература основная Нурахметов, Темирболатова. Учебник для 11 класса. «Мектеп»
Цветков Л.А. Органическая химия. Учебник для 10 класса. Просвещение 1990г.
| Содержание этапов урока (основные и необходимые методические пояснения и рекомендации) |
| I. Организационные вопросы |
| Приветствие |
| Подготовка учащихся к восприятию нового материала |
| II. Изложение нового материала (методика) |
|
|
|
|
|
|
| III. Закрепление нового материала (выполнение заданий, оценка знаний и др.) |
|
|
|
|
|
|
| IV. Домашнее задание |
| |
| |


